|
PATOLOGÍA BASADA EN LA EVIDENCIA (PATOLOGÍA BASADA EN PRUEBAS),
GUÍAS DE CONSENSO Y SU APLICACIÓN A LA PRÁCTICA DIARIA
Marcial García
Rojo. Complejo Hospitalario de Ciudad Real. España.
B. TIPOS DE ESTUDIOS CIENTÍFICOS Y BÚSQUEDA DE LA MEJOR EVIDENCIA
(PRUEBAS)
La figura 1 resume los posibles tipos de estudios utilizados en
investigación clínica [9].
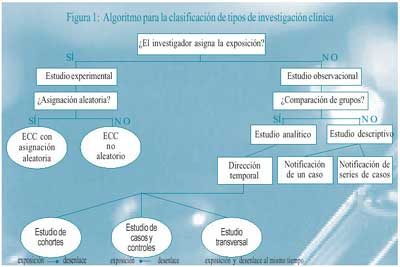
(ECC: Ensayo clínico controlado).
De todos ellos, describiremos las ventajas y desventajas de los
siguientes [10]:
- Estudio caso-control (Case-Control Study)
- Encuesta transversal (Cross-Sectional Survey)
- Estudio de cohortes (Cohort Study)
- Ensayo clínico controlado y randomizado (Randomised
Controlled Trial)
- Diseño de cruce (Crossover Design)
Estudios caso control
Los estudios observacionales de caso-control o retrospectivos
son los realizados a lo largo de un periodo de tiempo recogiendo
información de hechos ocurridos en el pasado. Se inicia el estudio
partiendo de conocer la presencia o no de enfermedad en el presente
y continúan analizando la exposición o no al factor en el pasado
[11].
- Ventajas:
- rápidos y baratos;
- es el único método factible en trastornos infrecuentes o
en aquellos con un largo intervalo entre exposición y
resultados;
- son necesarios menos sujetos que en estudios
transversales.
- Desventajas:
- se basa en recuerdos o en registros de determinados
estados de exposición;
- factores de confunden;
- la selección de grupos control es difícil;
- posibles sesgos: recuerdo, selección.
Encuesta transversal
El estudio transversal es un estudio epidemiológico realizado en
un momento concreto del tiempo.
- Ventajas:
- barato y simple;
- éticamente seguro.
- Desventajas:
- como mucho, establece asociación no causalidad;
- susceptible al sesgo de recuerdo;
- los factores de confunden pueden estar distribuidos
irregularmente;
- sesgo de Nyeman(*);
- el tamaño de los grupos puede ser desigual.
(*) La decisión para inclinarse hacia una u
otra hipótesis implica un riesgo de error. La teoría de Neyman-Pearson
sobre las pruebas estadísticas intenta hacer una valoración
objetiva de este riesgo [12].
Estudio de cohorte
Los estudios observacionales de cohorte o prospectivos son los
realizados a lo largo un periodo de tiempo pero recogiendo
información hacia el futuro. Se inician partiendo de conocer la
exposición o no al factor en el presente entre pacientes sanos y
analizan la presentación o no de la enfermedad en el futuro.
- Ventajas:
- éticamente seguros;
- los sujetos pueden ser emparejados;
- es posible establecer temporalidad y dirección de los
eventos;
- los criterios de selección y la evaluación de resultados
se pueden estandarizar;
- son administrativamente más fáciles y más baratos que los
ensayos randomizados y aleatorizados.
- Desventajas:
- puede ser difícil identificar controles;
- la exposición puede estar relacionada con algún factor de
confusión;
- es difícil cegarlos;
- no existe randomización;
- para las enfermedades raras, son necesarios muestras
grandes o tiempos de seguimiento largos.
Ensayos clínicos controlados y randomizados
Un ensayo clínico es un estudio experimental de tipo sistemático
llevado a cabo en una población o en algún estrato de la misma con
el fin de determinar, generalmente, efectos preventivos o
terapéuticos. Las condiciones del estudio y la distribución de los
individuos en los distintos grupos están controladas por el
investigador.
- Ventajas:
- distribución no sesgada de factores que pueden confundir;
- es más factible el cegarlos;
- la aleatorización facilita el análisis estadístico.
- Desventajas:
- caros: en tiempo y en dinero;
- sesgo de voluntarios;
- a veces, éticamente problemático.
Diseño de cruce
- Ventajas:
- todos los sujetos sirven de sus propios controles y la
varianza del error se reduce, lo que permite reducir el tamaño
de la muestra necesaria;
- todos los sujetos reciben tratamiento (al menos durante
algún tiempo);
- es posible aplicar test que impliquen que se ha realizado
aleatorización;
- es posible mantener el cegamiento.
- Desventajas:
- todos los sujetos reciben placebo o tratamiento
alternativo en algún momento;
- periodo de aclarado largo o desconocido;
- no se puede emplear en tratamientos con efectos
permanentes.
¿Cómo podemos medir la evidencia?
Para medir la evidencia podemos seguir unos criterios detallados
y extensamente desarrollados y consensuados por diversos autores,
que hemos resumido en la tabla 1 para los niveles de evidencia en
diagnóstico, pronóstico y diagnóstico diferencial, siguiendo las
recomendaciones del Centro de Oxford para la Medicina basada en
pruebas [13]. En base a esos criterios, se concluyen unos grados de
recomendación, expresados en la tabla 2.
Otros autores utilizan una escala más sencilla, clasificando los
niveles de evidencia en tres grupos, con un total de cinco niveles
(tabla 3) [14].
Las diversas escalas de niveles de evidencia, jerarquía de
estudios y grados de recomendación han sido previamente revisados y
traducidos al español por otros autores
[15],[16].
Tabla 1. Niveles de evidencia aplicables a
la medicina basada en la evidencia [13]
|
Nivel |
Diagnóstico |
Diagnóstico diferencial /estudios de prevalencia de
síntomas |
Pronóstico |
|
1a |
RS (homogéneas) de
estudios diagnósticos de nivel 1; RDC con estudios 1b de
diferentes centros clínicos |
RS (homogéneas) de
estudios de cohortes prospectivos |
RS (homogéneas) de
estudios de cohortes de inicio; RDC validada en poblaciones
diferentes |
|
1b |
Estudio de cohorte
de validación* con buenos estándares de referencia; o RDC
validada en un centro clínico |
Estudio de cohorte
prospectivo con un buen seguimiento |
Estudio aislado de
cohortes de inicio con > 80% de seguimiento; RDC
validada en una única población |
|
1c |
SpPins y SnNouts
absolutos** |
Series con todos
los casos o con ninguno |
Series con todos
los casos o con ninguno |
|
2a |
RS (homogéneas) de
estudios de diagnóstico de nivel >2 |
RS (homogéneas) de
estudios 2b y mejores |
RS (homogéneas) ya
sea de estudios de cohortes retrospectivos o de grupos de
control no tratados en ECRs. |
|
2b |
Estudio de cohorte
de exploración con buenos estándares de referencia; RDC tras
derivación, o validado sólo en una muestra artificialmente
dividida o en bases de datos. |
Estudios de
cohortes retrospectivos, o con escaso seguimiento |
Estudio de cohorte
retrospectivo o seguimiento se pacientes control no tratados
en un ECR; derivación de RDC o validado sólo en una muestra
artificialmente dividida |
|
2c |
|
Estudios
ecológicos |
Investigación de
"Resultados" |
|
3a |
RS (homogéneas) de
estudios 3b y mejores |
RS (homogéneas) de
estudios 3b y mejores |
|
|
3b |
Estudio no
consecutivo; o sin estándares de referencia aplicados con
coherencia. |
Estudio de
cohortes no consecutivos, o con una población muy limitada |
|
|
4 |
Estudio
caso-control, estándar de referencia pobre o no independiente |
Series de casos o
normas de referencia sustituidas |
Series de casos (y
estudios de cohortes de pronóstico de poca calidad) |
|
5 |
Opinión de experto
sin un enfoque claramente crítico, o basado en fisiología, en
investigación de despacho o en "principios básicos" |
Opinión de experto
sin un enfoque claramente crítico, o basado en fisiología, en
investigación de despacho o en "principios básicos" |
Opinión de experto
sin un enfoque claramente crítico, o basado en fisiología, en
investigación de despacho o en "principios básicos" |
Leyenda
RS: Revisión Sistemática; RDC: Regla de Decisión Clínica
(sistemas de puntuación que permiten una estimación de pronóstico
o de categoría diagnóstica); ECR: Ensayo Clínico Randomizado.
* Los estudios de validación comprueban la calidad de una
prueba diagnóstica determinada, basándose en evidencia anterior.
Un estudio exploratorio recoge información y analiza los datos
(por ej. utilizando un análisis de regresión) para encontrar
aquellos factores que son significativos.
** Un "SpPin absoluto" es un hallazgo diagnóstico cuya eSpecificidad
es tan alta que un resultado Positivo confirma ("rules-in")
el diagnóstico. Un "SnNout absoluto" es un hallazgo diagnóstico
cuya Sensibilidad es tan alta que un resultado Negativo
permite descartar ("rules-out") el diagnóstico.
Tabla 2. Grados de recomendación [13]
|
A |
Estudios de nivel
1 |
|
B |
Estudios de nivel
2 ó 3 o extrapolaciones de estudios de nivel 1 |
|
C |
Estudios de nivel
4 o extrapolaciones de estudios de nivel 2 ó 3. |
|
D |
Evidencia de nivel
5 o estudios inconsistentes o no concluyentes de cualquier
nivel |
Tabla 3. Niveles de evidencia y clasificación
de diseño de investigación [14]
|
I |
Evidencia procedente de ensayo(s)
controlado(s) randomizado(s) |
|
II-1 |
Evidencia procedente de ensayo(s)
controlado(s) sin randomización |
|
II-2 |
Evidencia procedente de cohortes
o estudios analíticos caso-control, preferentemente de más de
un centro o grupo de investigación |
|
II-3 |
Evidencia procedente de
comparaciones entre fechas o lugares con o sin la actuación;
resultados llamativos en experimentos no controlados |
|
III |
Opiniones de autoridades
reconocidas, basándose en la experiencia clínica; estudios
descriptivos o informes de comités de expertos. |
¿Cómo buscar las mejores pruebas en la literatura científica?
Si buscamos trabajos científicos realizados con criterios de
MBE, la mayoría de los autores recomienda el uso de recursos
especializados en MBE como la biblioteca Cochrane o la revista ACP
Journal Club. Estas son las llamadas fuentes secundarias, que se
caracterizan por resumir de forma elaborada los resultados de
muchas búsquedas en la literatura científica y, además seleccionan
(filtran) los trabajos de calidad
[17].
Sólo una pequeña proporción de la literatura médica contiene
avances sólidos en diagnóstico, prevención, tratamiento, causa o
pronóstico de la enfermedad. Para encontrar esos estudios
realmente válidos se han diseñado una serie de herramientas para
una recuperación eficiente y efectiva de información, que
describimos en este artículo.
La estrategia de búsqueda recomendada es la siguiente:
- Formular de forma adecuada la pregunta. Para beneficiar a
los pacientes y a los médicos, la pregunta ha de ser
directamente relevante a los problemas del paciente y debe ser
formulada de forma que la búsqueda permita encontrar respuestas
relevantes y precisas. Una pregunta bien realizada debe contener
cuatro elementos (PICO) (tabla 4).
Tabla 4. Estrategia para formular correctamente una pregunta
cínica
|
|
1
|
2
|
3
|
4
|
|
|
Paciente o
problema
|
Intervención
(causa, factor pronóstico, tratamiento,
)
|
Comparado con
otra intervención
(si es necesario)
|
Outcome
|
|
Trucos para la redacción
|
Empezando con el paciente, pregúntese "¿cómo
describiría yo un grupo de pacientes similar a este paciente?"
Halle el equilibrio entre precisión y brevedad
|
Pregúntese "¿Qué intervención principal
estoy considerando?"
Sea específico
|
Pregúntese "¿Cuál es la principal alternativa
con la que voy a comparar la intervención?"
Sea específico
|
Pregúntese "¿Qué espero conseguir?"
o "¿a qué podría afectar realmente esta exposición?"
Sea específico
|
|
Ejemplo
|
"En pacientes con insuficiencia cardiaca
por miocardiopatía dilatada en ritmo sinusal
"
|
"
¿añadir anticoagulación con warfarina
al tratamiento estándar de la insuficiencia cardiaca
|
si se compara con el tratamiento estándar
aislado
|
conlleva a una menor mortalidad o morbilidad
por tromboembolismo? ¿Es esto suficiente como para justificar
el mayor riesgo de sangrado?
|
- Identificar el tipo de investigación (véase "tipos
de estudios científicos") que más probablemente
permita responder a la pregunta.
- ¿Ha contestado alguien previamente a esa pregunta?
- Busque fuentes secundarias (filtros de calidad y
resúmenes)
- ¿Puede confiar en la calidad del proceso de selección de
estas fuentes?
- ¿Tiene que ir a fuentes primarias en bases de datos
bibliográficas para responder a la pregunta?
- Utilice filtros de búsquedas metodológicos,
disponibles para PubMed
[18] y otras bases de datos
[14]. Por ejemplo, para diagnóstico, los mejores
términos para realizar una búsqueda en PubMed serían:
((((("sensitivity and specificity"[mh] OR
sensitivity[tiab]) OR specificity[tiab]) OR (likelihood
ratio[All Fields] OR likelihood ratios[All Fields])) OR
practice guideline[pt]) OR "likelihood functions"[MeSH Terms])
Existen colecciones de CATs (Critically Appraised
Topics) que recopilan una serie de búsquedas ya
elaboradas [19].
- Asegúrese de obtener las referencias que necesita, valorando
la especificidad y la sensibilidad de los resultados obtenidos.
- La especificidad o precisión se refiere a la proporción
de documentos obtenidos que son relevantes, es decir, la probabilidad
de excluir documentos no relevantes.
Si el resultado de la búsqueda que hemos realizado muestra
un número muy elevado de elementos, lo más seguro es que sea
necesario aumentar la especificidad de la búsqueda, para ello
podemos:
- formular una pregunta más concreta;
- utilizar términos más específicos en la búsqueda por
texto libre;
- utilizar una búsqueda mediante el tesauro (términos
MESH en Pubmed) en vez de texto libre;
- utilizar términos más específicos en el tesauro;
- añadir términos (en Pubmed no es necesario incluir la
palabra AND) que representen otros aspectos de la pregunta;
- especificar el idioma de los artículos, si se limita
a humanos y el tipo de publicación (ensayos controlados
aleatorizados, revisiones, etc.), el país o el año de
publicación.
- La sensibilidad permite valorar la proporción de documentos
relevantes que nuestra búsqueda nos ha permitido localizar,
es decir, la probabilidad de obtener documentos relevantes
o útiles.
Si el resultado de la búsqueda que hemos realizado muestra
un número muy reducido de elementos, probablemente sea necesario
aumentar la sensibilidad:
- formulando una pregunta más genérica;
- incluyendo términos más adecuados que encontremos en
artículos relevantes
- intentando diferentes combinaciones de térmicos
- utilizando comodines (*, ?) en el texto libre o en los
términos del tesauro
- añadiendo términos de significado similar usando OR
- utilizando NEAR entre dos términos que deban estar en
la misma frase
- utilizando una combinación de texto libre y términos
del tesauro
- seleccionando todos los subapartados de los términos
del tesauro (MESH)
- buscando desde una fecha anterior
|