 Nº 867. Comunicación libre
Nº 867. Comunicación libre
|
Jon Celay Leoz[1], Mirja Rotinen Díaz[1], Paula Lazcoz Ripoll[1], Javier Saez Castresana[2], Aranzazu Arrazola Zabaleta[1], Ignacio Encío Martinez[1] |
|
|
9;590;591;592;593;594;595;596;597;598;599;602;603;604;605;606;607;608;609;613;614;615;616;617;618;619;620;622;623;624;625;629;630;631;632;633;634;635;636;637;638;639;640;641;642;643;645;647;648;649;650;652;653;654;655;656;657;658;659;660;661;662;663;664;665;666;667;668;669;670;671;672;673;674;675;676;677;678;679;680;681;682;683;686;687;688;689;690;691;692;693;694;695;696;697;698;699;700;701;702;703;704;706;707;708;709;710;711;712;713;714;715;716;718;719;720;721;722;723;724;725;726;727;728;729;730;731;732;733;734;735;736;737;739;740;741;743;744;745;746;747;748;749;750;751;752;753;754;755;756;757;758;759;760;762;763;764;765;766;767;768;769;770;771;772;773;774;775;776;777;778;779;780;781;782;783;784;785;787;788;789;790;791;792;793;794;795;796;797;798;799;800;801;803;804;805;806;807;811;812;813;814;815;816;817;818;819;820;821;822;823;824;825;826;827;830;831;832;833;834;835;836;837;838;840;841;842;843;844;845;846;847;848;849;850;851;852;853;854;855;856;858;859;860;861;862;863;864;865;866;867;868;869;870;871;872;873;874;875;876;877;878;879;880;881;882;883;884;885;886;888;889;890;891;892;893;894;895;896;897;898;899;900;901;902;903;904;905;906;907;908;909;910;911;913;914;915;916;917;918;919;920;921;922;923;924;925;929;931;934;936;937;939;940;941;942;943;944;945;946;947;948;949;950;951;952;953;954;955;956;957;960;961;962;963;964;965;966;967;968;969;970;971;972;973;974;975;976;977;978;979;980;981;982;983;984;985;986;987;988;989;990;991;992;993;994;995;996;997;998;999;1000;1001;1002;1003;1004;1005;1006;1007;1008;1009;1010;1012;1013;1014;1015;1016;1017;1018;1019;1020;1021;1022;1023;1024;1025;1026;1027;1028;1029;1030;1031;1033;1034;1035;1036;1037;1038;1039;1040;1041;1042;1043;1044;1045;1046;1047;1048;1049;1050;1051;1052;1054;1055;1056;1057;1058;1059;1060;1061;1062;1063;1064;1065;1066;1067;1068;1069;1070;1071;1072;1073;1075;1076;1077;1078;1079;1080;1081;1082;1084;1085;1086;1087;1088;1089;1090;1091;1093;1094;1095;1096;1097;1098;1099;1100;1102;1103;1104;1105;1106;1107;1108;1109;1111;1112;1113;1114;1115;1116;1117;1118;1119;1120;1121;1122;1123;1124;1125;1126;1127;1128;1129;1130;1131;1132;1133;1134;1135;1136;1137;1138;1139;1140;1141;1142;1143;1144;1145;1146;1147;1148;1149;1150;1151;1152;1153;1154;1155;1156;1157;1158;1159;1160;1161;1162;1163;1164;1165;1166;1167;1168;1169;1170;1171;1172;1173;1174;1175;1176;1177;1178;1179;1180;1181;1182;1183;1184;1185;1186;1187;1188;1189;1190;1191;1192;1193;1194;1195;1196;1197;1198;1199;1200;1201;1202;1203;1204;1205;1206;1207;1208;1209;1210;1211;1212;1213;1214;1215;1216;1217;1218;1219;1220;1221;1222;1223;1224;1225;1226;1227;1228;1229;1230;1231;1232;1233;1234;1235;1236;1237;1238;1239;1240;1241;1242;1243;1244;1245;1246;1247;1248;1249;1250;1251;1252;1253;1254;1255;1256;1257;1258;1259;1260;1261;1262;1263;1264;1265;1266;1267;1268;1269;1270;1271;1272;1273;1274;1275;1276;1277;1278;1279;1280;1281;1282;1283;1284;1285;1286;1287;1288;1289;1290;1291;1292;1293;1294;1295;1296;1297;1298;1299;1300;1301;1302;1303;1304;1305;1306;1307;1308;1309;1310;1311;1312;1313;1314;1315;1316;1317;1318;1319;1320;1321;1322;1323;1324;1325;1326;1327;1328;1329;1330;1331;1332;1333;1334;1335;1336;1337;1338;1339;1340;1341;1342;1343;1344;1345;1346;1347;1348;1349;1350;1351;1352;1353;1354;1355;1356;1357;1358;1359;1360;1361;1362;1363;1364;1365;1366;1367;1368;1369;1370;1371;1372;1373;1374;1375;1376;1377;1378;1379;1380;1381;1382;1383;1384;1385;1386;1387;1388;1389;1390;1391;1392;1393;1394;1395;1396;1397;1398;1399;1400;1401;1402;1403;1404;1405;1406;1407;1408;1409;1410;1411;1412;1413;1414;1415;1416;1417;1418;1419;1420;1421;1422;1423;1424;1425;1426;1427;1428;1429;1430;1431;1432;1433;1434;1435;1436;1437;1438;1439;1440;1441;1442;1443;1444;1445;1446;1447;1448;1449;1450;1451;1452;1453;1454;1455;1456;1457;1458;1459;1460;1461;1462;1463;1464;1465;1466;1467;1468;1469;1470;1471;1472;1473;1474;1475;1476;1477;1478;1479;1480;1481;1482;1483;1484;1485;1486;1487;1488;1489;1490;1491;1492;1493;1494;1495;1496;1497;1498;1499;1500;1501;1502;1503;1504;1505;1506;1507;1508;1509;1510;1511;1512;1513;1514;1515;1516;1517;1518;1519;1520;1521;1522;1523;1524;1525;1526;1527;1528;1529;1530;1531;1532;1533;1534;1535;1536;1537;1538;1539;1540;1541;1542;1543;1544;1545;1546;1547;1548;1549;1550;1551;1552;1553;1554;1555;1556;1557;1558;1559;1560;1561;1562;1563;1564;1565;1566;1567;1568;1569;1570;1571;1572;1573;1574;1575;1576;1577;1578;1579;1580;1581;1582;1583;1584;1585;1586;1587;1588;1589;1590;1591;1592;1593;1594;1595;1596;1597;1598;1599;1600;1601;1602;1603;1604;1605;1606;1607;1608;1609;1610;1611;1612;1613;1614;1615;1616;1617;1618;1619;1620;1621;1622;1623;1624;1625;1626;1627;1628;1629;1630;1631;1632;1633;1634;1635;1636;1637;1638;1639;1640;1641;1642;1643;1644;1645;1646;1647;1648;1649;1650;1651;1652;1653;1654;1655;1656;1657;1658;1659;1660;1661;1662;1663;1664;1665;1666;1667;1668;1669;1670;1671;1672;1673;1674;1675;1676;1677;1678;1679;1680;1681;1682;1683;1684;1685;1686;1687;1688;1689;1690;1691;1692;1693;1694;1695;1696;1697;1698;1699;1700;1701;1702;1703;1704;1705;1706;1707;1708;1709;1710;1711;1712;1713;1714;1715;1716;1717;1718;1719;1720;1721;1722;1723;1724;1725;1726;1727;1728;1729;1730;1731;1732;1733;1734;1735;1736;1737;1738;1739;1740;1741;1742;1743;1744;1745;1746;1747;1748;1749;1750;1751;1752;1753;1754;1755;1756;1757;1758;1759;1760;1761;1762;1763;1764;1765;1766;1767;1768;1769;1770;1771;1772;1773;1774;1775;1776;1777;1778;1779;1780;1781;1782;1783;1784;1785;1786;1787;1788;1789;1790;1791;1792;1793;1794;1795;1796;1797;1798;1799;1800;1801;1802;1803;1804;1805;1806;1807;1808;1809;1810;1811;1812;1813;1814;1815;1816;1817;1818;1819;1820;1821;1822;1823;1824;1825;1826;1827;1828;1829;1830;1831;1832;1833;1834;1835;1836;1837;1838;1839;1840;1841;1842;1843;1844;1845;1846;1847;1848;1849;1850;1851;1852;1853;1854;1855;1856;1857;1858;1859;1860;1861;1862;1863;1864;1865;1866;1867;1868;1869;1870;1871;1872;1873;1874;1875;1876;1877;1878;1879;1880;1881;1882;1883;1884;1885;1886;1887;1888;1889;1890;1891;1892;1893;1894;1895;1896;1897;1898;1899;1900;1901;1902;1903;1904;1905;1906;1907;1908;1909;1910;1911;1912;1913;1914;1915;1916;1917;1918;1919;1920;1921;1922;1923;1924;1925;1926;1927;1928;1929;1930;1931;1932;1933;1934;1935;1936;1937;1938;1939;1940;1941;1942;1943;1944;1945;1946;1947;1948;1949;1950;1951;1952;1953;1954;1955;1956;1957;1958;1959;1960;1961;1962;1963;1964;1965;1966;1967;1968;1969;1970;1971;1972;1973;1974;1975;1976;1977;1978;1979;1980;1981;1982;1983;1984;1985;1986;1987;1988;1989;1990;1991;1992;1993;1994;1995;1996;1997;1998;1999;2000;2001;2002;2003;2004;2005;2006;2007;2008;2009;2010;2011;2012;2013;2014;2015;2016;2017;2018;2019;2020;2021;2022;2023;2024;2025;2026;2027;2028;2029;2030;2031;2032;2033;2034;2035;2036;2037;2038;2039;2040;2041;2042;2043;2044;2045;2046;2047;2048;2049;2050;2051;2052;2053;2054;2055;2056;2057;2058;2059;2060;2061;2062;2063;2064;2065;2066;2067;2068;2069;2070;2071;2072;2073;2074;2075;2076;2077;2078;2079;2080;2081;2082;2083;2084;2085;2086;2087;2088;2089;2090;2091;2092;2093;2094;2095;2096;2097;2098;2099;2100;2101;2102;2103;2104;2105;2106;2107;2108;2109;2110;2111;2112;2113;2114;2115;2116;2117;2118;2119;2120;2121;2122;2123;2124;2125;2126;2127;2128;2129;2130;2131;2132;2133;2134;2135;2136;2137;2138;2139;2140;2141;2142;2143;2144;2145;2146;2147;2148;2149;2150;2151;2152;2153;2154;2155;2156;2157;2158;2159;2160;2161;2162;2163;2164;2165;2166;2167;2168;2169;2170;2171;2172;2173;2174;2175;2176;2177;2178;2179;2180;2181;2182;2183;2184;2185;2186;2187;2188;2189;2190;2191;2192;2193;2194;2195;2196;2197;2198;2199;2200;2201;2202;2203;2204;2205;2206;2207;2208;2209;2210;2211;2212;2213;2214;2215;2216;2217;2218;2219;2220;2221;2222;2223;2224;2225;2226;2227;2228;2229;2230;2231;2232;2233;2234;2235;2236;2237;2238;2239;2240;2241;2242;2243;2244;2245;2246;2247;2248;2249;2250;2251;2252;2253;2254;2255;2256;2257;2258;2259;2260;2261;2262;2263;2264;2265;2266;2267;2268;2269;2270;2271;2272;2273;2274;2275;2276;2277;2278;2279;2280;2281;2282;2283;2284;2285;2286;2287;2288;2289;2290;2291;2292;2293;2294;2295;2296;2297;2298;22 El neuroblastoma es el tumor pediátrico más frecuente y se caracteriza por la amplificación del protooncogén MYCN. El tratamiento de líneas celulares de neuroblastoma con ácido retinoico (RA) induce una diferenciación y/o apoptosis celular. En este trabajo se ha tratado la línea celular IMR-32 con las isoformas 9-cis y todo trans del ácido durante 5 o 9 días. Tras el tratamiento se analizó el efecto sobre la viabilidad celular y el nivel de expresión de los genes MYCN, RET, MST1, Rb1 e ID2, que participan en diversas vías de diferenciación y/o apoptosis. El tratamiento de estas células con RA induce un aumento en el nivel de expresión de RET y Rb1 y una disminución de la expresión de ID2 y MYCN, indicando una disminución de la proliferación celular y/o la entrada de las células en un proceso de diferenciación. El nivel de expresión de MST1, en cambio, no varía significativamente, por lo que la vía controlada por efectores de Ras podría no verse afectada por el tratamiento con RA. Además, el tratamiento continuado de la línea IMR-32 con RA induce un aumento en el nivel de apoptosis celular, y este aumento desaparece al suspender el tratamiento.
|
||
|
|
El neuroblastoma es el tumor extracraneal sólido maligno más frecuente en la edad pediátrica, y se caracteriza por una interrupción temprana del proceso de diferenciación celular (1). La amplificación del proto-oncogén MYCN es la alteración genética más frecuente en neuroblastoma. MYCN promueve la proliferación, el crecimiento celular y la síntesis proteica, y, en líneas en las que está amplificado, también promueve la apoptosis celular (2). Con el fin de inducir diferenciación y/o apoptosis en líneas celulares de neuroblastoma se han analizado diferentes compuestos y se ha observado que los tratamientos con diferentes isómeros del ácido retinoico (RA) dan lugar a una reducción de la población celular tratada (3). Los mecanismos moleculares que controlan el proceso son poco conocidos y parecen específicos del programa de diferenciación escogido. Así, mientras en la línea celular de leucemia promielocítica HL-60 el tratamiento con RA induce la expresión de la proteína proapoptótica Mst1 (4), en la de carcinoma embrionario F9 disminuye los niveles de expresión del inhibidor de diferenciación ID2 (5). Por su parte, el tratamiento de líneas celulares de neuroblastoma como LA-N-5 y SH-SY5Y con RA induce un aumento en el nivel de expresión de RET y de su ligando GDNF (6, 7 y 8) y una disminución de la expresión de MYCN. RET codifica un receptor de membrana con actividad tirosina kinasa que juega un papel importante en el desarrollo del sistema nervioso y se emplea como marcador temprano de diferenciación celular. Por ello, los aumentos de su expresión en respuesta al tratamiento con RA en líneas de neuroblastoma indican que el RA tiene capacidad de inducir diferenciación y neuritogénesis en estas líneas. A su vez, la expresión exógena de MYCN en líneas celulares de neuroblastoma con amplificación de MYCN produce como resultado un bloqueo de la diferenciación inducida por el RA en estas líneas. Sin embargo la capacidad de diferenciarse de las células de neuroblastoma no se ve afectada in vivo por la elevación en los niveles de expresión de MYCN, ya que estos niveles no se correlacionan con el estadío de diferenciación de los neuroblastomas. Ya que la amplificación de MYCN induce un aumento importante en la expresión del gen ID2, un represor transcripcional capaz de enlazar con la pRb1 y suprimir su efecto antiproliferativo, se ha sugerido la existencia de una posible correlación entre la amplificación de MYCN y la pérdida de la función de la pRb1 (9). Junto a su interacción con la pRb1 también se ha descrito que ID2 puede inducir apoptosis en células 32D.3, y se ha podido comprobar que la apoptosis mediada por ID2 es independiente de su interacción con otras proteínas de la familia HLH y está relacionada con aumentos en la expresión de Bax (10). La expresión exógena de MYCN también favorece la apoptosis celular mediada por compuestos como el IFN-γ, TRAIL o FasL. Por este motivo, parece razonable pensar que la amplificación de MYCN en neuroblastoma debería aumentar la sensibilidad de la célula a factores inductores de apoptosis (11). Sin embargo, muchas líneas de neuroblastoma sobreexpresan MYCN pero no entran en apoptosis espontáneamente o tras estimulación, sino que son muy resistentes a la inducción por TRAIL (12). Estos datos, junto con la asociación de la amplificación de MYCN con expectativas de supervivencia pobres en neuroblastomas nos han llevado a analizar el efecto del tratamiento con RA sobre la inducción de diferenciación y/o apoptosis inducida en células IMR-32 y su relación con el estado de expresión y función de los genes MYCN, Rb1, ID2, RET y MST1.
|
|
|
|
Cultivo celular Las células IMR-32 se cultivaron en frascos de 75 cm2 en medio DMEM Glutamax suplementado con suero bovino fetal descomplementado al 10%, aminoácidos no esenciales al 5% y 5 μg/ml de Plasmocín. Las células se trataron con 9-cis RA o at-RA a una concentración final de 1 mM, durante 9 días consecutivos, o durante 5 días seguidos de 4 días de cultivo en ausencia de RA. El medio de cultivo se cambió a las 24 horas de tratamiento y se realizaron cambios adicionales cada 48 horas. En los cambios se conservaron las células apoptóticas recogiéndolas por centrifugación y añadiéndolas junto con el nuevo medio Apoptosis La viabilidad celular se determinó por citometría de flujo mediante la técnica TUNEL, ya que cuando una célula entra en apoptosis se producen roturas en el DNA, y mediante esta técnica estas roturas son reparadas enzimáticamente, de forma que se añaden nucleótidos marcados con el fluorocromo FITC en los puntos de rotura. Una vez marcadas las células éstas se analizaron mediante citometría de flujo. Expresión génica Los estudios de expresión génica se llevarán acabo por PCR a tiempo real. La expresión se cuantificó de forma relativa por comparación con la del GAPDH, empleando la técnica de los -∆∆Ct. En los experimentos se utilizó como agente intercalante el SYBR Green I (Stratagene), Como cebadores se utilizaron los oligonucleótidos GAPDH (Sentido:
|
|
|
|
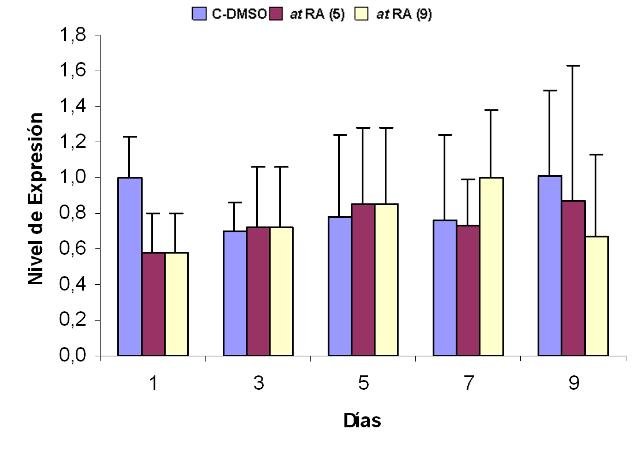
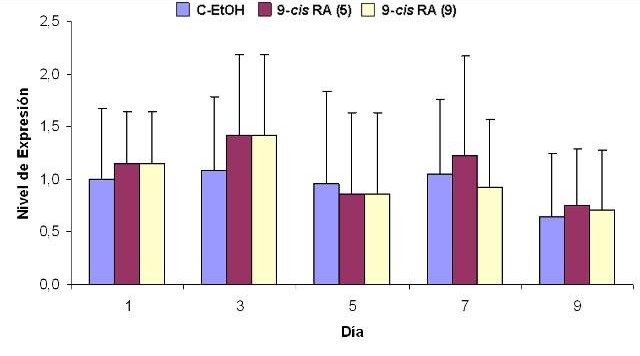
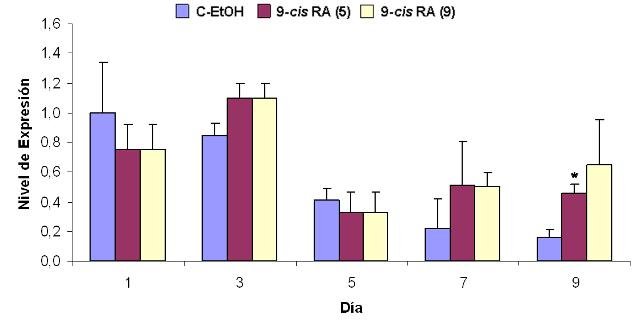
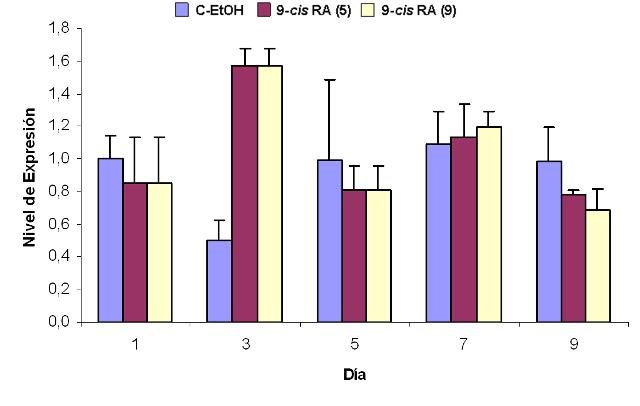
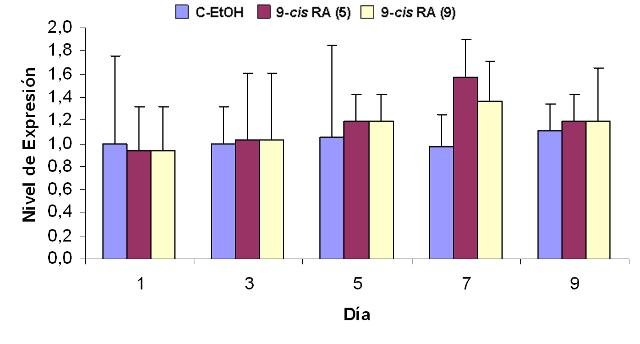
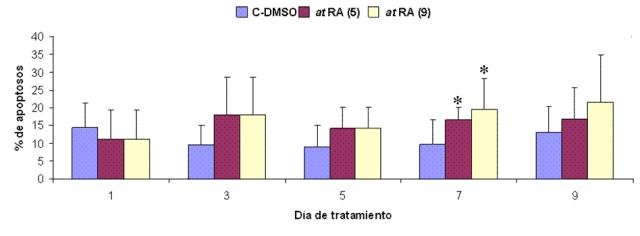
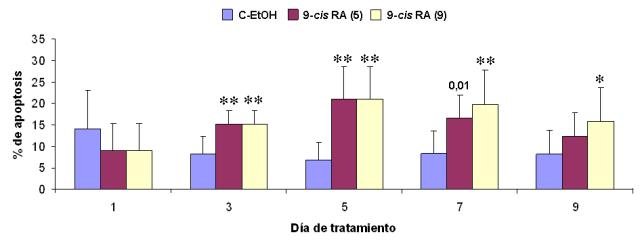
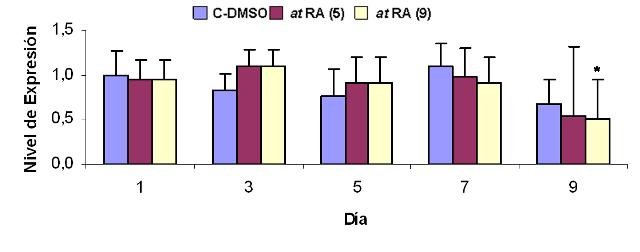
El tratamiento de la línea celular IMR-32 con los isomeros 9-cis o at-RA a concentración 1 µM induce en las células un proceso de diferenciación que se manifiesta con aumentos en la expresión del marcador de diferenciación RET. Este aumento que llega a alcanzar valores de hasta 60 veces en el caso del tratamiento isómero 9-cis (Figura1)y de entre 11 y 13 veces en él del isómero todo-trans (Figura 2), se observa desde el primer día de tratamiento y se mantiene mientras éste persista. Además, el tratamiento con el isómero at-RA disminuye significativamente los niveles de expresión de los genes MYCN e ID2, aumenta el del gen Rb1 y no modifica el del gen MST1 (Figuras 3 a 6). Por su parte, el tratamiento con el isómero 9cRA no modifica significativamente el nivel de expresión de estos genes (Figuras 7 a 10). A su vez, el tratamiento de la línea celular IMR-32 con los isómeros 9-cis o at-RA a concentración 1 mM induce un aumento significativo en el nivel de apoptosis celular, aunque ambos isómeros difieren en su capacidad para inducir la apoptosis. Así, el isómero at-RA induce la apoptosis de forma lenta y progresiva, por lo que sus efectos sólo se manifiestan a largo plazo (Figura 11), mientras que el isómero 9-cis RA lo hace de forma más rápida, pero menos persistente (Figura12).
|
|
|
|
|
|
|
|
1 - van Noesel MM, Versteeg R. Pediatric neuroblastomas: genetic and epigenetic 'danse macabre'. Gene. 2004 Jan 21;325:1-15. Review. 2 - Schwab M, Alitalo K, Klempnauer KH, Varmus HE, Bishop JM, Gilbert F, Brodeur G, Goldstein M, Trent J. Amplified DNA with limited homology to myc cellular oncogene is shared by human neuroblastoma cell lines and a neuroblastoma tumour. Nature. 1983 Sep 15-21;305(5931):245-8. 3 - Sleigh MJ. Differentiation and proliferation in mouse embryonal carcinoma cells. Bioessays. 1992 Nov;14(11):769-75. Review. 4 - Lu ML, Sato M, 5 - H. Kindregan, S. Ohno, S.M. Niles, Characterization of conventional PKC isotype expression during F9 teratocarcinoma differentiation: overexpression of PKC_ alters the expression of some differentiation-dependent genes, J. Biol. Chem. 269 (1994) 2775627761. 6 - Acheson A, Conover JC, Fandl JP, DeChiara TM, Russell M, Thadani A, Squinto SP, Yancopoulos GD, Lindsay RM. A BDNF autocrine loop in adult sensory neurons prevents cell death. Nature. 1995 Mar 30;374(6521):450-3. 7 - Bunone G, Borrello MG, Picetti R, Bongarzone I, Peverali FA, de Franciscis V, Della Valle G, Pierotti MA. Induction of RET proto-oncogene expression in neuroblastoma cells precedes neuronal differentiation and is not mediated by protein synthesis. Exp Cell Res. 1995 Mar;217(1):92-9. 8 - D'Alessio A, De Vita G, Cali G, Nitsch L, Fusco A, Vecchio G, Santelli G, Santoro M, de Franciscis V. Expression of the RET oncogene induces differentiation of SK-N-BE neuroblastoma cells. Cell Growth Differ. 1995 Nov;6(11):1387-94. 9 - Lasorella A, Noseda M, Beyna M, Yokota Y, Iavarone A. Id2 is a retinoblastoma protein target and mediates signalling by Myc oncoproteins. Nature. 2000 Oct 5;407(6804):592-8. Erratum in: Nature 2000 Nov 23;408(6811):498. 10 - Florio M, Hernandez MC, Yang H, Shu HK, Cleveland JL, Israel MA. Id2 promotes apoptosis by a novel mechanism independent of dimerization to basic helix-loop-helix factors. Mol Cell Biol. 1998 Sep;18(9):5435-44. 11 - van Noesel MM, Pieters R, Voute PA, Versteeg R. The N-myc paradox: N-myc overexpression in neuroblastomas is associated with sensitivity as well as resistance to apoptosis. Cancer Lett. 2003 Jul 18;197(1-2):165-72. 12 - Teitz, T., Wei, T., Valentine, M.B., Vanin, E.F., Grenet, J., Valentine, V.A., Behm, F.G., Look, A.T.,
|
|
|
|
|
|
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 17:19:20
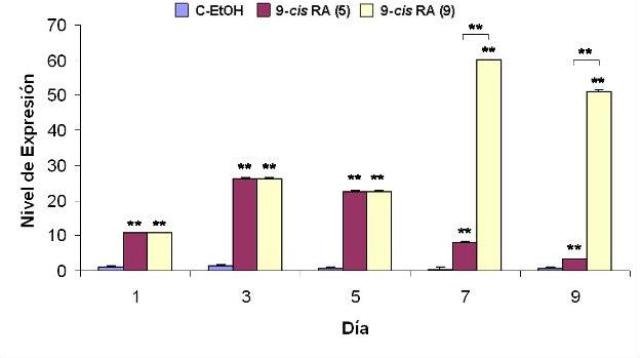 fiogf49gjkf0dFigura 1. Efecto del tratamiento con 9-cis RA sobre la expresión de RET en células IMR-32. Se representan los niveles de expresión relativa de RET con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al 9-cis RA durante 9 días. (5) indica exposición al 9-cis RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (**, p< 0,01).">
fiogf49gjkf0dFigura 1. Efecto del tratamiento con 9-cis RA sobre la expresión de RET en células IMR-32. Se representan los niveles de expresión relativa de RET con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al 9-cis RA durante 9 días. (5) indica exposición al 9-cis RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (**, p< 0,01).">
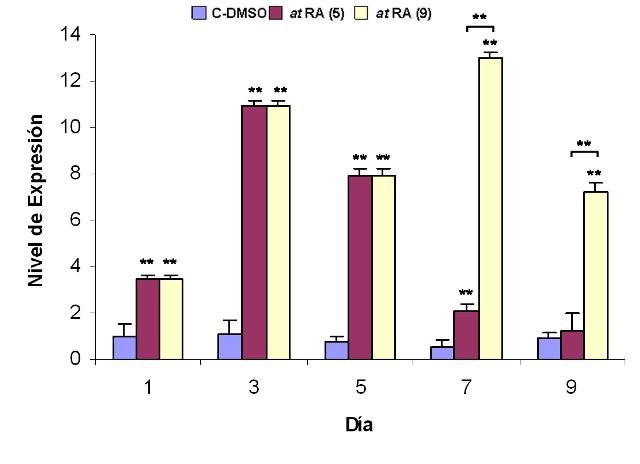 fiogf49gjkf0dFigura 2. Efecto del tratamiento con at RA sobre la expresión de RET en células IMR-32. Se representan los niveles de expresión relativa de RET con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al at RA durante 9 días. (5) indica exposición al at RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (*, p< 0,05; **, p< 0,01).">
fiogf49gjkf0dFigura 2. Efecto del tratamiento con at RA sobre la expresión de RET en células IMR-32. Se representan los niveles de expresión relativa de RET con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al at RA durante 9 días. (5) indica exposición al at RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (*, p< 0,05; **, p< 0,01).">
 fiogf49gjkf0dFigura 3. Efecto del tratamiento con at-RA sobre la expresión de MYCN en células IMR-32. Se representan los niveles de expresión relativa de MYCN con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al at RA durante 9 días. (5) indica exposición al at RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (*, p< 0,05; **, p< 0,01).">
fiogf49gjkf0dFigura 3. Efecto del tratamiento con at-RA sobre la expresión de MYCN en células IMR-32. Se representan los niveles de expresión relativa de MYCN con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al at RA durante 9 días. (5) indica exposición al at RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (*, p< 0,05; **, p< 0,01).">
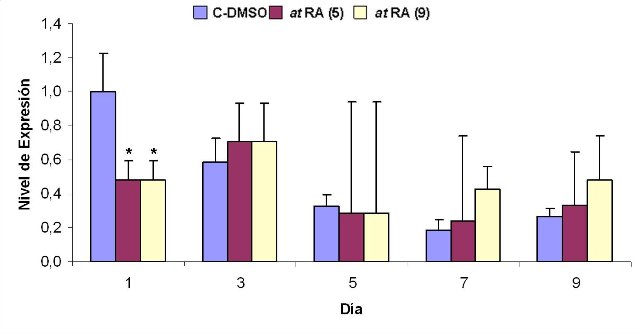 fiogf49gjkf0dFigura 4. Efecto del tratamiento con at RA sobre la expresión de ID2 en células IMR-32. Se representan los niveles de expresión relativa de ID2 con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al at RA durante 9 días. (5) indica exposición al at RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (*, p< 0,05).">
fiogf49gjkf0dFigura 4. Efecto del tratamiento con at RA sobre la expresión de ID2 en células IMR-32. Se representan los niveles de expresión relativa de ID2 con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al at RA durante 9 días. (5) indica exposición al at RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (*, p< 0,05).">
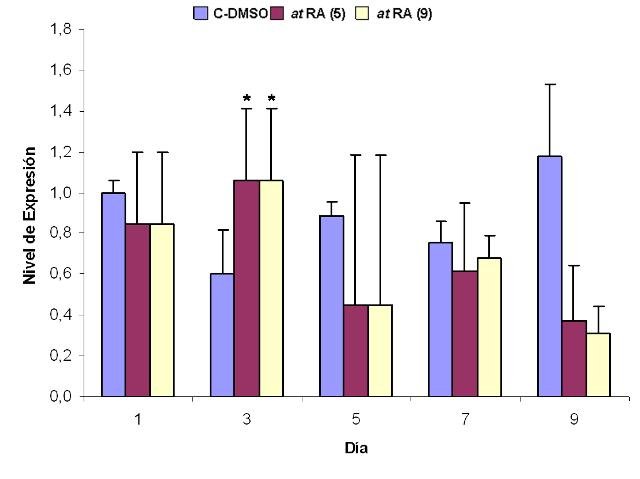 fiogf49gjkf0dFigura 5. Efecto del tratamiento con at RA sobre la expresión de Rb1 en células IMR-32. Se representan los niveles de expresión relativa de Rb1 con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al at RA durante 9 días. (5) indica exposición al at RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (*, p< 0,05).">
fiogf49gjkf0dFigura 5. Efecto del tratamiento con at RA sobre la expresión de Rb1 en células IMR-32. Se representan los niveles de expresión relativa de Rb1 con respecto al control interno GAPDH (expresados como 2-ΔΔCt) frente a los días de tratamiento. (9) indica exposición al at RA durante 9 días. (5) indica exposición al at RA durante los 5 primeros días de tratamiento. Los valores que se muestran (media ± SEM) se calcularon a partir de los resultados obtenidos tras la realización de 3 experimentos realizados por triplicado. Los asteriscos indican diferencias significativas con respecto al control en cada día de tratamiento (*, p< 0,05).">