
 Nº 768. Foro técnico
Nº 768. Foro técnico
|
Biopsia de medula ósea extracción y procesamiento en el laboratorio de anatomía patologica Francisco Borja Gutierrez Corres (TEAP)[1], Consuelo Izcara Melgosa (DUE)[1], Consuelo Del Campo Clemente (TEAP)[2], Elisa Cuero Ruiz (TEAP)[2], Maria Perez de Albeniz Vesga (DUE)[3], Maria Gloria Diaz Foncea (DUE)[2] |
||
|
lay:none">fiogf49gjkf0d
La medula ósea es un tipo de tejido que se encuentra en las cavidades de los huesos del organismo y se encarga de producir componentes de la sangre (hematopoyesis), porque contiene las células madre que originan los tres tipos de células sanguíneas: leucocitos (elementos principales del sistema inmunológico del organismo), hematíes y plaquetas.
El examen de medula ósea es un procedimiento diagnostico especializado de suma importancia no solo para la evaluación y manejo de desordenes hematológicos malignos y no malignos, sino también para el seguimiento de neoplasias hematológicas y tumores sólidos.
Material y métodos
- Extracción de la muestra
- Fijación y decalcificación
- Procesamiento, confección de bloque y corte.
- Tinciones de rutina.
-Hematoxilina-eosina
-Giemsa
-Técnica de PAS
-Técnicas de impregnación argéntica de Gordon-sweet para fibras reticulares
-Técnica de Azul de Perls
- Montaje de las muestra
Conclusiones
Para obtener unos resultados adecuados, debemos seguir una serie de normas y precauciones a lo largo de todo el procesamiento de la biopsia de medula ósea.
|
||
|
|
La medula ósea es un tipo de tejido que se encuentra en las cavidades de los huesos del organismo y se encarga de producir componentes de la sangre (hematopoyesis), porque contiene las células madre que originan los tres tipos de células sanguíneas: leucocitos (elementos principales del sistema inmunológico del organismo), hematíes y plaquetas. La medula ósea puede ser de dos tipos: -Medula ósea roja, que ocupa el tejido esponjoso de los huesos planos, como el esternón, las vértebras, la pelvis y las costillas. -Medula ósea amarilla, que es el tejido adiposo y se localiza en los canales medulares de los huesos largos. El examen de medula ósea es un procedimiento diagnostico especializado de suma importancia no solo para la evaluación y manejo de desordenes hematológicos malignos y no malignos, sino también para el seguimiento de neoplasias hematológicas y tumores sólidos. La extracción de la medula ósea se realiza en los huesos planos. Los más habituales son el manubrio esternal y cresta iliaca anterior y posterior. También se puede realizar en las costillas, vértebras. Si queremos extraer una biopsia ósea es mejor realizarla después de la aspiración y en un lugar distinto, pues la estructura de la medula ósea puede ser alterada después de la aspiración
|
|
|
|
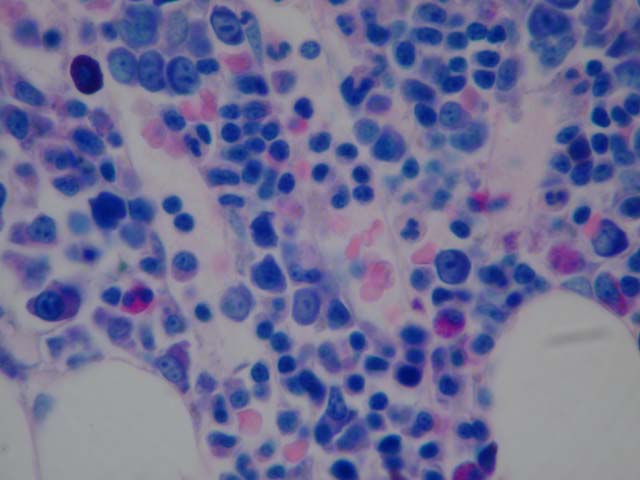
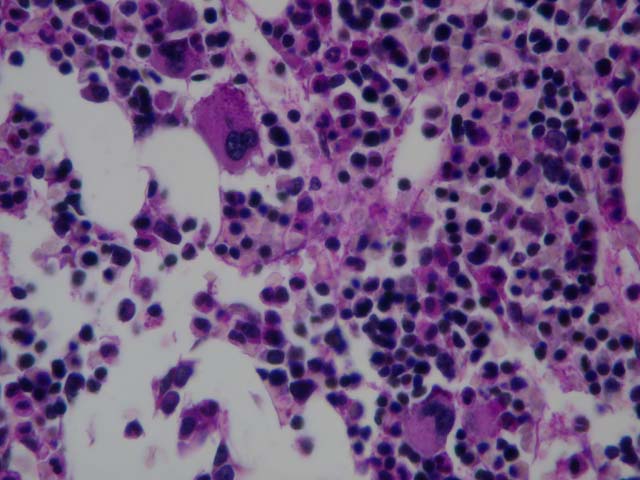
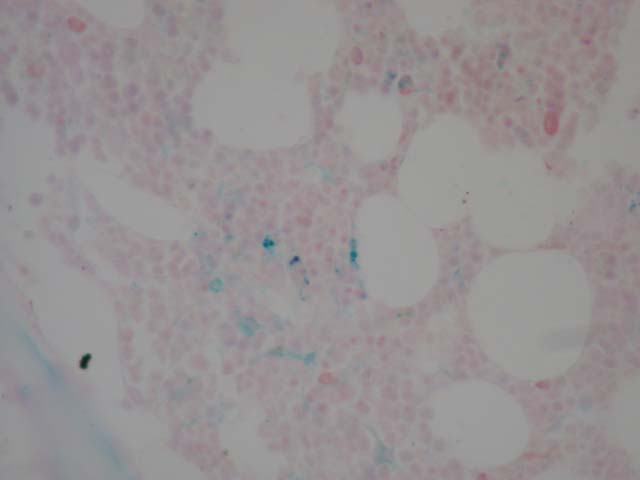
Método de extracción de la muestra Una vez elegida la zona, se realiza una desinfección y se anestesia la zona con anestesia local. Se introduce una aguja d e 15 G. Tras pasar la cortical se realiza un aspirado con jeringa y se deposita la parte de medula ósea en un vidrio de reloj para hacer extensiones en los portaobjetos y preparados para realizar posteriormente las tinciones oportunas en el departamento de hematológica sección citoquímica, según el criterio diagnostico. Una vez realizada la aspiración se adentra más en el hueso, para conseguir una toma del mismo y después de la extracción se introduce en líquido de Bouin y se remite al servicio de anatomía patológica. Fijación y decalcificación Se recibe la muestra de medula ósea del departamento de hepatología con su correspondiente hoja de estudio anatomo-patológico, en la cual viene referenciada con los datos del paciente, material remitido y la sospecha clínica. La muestra que envían viene fijada desde la extracción en liquido de Bouin, este liquido actúa como fijador estructural, por su contenido de ácido pícrico actúa coagulando las proteínas a través de la formación de picratos. El liquido de Bouin tiene poder de descalcificación, pero hay que evitar que el tejido no este en esta solución mas de 48 horas. Liquido de Bouin: -Solución acuosa saturada de ácido pícrico (Ácido pícrico 2% en agua destilada) 750 ml. -Formol 40% 250 ml. -Ácido acético glacial 50 ml. Antes de su procesamiento automático se realizara una prueba por métodos físicos del control del grado de decalcificacion tisular y después un lavado con alcohol de 70º para eliminar los restos amarillentos de ácido pícrico. Procesamiento, confección de bloque y corte. El procesamiento se realiza automáticamente (Leica TP 1050) con sistema de vació. La realización del bloque se realiza en una estación e inclusión, colocando eje mayor de la muestra paralela a la superficie de corte, con un ángulo leve de inclinación. Esta comenzara el corte con menos resistencia, reduciendo así la posibilidad de desplazar el tejido fuera del bloque y la vibración e inestabilidad del borde de la cuchilla o del bloque también se minimizan notablemente. Después de confeccionado el bloque se colocara este, en una placa de frió para su posterior corte por medio de micrótomo de rotación o tipo minot. Se realizaran varios cortes de entre 3 a 5 micras. El secado de las preparaciones después de realizar los cortes, se introducirán en una estufa a 60ª C durante 24 horas. Tinciones de rutina. Hematoxilina-eosina Esta técnica advierte del patrón arquitectural del crecimiento, identifica los característicos nucleolos, que definen a las células de Stermberg-red en la enfermedad de Hodgkin y los diversos matices de basofilia citoplasmáticas d los elementos de diferenciación plamocitica. Soluciones: -Hematoxilina de Harris (Merck). -Eosina acuosa 1%. -Alcohol-clorhídrico 0.5%. Procedimiento: 1.- Desparafinar e hidratar 2.-Solución hematoxilina de Harris . .5 minutos 3.-Agua corriente. 4.-Diferenciar con solución alcohol-clorhídrico 0.5%..........2 pases 5.-Azulear con agua corriente caliente. 6.-Solución eosina 1%...........................................................1 minuto. 7.-Lavar con agua corriente. 8.-Deshidratar, aclara y montar. Resultados: Núcleos .Azul. Citoplasma Rosado a rojo. Restantes estructuras .Rosado a rojo. Giemsa Con esta técnica nos permite identificar notablemente los infiltrados de granulocitos eosinofilos y mastocitos por su carácter metacromático. Soluciones: -Solución Giemsa comercializada (Azur eosina-azul de metileno según Giemsa-Merck) al 35 % en agua destilada. -Agua acética al 1%. Procedimiento: 1.- Desparafinar e hidratar 2.-Solución Giemsa comercializada 2 horas. 3.- Diferenciar con agua acética 1%.........................................2 pases. 4.- Deshidratar con alcohol absoluto. 5.-Aclara y montar. Resultados: Citoplasma .... .Rosa. Núcleos ......Azul. Eritrocitos ..Rojo. Gránulos de células cebadas ..Púrpura. Técnica de PAS Identifica los elementos en diferenciación hacia células plasmáticas (inclusiones PAS+) Soluciones: -Solución acuosa de ácido periódico 0.8% -Reactivo de Shiff comercializado ( Schiff´s reagent fuchisin-sulfite reagent Sigma-Aldrich.) -Hematoxilina de Harris. -Solución Alcohol-clorhídrico 0.5%. Procedimiento: 1.- Desparafinar e hidratar 2.-Solución acuosa de ácido periódico 0.8%.....................................................5 minutos. 3.-Agua corriente. 4.-Reactivo de Shiff comercializado.................................................................30 minutos. 5.-Lavar con agua caliente. 6.-Hematoxilina de Harris 5 minutos. 7.-Lavar con agua corriente. 8.-Diferenciar con solución alcohol clorhídrico 2 pases. 9.-Lavar con agua corriente caliente. 10.-Deshidratar, aclara y montar. Resultados: Núcleos .. .Azul. Material PAS positivo Rojo oscuro a magenta. Técnicas de impregnación argéntica de Gordon-sweet para fibras reticulares Sirve para identificar las perdidas de arquitectura ganglionar que denota infiltración por una neoplasia y para reconocer las zonas de nodularidad, que otorgan los linfomas no Hodgkin. Soluciones: -Solución acuosa de permanganato potasico 2%. -Solución acuosa de ácido oxálico 5%. -Solución acuosa de alumbre férrico 2%. -Solución acuosa de cloruro de oro 0.2%. -solución acuosa de hiposulfito sodico 5%. -Formol tamponado 10%. -Solución de plata amoniacal: -Solución acuosa de nitrato de plata al 10%...........10 cc. -Solución acuosa de hidróxido sodico 10%...............2cc. Se mezclan estas dos soluciones y se añade gota a gota amoniaco, hasta disolver el precipitado. -Medir la mezcla y añadir la misma cantidad de agua destilada. Procedimiento: 1.- Desparafinar e hidratar 2.-Solución acuosa de permanganato potasico.....................................................1 minuto. 3.-Lavar en agua corriente. 4.-Blanquear con solución acuosa de ácido oxálico. 5.-Lavar en agua corriente. 6.-Mordentaje con solución acuosa de alumbre ferrico .. .2 minutos. 7.-Lavar en agua corriente 8.-Solución de plata amoniacal ... 2 minutos. 9.-Lavar en agua destilada 10.-Reducción con formol tamponado al 10% 11.-Lavar en agua destilada. 12.-Realizar un viraje con la solución acuosa cloruro de oro 2minutos. 13.- Lavar en agua destilada. 14.-Fijar la coloración con la solución acuosa de hiposulfito sodico .5 minutos. 15.- Lavar en agua destilada. 16.-Deshidratar y montar. Resultados: Fibras reticulares ..negras. Técnica de Azul de Perls Tiene como utilidad la identificación de hierro ferrico. Soluciones: -Solución acuosa de ferrocianuro potasico 20%. -Solución acuosa de ácido clorhídrico 2%. -Solución de rojo nuclear extra. -Rojo nuclear .. ..0.2 gr. -Solución acuosa de sulfato de aluminio al 5%.....100 cc. Procedimiento: 1.- Desparafinar e hidratar 2.-Solución acuosa de ferrocianuro potasico y ácido clorhídrico 2% a partes iguales ..................................................30 minutos. 3.-Lavar con agua corriente. 4..-Solución de rojo nuclear extra.................................................................10 minutos. 5.-Lavar con agua corriente. 6.-Deshidratar, aclara y montar. Resultados: Núcleos .. .Rojo. Hierro ferrico incluida la hemosiderina .Azul. Montaje de las muestra Por medio automático (Tissue-Tk sca-Sakura) con rollos de film.
|
|
|
|
|
|
|
|
Para obtener unos resultados adecuados, debemos seguir una serie de normas y precauciones a lo largo de todo el procesamiento de la biopsia de medula ósea: 1.- Es aconsejable que el cilindro óseo tenga unas dimensiones mininas 2 por 0.2 cm. 2.-Fija la muestra lo más rápido posible, después de ser extraída. Si la muestra no se fija en ese momento se desecara y se producirán artefactos. 3.-El liquido de Bouin es un fijador y decalcificador, pero hay que tener cuidado que no este incluido el tejido en esta solución mas de 48 horas, porque endurece el tejido. 4.-Antes de su procesado automático controlar el grado de decalcificación y lavar con alcohol 70%, para eliminar el pigmento amarillento del ácido pícrico. 5.-La correcta confección del bloque, con el eje mayor de la muestra paralela a la superficie de corte y una leve inclinación, permitirá que la cuchilla ejerza menos resistencia y minimice la vibración e inestabilidad. 6.-Evitar un desbastado rápido al realizar el corte. 7.-El secado de las preparaciones es importante para que el material no se desprenda del portaobjetos al realizar las técnicas de coloración. 8.-Un estudio adecuado de la medula ósea, requiere la realización de técnicas histoquímicas y en algunos casos inmunohistoquimicas y ultraestructurales, que en conjunto nos permiten obtener el diagnostico para establecer el tratamiento, el pronostico y control de la enfermedad.
|
|
|
|
1 -Histología funcional texto y altas en color. Segunda edición. P.R. Wheater, H.G. Burkitt. Editorial Jims.
2 -Laboratorio de anatomía patológica. Raimundo García del Moral. Editorial Interamericana McGraw-Hill.
3 -Enfermería profesional, técnicas en enfermería. Dossier-Erb-Blais-Johnson-Tempel. Editorial Interamericana McGraw-Hill. Editorial Interamericana McGraw-Hill.
4 -Dorland diccionario enciclopédico ilustrado de medicina. 20 edicion. Editorial Interamericana McGraw-Hill.
5 -Exámenes de laboratorio, técnicas microscópicas. C. Nezelof, P. Galle, N. Hinglais. Editorial Jims.
6 -Instituto de patología de las fuerzas armadas de los estados unidos de América (AFIP), Métodos Histotecniologicos.
Washington D.C. 1995
|
|
|
|
- MARIA DOLORES BLANCO FLORES (01/05/2007 19:10:52)
- FRANCISCO BORJA GUTIERREZ CORRES (09/05/2007 12:04:08)
- Aleida Herrera Batista (18/05/2007 1:08:28)
- Maria Haydee Aunchayna Mary (27/05/2007 19:04:11)
- maritza gonzalez fernandez (01/06/2007 16:12:51)
- maritza gonzalez fernandez (01/06/2007 16:14:15)
- Mirta Garcia Jardon (02/06/2007 15:00:02)
- FRANCISCO BORJA GUTIERREZ CORRES (04/06/2007 10:39:09)
- Julio Cesar Perez Suarez (03/07/2007 18:13:56)
- Julio Cesar Perez Suarez (03/07/2007 18:17:28)
- FRANCISCO BORJA GUTIERREZ CORRES (04/07/2007 12:09:22)
|
|
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 17:19:20
 fiogf49gjkf0d">
fiogf49gjkf0d">
 fiogf49gjkf0d">
fiogf49gjkf0d">
 fiogf49gjkf0d">
fiogf49gjkf0d">
 fiogf49gjkf0d">
fiogf49gjkf0d">