 Nº 638. Comunicación libre
Nº 638. Comunicación libre
|
Nevus melanocítico fusocelular pigmentado combinado atípico Carmelo Cebrián García[1], Servando E. Marrón Moya[2] |
|
|
9;590;591;592;593;594;595;596;597;598;599;602;603;604;605;606;607;608;609;613;614;615;616;617;618;619;620;622;623;624;625;629;630;631;632;633;634;635;636;637;638;639;640;641;642;643;645;647;648;649;650;652;653;654;655;656;657;658;659;660;661;662;663;664;665;666;667;668;669;670;671;672;673;674;675;676;677;678;679;680;681;682;683;686;687;688;689;690;691;692;693;694;695;696;697;698;699;700;701;702;703;704;706;707;708;709;710;711;712;713;714;715;716;718;719;720;721;722;723;724;725;726;727;728;729;730;731;732;733;734;735;736;737;739;740;741;743;744;745;746;747;748;749;750;751;752;753;754;755;756;757;758;759;760;762;763;764;765;766;767;768;769;770;771;772;773;774;775;776;777;778;779;780;781;782;783;784;785;787;788;789;790;791;792;793;794;795;796;797;798;799;800;801;803;804;805;806;807;811;812;813;814;815;816;817;818;819;820;821;822;823;824;825;826;827;830;831;832;833;834;835;836;837;838;840;841;842;843;844;845;846;847;848;849;850;851;852;853;854;855;856;858;859;860;861;862;863;864;865;866;867;868;869;870;871;872;873;874;875;876;877;878;879;880;881;882;883;884;885;886;888;889;890;891;892;893;894;895;896;897;898;899;900;901;902;903;904;905;906;907;908;909;910;911;913;914;915;916;917;918;919;920;921;922;923;924;925;929;931;934;936;937;939;940;941;942;943;944;945;946;947;948;949;950;951;952;953;954;955;956;957;960;961;962;963;964;965;966;967;968;969;970;971;972;973;974;975;976;977;978;979;980;981;982;983;984;985;986;987;988;989;990;991;992;993;994;995;996;997;998;999;1000;1001;1002;1003;1004;1005;1006;1007;1008;1009;1010;1012;1013;1014;1015;1016;1017;1018;1019;1020;1021;1022;1023;1024;1025;1026;1027;1028;1029;1030;1031;1033;1034;1035;1036;1037;1038;1039;1040;1041;1042;1043;1044;1045;1046;1047;1048;1049;1050;1051;1052;1054;1055;1056;1057;1058;1059;1060;1061;1062;1063;1064;1065;1066;1067;1068;1069;1070;1071;1072;1073;1075;1076;1077;1078;1079;1080;1081;1082;1084;1085;1086;1087;1088;1089;1090;1091;1093;1094;1095;1096;1097;1098;1099;1100;1102;1103;1104;1105;1106;1107;1108;1109;1111;1112;1113;1114;1115;1116;1117;1118;1119;1120;1121;1122;1123;1124;1125;1126;1127;1128;1129;1130;1131;1132;1133;1134;1135;1136;1137;1138;1139;1140;1141;1142;1143;1144;1145;1146;1147;1148;1149;1150;1151;1152;1153;1154;1155;1156;1157;1158;1159;1160;1161;1162;1163;1164;1165;1166;1167;1168;1169;1170;1171;1172;1173;1174;1175;1176;1177;1178;1179;1180;1181;1182;1183;1184;1185;1186;1187;1188;1189;1190;1191;1192;1193;1194;1195;1196;1197;1198;1199;1200;1201;1202;1203;1204;1205;1206;1207;1208;1209;1210;1211;1212;1213;1214;1215;1216;1217;1218;1219;1220;1221;1222;1223;1224;1225;1226;1227;1228;1229;1230;1231;1232;1233;1234;1235;1236;1237;1238;1239;1240;1241;1242;1243;1244;1245;1246;1247;1248;1249;1250;1251;1252;1253;1254;1255;1256;1257;1258;1259;1260;1261;1262;1263;1264;1265;1266;1267;1268;1269;1270;1271;1272;1273;1274;1275;1276;1277;1278;1279;1280;1281;1282;1283;1284;1285;1286;1287;1288;1289;1290;1291;1292;1293;1294;1295;1296;1297;1298;1299;1300;1301;1302;1303;1304;1305;1306;1307;1308;1309;1310;1311;1312;1313;1314;1315;1316;1317;1318;1319;1320;1321;1322;1323;1324;1325;1326;1327;1328;1329;1330;1331;1332;1333;1334;1335;1336;1337;1338;1339;1340;1341;1342;1343;1344;1345;1346;1347;1348;1349;1350;1351;1352;1353;1354;1355;1356;1357;1358;1359;1360;1361;1362;1363;1364;1365;1366;1367;1368;1369;1370;1371;1372;1373;1374;1375;1376;1377;1378;1379;1380;1381;1382;1383;1384;1385;1386;1387;1388;1389;1390;1391;1392;1393;1394;1395;1396;1397;1398;1399;1400;1401;1402;1403;1404;1405;1406;1407;1408;1409;1410;1411;1412;1413;1414;1415;1416;1417;1418;1419;1420;1421;1422;1423;1424;1425;1426;1427;1428;1429;1430;1431;1432;1433;1434;1435;1436;1437;1438;1439;1440;1441;1442;1443;1444;1445;1446;1447;1448;1449;1450;1451;1452;1453;1454;1455;1456;1457;1458;1459;1460;1461;1462;1463;1464;1465;1466;1467;1468;1469;1470;1471;1472;1473;1474;1475;1476;1477;1478;1479;1480;1481;1482;1483;1484;1485;1486;1487;1488;1489;1490;1491;1492;1493;1494;1495;1496;1497;1498;1499;1500;1501;1502;1503;1504;1505;1506;1507;1508;1509;1510;1511;1512;1513;1514;1515;1516;1517;1518;1519;1520;1521;1522;1523;1524;1525;1526;1527;1528;1529;1530;1531;1532;1533;1534;1535;1536;1537;1538;1539;1540;1541;1542;1543;1544;1545;1546;1547;1548;1549;1550;1551;1552;1553;1554;1555;1556;1557;1558;1559;1560;1561;1562;1563;1564;1565;1566;1567;1568;1569;1570;1571;1572;1573;1574;1575;1576;1577;1578;1579;1580;1581;1582;1583;1584;1585;1586;1587;1588;1589;1590;1591;1592;1593;1594;1595;1596;1597;1598;1599;1600;1601;1602;1603;1604;1605;1606;1607;1608;1609;1610;1611;1612;1613;1614;1615;1616;1617;1618;1619;1620;1621;1622;1623;1624;1625;1626;1627;1628;1629;1630;1631;1632;1633;1634;1635;1636;1637;1638;1639;1640;1641;1642;1643;1644;1645;1646;1647;1648;1649;1650;1651;1652;1653;1654;1655;1656;1657;1658;1659;1660;1661;1662;1663;1664;1665;1666;1667;1668;1669;1670;1671;1672;1673;1674;1675;1676;1677;1678;1679;1680;1681;1682;1683;1684;1685;1686;1687;1688;1689;1690;1691;1692;1693;1694;1695;1696;1697;1698;1699;1700;1701;1702;1703;1704;1705;1706;1707;1708;1709;1710;1711;1712;1713;1714;1715;1716;1717;1718;1719;1720;1721;1722;1723;1724;1725;1726;1727;1728;1729;1730;1731;1732;1733;1734;1735;1736;1737;1738;1739;1740;1741;1742;1743;1744;1745;1746;1747;1748;1749;1750;1751;1752;1753;1754;1755;1756;1757;1758;1759;1760;1761;1762;1763;1764;1765;1766;1767;1768;1769;1770;1771;1772;1773;1774;1775;1776;1777;1778;1779;1780;1781;1782;1783;1784;1785;1786;1787;1788;1789;1790;1791;1792;1793;1794;1795;1796;1797;1798;1799;1800;1801;1802;1803;1804;1805;1806;1807;1808;1809;1810;1811;1812;1813;1814;1815;1816;1817;1818;1819;1820;1821;1822;1823;1824;1825;1826;1827;1828;1829;1830;1831;1832;1833;1834;1835;1836;1837;1838;1839;1840;1841;1842;1843;1844;1845;1846;1847;1848;1849;1850;1851;1852;1853;1854;1855;1856;1857;1858;1859;1860;1861;1862;1863;1864;1865;1866;1867;1868;1869;1870;1871;1872;1873;1874;1875;1876;1877;1878;1879;1880;1881;1882;1883;1884;1885;1886;1887;1888;1889;1890;1891;1892;1893;1894;1895;1896;1897;1898;1899;1900;1901;1902;1903;1904;1905;1906;1907;1908;1909;1910;1911;1912;1913;1914;1915;1916;1917;1918;1919;1920;1921;1922;1923;1924;1925;1926;1927;1928;1929;1930;1931;1932;1933;1934;1935;1936;1937;1938;1939;1940;1941;1942;1943;1944;1945;1946;1947;1948;1949;1950;1951;1952;1953;1954;1955;1956;1957;1958;1959;1960;1961;1962;1963;1964;1965;1966;1967;1968;1969;1970;1971;1972;1973;1974;1975;1976;1977;1978;1979;1980;1981;1982;1983;1984;1985;1986;1987;1988;1989;1990;1991;1992;1993;1994;1995;1996;1997;1998;1999;2000;2001;2002;2003;2004;2005;2006;2007;2008;2009;2010;2011;2012;2013;2014;2015;2016;2017;2018;2019;2020;2021;2022;2023;2024;2025;2026;2027;2028;2029;2030;2031;2032;2033;2034;2035;2036;2037;2038;2039;2040;2041;2042;2043;2044;2045;2046;2047;2048;2049;2050;2051;2052;2053;2054;2055;2056;2057;2058;2059;2060;2061;2062;2063;2064;2065;2066;2067;2068;2069;2070;2071;2072;2073;2074;2075;2076;2077;2078;2079;2080;2081;2082;2083;2084;2085;2086;2087;2088;2089;2090;2091;2092;2093;2094;2095;2096;2097;2098;2099;2100;2101;2102;2103;2104;2105;2106;2107;2108;2109;2110;2111;2112;2113;2114;2115;2116;2117;2118;2119;2120;2121;2122;2123;2124;2125;2126;2127;2128;2129;2130;2131;2132;2133;2134;2135;2136;2137;2138;2139;2140;2141;2142;2143;2144;2145;2146;2147;2148;2149;2150;2151;2152;2153;2154;2155;2156;2157;2158;2159;2160;2161;2162;2163;2164;2165;2166;2167;2168;2169;2170;2171;2172;2173;2174;2175;2176;2177;2178;2179;2180;2181;2182;2183;2184;2185;2186;2187;2188;2189;2190;2191;2192;2193;2194;2195;2196;2197;2198;2199;2200;2201;2202;2203;2204;2205;2206;2207;2208;2209;2210;2211;2212;2213;2214;2215;2216;2217;2218;2219;2220;2221;2222;2223;2224;2225;2226;2227;2228;2229;2230;2231;2232;2233;2234;2235;2236;2237;2238;2239;2240;2241;2242;2243;2244;2245;2246;2247;2248;2249;2250;2251;2252;2253;2254;2255;2256;2257;2258;2259;2260;2261;2262;2263;2264;2265;2266;2267;2268;2269;2270;2271;2272;2273;2274;2275;2276;2277;2278;2279;2280;2281;2282;2283;2284;2285;2286;2287;2288;2289;2290;2291;2292;2293;2294;2295;2296;2297;2298;22
INTRODUCCIÓN: Actualmente existe una preocupación creciente sobre el melanoma maligno y las lesiones que pueden precederlo o simularlo. CASO: Presentamos un nevus fusocelular pigmentado (nevus de Reed) en una mujer de 34 años localizado en el antebrazo, originado sobre un léntigo previo, con la impresión clínica de nevus atípico vs. Melanoma. DISCUSIÓN: Esta es una entidad de reciente descripción con un cuadro clínico característico, ya que afecta a pacientes jóvenes, se localiza en extremidades, siendo más frecuente el muslo, y se presenta a modo de pápula muy pigmentada, bien circunscrita, de reciente comienzo. Las características definitorias histológicas comunes, son la presencia de fascículos de células fusiformes pigmentadas, limitadas a la dermis papilar y con marcada uniformidad celular. Morfológicamente, se solapa con otras lesiones como el nevus de Spitz, o nevus displásico, con los cuales puede estar emparentado en cuanto a lesión precursora o premaligna. La principal razón para conocerlo es su distinción del melanoma maligno, y concretamente sus formas atípicas, no reconocidas por todos autores, y caracterizadas por presentar algún rasgo displásico arquitectural, componente epitelioide o atipia citológica. No se han descrito casos de comportamiento maligno, aunque debido a su relativamente reciente descripción todavía no está completamente documentada su evolución. A diferencia del melanoma cutáneo, esta lesión muestra una proliferación simétrica, de crecimiento ordenado, diseminación pagetoide restringida a la epidermis inferior, maduración del componente dérmico, y carencia de marcada atipia citológica. En casos dudosos, para ayudarnos en la distinción del melanoma se han mostrado útiles algunas técnicas como la valoración de la proliferación celular mediante Ki67 y la medición de la capacidad angiogénica mediante el factor de crecimiento endotelial vascular, mientras que otros métodos como la actividad de la telomerasa y bcl-2 no han mostrado utilidad.
|
||
|
|
Presentamos un caso de nevus fusocelular pigmentado (NFP) o nevus de Reed, una lesión de reciente descripción (1), que despierta algunas controversias ya que para algunos autores forma parte del espectro del nevus de Spitz (NS), y que es necesario conocer bien y considerar en el diagnóstico diferencial del melanoma cutáneo, ya que por sus características clínicas e histológicas puede simularlo, sobre todo las variantes atípicas, no mencionadas por todos autores.
|
|
|
|
Mujer de 34 años, gestante, con una lesión definida clínicamente como pigmentada dicromática en el antebrazo izquierdo, con crecimiento y cambios de tamaño recientes, en torno a 2 meses, a modo de pápula negra, sobre léntigo previo. Con la sospecha clínica de nevus melanocítico atípico o melanoma maligno, se extirpa. No hay antecedentes, ni otros datos de interés, ni otras lesiones. Macroscópicamente, se observa una lesión pigmentada, ligeramente sobreelevada, de coloración algo irregular con márgenes imprecisos, y unos diámetros de 0,6 cm. y 0,5 cm. Microscópicamente, la lesión consta de una proliferación fusocelular en la zona de unión dermo-epidérmica con tendencia a formar fascículos mal definidos de orientación vertical (figuras 1, 2, 3, 4 y 5). La epidermis está ligeramente engrosada y con ligera papilomatosis (figura 1). No hay proliferación lentiginosa en la unión dermo-epidérmica. Los melanocitos tienen extensa morfología fusiforme, muchos de ellos muestran abundante pigmento melánico intracitoplasmático (figuras 6, 7 y 8). Los núcleos son bastante isomorfos, con cromatina clara y nucleolo eosinofílico. Aunque predomina el componente de unión, se observa cierta difusión de los melanocitos entre los haces colágenos, con sensación de maduración en profundidad (figura 9). No aparecen diseminación pagetoide, ni figuras de mitosis. Adyacentemente, hay una proliferación de células típicas de un nevus melanocítico intradérmico, con tendencia a situarse por debajo de la proliferación fusocelular (figuras 3 y 6). No se observa reacción del huésped, ni fibroplasia ni inflamación asociada a la proliferación fusocelular. Las células muestran positividad inmunohistoquímica para S-100 (figura 10) y HMB 45 (figura 11), de distribución uniforme, que no tiñe las células de nevus intradérmico en el caso del HMB45. El Ki67 muestra un bajo índice de proliferación celular, comparable a los melanocitos del nevus intradérmico (figura 12). Con el cuadro descrito se diagnosticó un nevus fusocelular pigmentado (de Reed) compuesto atípico. Después de 9 meses de evolución no se ha comunicado recidiva local ni a distancia.
|
|
|
|
Desde la reciente descripción inicial de Reed que le da el nombre a esta lesión (1), varias series de casos de NFP se han publicado (2, 3, 4, 5, 6). El cuadro clínico es característico, ya que afecta a pacientes jóvenes, se localiza en extremidades, siendo lo más frecuente el muslo, y se presenta a modo de pápula muy pigmentada, bien circunscrita, de reciente comienzo. Puede localizarse en tronco y son muy raros en cabeza y cuello. La edad media de debut está entre los 17 y los 25 años, con una evolución general entre 2 y 6 meses. No se presenta al nacimiento. Es bastante típico que se constaten cambios recientes con aumento de tamaño o pigmentación. Es una lesión pequeña, mide de 1 a 10 mm. con un diámetro medio de 4 mm. La relación mujer / hombre es de 1,4/1, aunque puede variar según las formas clínico-patológicas. Afecta fundamentalmente a individuos de raza blanca. La forma típica está constituida por grandes nidos confluentes de células fusiformes a modo de fascículos orientados preferentemente de manera vertical, situados regularmente, de tamaño similar y en localización superficial, ya que están limitados a la epidermis y dermis papilar, sin afectación de la dermis reticular. La arquitectura de conjunto es simétrica. Se puede formar un espacio de separación artificioso entre la epidermis y nidos de melanocitos. Los fascículos comprimen el colágeno adyacente, son nidos compactos y raramente las células se extienden a corta distancia desde el foco principal. En pocos casos la proliferación fusocelular se presenta de manera difusa, sin formar fascículos, o muy rara disposición en células aisladas o pequeños grupos entre el colágeno. El espesor en conjunto, no suele ser superior a 2 mm. Las células tienen bordes mal definidos, núcleo alargado, dispersión de la cromatina con pequeño nucleolo central. Una minoría de células contiene abundante melanina. Es típica la uniformidad celular, con maduración de las células en profundidad si tiene componente dérmico, con núcleos celulares y masas fusocelulares más pequeñas. Puede perder el patrón en fascículos en los niveles más profundos, donde las células, con núcleo pequeño, redondo u oval, con escaso citoplasma, semejan las células del nevus convencional y se sitúan como células aisladas, aunque siempre mantiene un fenotipo fusocelular. Puede haber glóbulos eosinofílicos extracelulares (Kamino) en epidermis inferior o nidos de unión, y ocasionales células grandes con núcleo oval o irregular, cromatina grumosa y nucleolo grande. No hay acuerdo sobre el número de mitosis, ya que para algunos autores son de 0 a 11 mitosis en 10 campos de gran aumento (2, 5), y para otros no se observan mitosis (6), en cualquier caso nunca son atípicas. La lesión se caracteriza también por tener una buena demarcación lateral e hiperplasia melanocitaria lentiginosa mínima o ausente. Muestra hiperplasia escamosa uniforme de tipo lámina ligera a moderada, sin crestas interpapilares alargadas como en nevus lentiginoso y displásico, así como, hiperqueratosis y melanina en la capa córnea. Las células pueden extenderse por la vaina de estructuras anexiales, como los conductos de las glándulas salivares ecrinas o folículos pilosos, pero no por nervios o vasos. No se presentan células epitelioides, atipia celular, así como ausencia o poca inflamación asociada o fibroplasia y telangiectasias raras. Sin embargo, el NFP típico es una lesión rara, mientras que las variantes son más frecuentes. Existen formas de NFP que se separan por determinadas características de la forma típica y que pueden presentar aun mayores problemas para diferenciar del melanoma maligno cutáneo. A estas variantes se conoce como NFP atípico y no son reconocidas por todos los autores ya que no las mencionan en sus series o no las reconocen como variantes, incluyéndolas en el propio espectro de la lesión y sin diferenciarlas (4, 5). Las variantes atípicas muestran como características generales anomalías arquitecturales, atipia citológica o prominente componente de células epitelioides (la última característica lo asemeja al NS). Las alteraciones arquitecturales consisten en márgenes laterales poco circunscritos con extensión lateral del componente intraepidérmico o componente de unión, a base de células aisladas (hiperplasia lentiginosa de melanocitos), crestas interpapilares alargadas, y migración hacia arriba en la epidermis de los melanocitos (pagetoide). También se observa respuesta del huésped en forma de infiltrado inflamatorio linfoide perivascular, melanófagos perivasculares y también de manera difusa en la dermis papilar, y estroma reactivo con fibroplasia en láminas concéntricas de la dermis. La atipia citológica consta de aumento nuclear, polimorfismo, hipercromasia, prominente nucleolo, y tendencia de las células a adoptar un hábito epitelioide. Todas estas características, excepto la diseminación pagetoide son características propias del nevus displásico. Estas formas atípicas tienen preponderancia en mujeres y a edades más tempranas. Otra variante del NFP es el conocido como nevus fusocelular pigmentado plexiforme, que en la literatura ha sido descrito bajo otros nombres (nevus penetrante profundo, nevus combinado, nevus azul, NS). Se caracteriza por afectación más profunda que el típico, hasta la dermis reticular, en forma de cuña con base en la epidermis, fascículos discretos en íntima asociación con nervios, vasos y anejos. Suelen acompañar a los fascículos melanófagos. Muestran mayor atipia nuclear que las formas típicas y raras mitosis. Su localización característica, a diferencia de las formas típicas, es cabeza, cuello y parte superior de extremidades. Por último, las formas combinadas de NFP, en las que se asocian células típicas de nevus, como en nuestro caso. Esto plantea la posibilidad de que la lesión pueda originarse en relación con un nevus melanocítico convencional, y por otro lado, la existencia de células de menor tamaño del nevus puede sugerir erróneamente maduración (figura 6). En cualquier caso, existen unas características definitorias del NFP, comunes a todas las formas, como son: la presencia de fascículos de células fusiformes pigmentadas, y la uniformidad entre las células. La proliferación limitada al dermis papilar sin afectación del reticular se da en todas, excepto en la variante plexiforme. Para unos autores el NFP forma parte del espectro del NS (6, 7, 8), sin embargo, para la mayoría es una entidad distintiva (2, 3, 4, 5). La presencia de células epitelioides en el NFP puede establecer una relación con el NS. El NFP puede considerarse una entidad clínico-patológica, ya que es una lesión plana o ligeramente elevada, muy pigmentada, que clínicamente se confunde con nevus atípico, displásico o melanoma. El NS, por otro lado, es una lesión cupuliforme o polipoide sonrosada, que sugiere clínicamente hemangioma, verruga, tumor anexial o nevus. A diferencia del NS, el NFP tiene una típica predilección por las piernas de las mujeres, muestra prominentes nidos compactos de unión, con expansión de la dermis papilar, frente a la infiltración de la dermis reticular por células sueltas o pequeños grupos de células con un patrón en cuña. En NFS la hiperplasia escamosa es de tipo placa, mientras en NS hay mayor hiperplasia y más irregular. En NS hay mayor edema estromal y telangiectasias, así como escaso o ausente pigmento melánico. El NS se caracteriza por una población de células epitelioides o células fusiformes gruesas, mientras que en el NFP las células epitelioides suelen estar ausentes, aunque puede haberlas creando cuadros intermedios. Para diferenciar el NFP del nevus displásico, se debe tener en cuenta que éste último se presenta como una mácula o pápula de bordes mal definidos, con coloración variable y localizado, sobre todo, en el tronco. Características del nevus displásico que no son propias del NFP son la formación de puentes entre los nidos de melanocitos y los nidos de la unión irregulares. Por otro lado, otras características del nevus displásico que puede ayudar a diferenciarlo pueden darse también en las formas atípicas de NFP, como son: extensión lateral o márgenes laterales mal definidos, hiperplasia melanocítica lentiginosa, atipia nuclear o citológica, fibroplasia en láminas concéntricas. De hecho, hay un cierto solapamiento de características histológicas dentro de la categoría general de lesiones de displasia melanocitaria premaligna (proliferación melanocitaria atípica intermedia entre melanocitos normales basales o nevus y melanoma), a la que pertenecen: nevus displásico adquirido, nevus congénito atípico (displásico), lentigo maligno, proliferaciones melanocitarias lentiginosas acral atípica (displásica) o mucosa, nevus de Spitz atípico y nevus fusocelular pigmentado atípico (2). Para distinguir el NFP son útiles las características definitorias ya mencionadas. Las características del melanoma cutáneo que ayudan a diferenciarlo del NFP son la asimetría o mayor alteración arquitectural, desarrollada diseminación pagetoide (no limitado sólo a la mitad inferior de la epidermis), melanocitos atípicos solitarios o en nidos extendiéndose lateralmente en la epidermis más allá del componente principal, atipia nuclear más marcada, continua o completamente evolucionada, y carencia de maduración en profundidad del componente dérmico. El melanoma muestra mayor polimorfismo, mayor actividad proliferativa, y un infiltrado linfoide a modo de banda, frente al infiltrado linfoide perivascular del NFP. En todo caso, se recomienda para evitar errores diagnósticos un mayor énfasis en las anomalías citológicas del melanoma (3). En las forma plexiforme de NFP las características que pueden ayudar a diferenciarlo del melanoma son la localización en cabeza, cuello y parte proximal de extremidades, simetría, componente de unión inconspicuo, pocas mitosis, cromatina anodina, y ausencia de reacción estromal o inflamación. Para ayudar al patólogo en casos limítrofes, con características no definitivas a favor de melanoma o no, se han investigado diversos métodos. Ha resultado útil para esta distinción la determinación de la capacidad proliferativa con Ki67, y concretamente la determinación del porcentaje de mitosis en la lesión en su conjunto (sin dividir por tercios de profundidad), y según el porcentaje en los campos más activos (9). La determinación del factor de crecimiento endotelial vascular (VEGF) también ayuda, ya que los tumores malignos muestran fuerte expresión de VEGF, mientras que las lesiones benignas no son reactivas (10). Otros métodos investigados que no han resultado útiles para la diferenciación de procesos melanocíticos malignos y benignos, son la determinación de telomerasa medida por técnicas de hibridación in situ (11), el bcl-2, ya que es ampliamente expresado en lesiones melánicas independientemente de su comportamiento biológico (12), y las seudoinclusiones nucleares (13). El tratamiento recomendado es la escisión local completa. No hay evidencia de recurrencia, y no se ha comunicado evolución maligna hasta la fecha. No se ha documentado asociación con melanoma cutáneo o la presencia concomitante de nevus displásico o lesión semejante en otro sitio, pero no se puede descartar. Como siempre, se cree que el mayor riesgo de progresión a malignidad se relaciona con mayor atipia en células individuales. En conclusión, el NFP representa una entidad clínico-patológica bien diferenciada, que clínicamente puede sugerir melanoma y microscópicamente puede presentar problemas para diferenciarlo, fundamentalmente las formas atípicas, aunque nunca alcanza el grado de alteración arquitectural y atipia citológica propias del melanoma.
|
|
|
|
1. Reed RJ, Ichinose H, Clark WH Jr, Mihm MC Jr. Common and uncommon melanocytic nevi and borderline melanomas. Semin Oncol 1975; 2:119-47. 2. Barnhill RL, Barnhill MA, Berwick M, Mihm MC Jr. The histologic spectrum of pigmented spindle cell nevus: a review of 120 cases with emphasis on atypical variants. Hum Pathol 1991; 22:52-8. 3. Barnhill RL, Mihm MC Jr. Pigmented spindle cell naevus and its variants: distinction from melanoma. Br J Dermatol 1989; 121:717-725. 4. Requena L, Sanchez Yus E. Pigmentes spindle cell naevus. Br J Dermatol 1990; 123:757-63. 5. Sau P, Graham JH, Helwig EB. Pigmented spindle cell nevus: a clinicopathologic analysis of ninety-five cases. J Am Acad Dermatol 1993; 28:565-71. 6. Sagebiel RW, Chinn EK, Egbert BM. Pigmented spindle cell nevus: clinic and histological review of 90 cases. Am J Surg Pathol 1984; 8:645-53. 7. Echevarria R, Ackerman LV. Spindle and epithelioid cell nevi in the adult: clinicopathological report of 26 cases. Cancer 1967; 20:175-89. 8. Paniago-Pereira C, Maite JC, Ackerman AB. Nevus of large spindle and/or epithelioid cells (Spitz´s nevus). Arch Dematol 1987; 114:1811-1823. 9. Li LX, Crotty KA, McCarthy SW, Palmer AA, Dril JJ. A zonal comparison of MIB1-Ki67 immunoreactivity in benign and malignant melanocytic lesions. Am J Dermatopathol 2000; 22:489-95. 10. Simonetti O, Lucari G, Brancorsini D, Nita P, Bernardini ML, Biagini G, Offidani A. Immunohistochemical expression of vascular endotelial growth factor, matriz metalloproteinase 2, and matriz metalloproteinase 9 in cutaneous melanocytic lesions. Cancer 2002; 95:1963-70. 11. Guttman-Yassky E, Bergman R, Manov L, Sprecher E, Shaefer Y, Kerner H. Human telomerase RNA componet expression in Spitz nevi, common melanocytic nevi, and malignant melanomas. J Cutan Pathol 2002; 29:341-6. 12. Cerroni L, Soyer HP, Kerl H. bcl-2 protein expression in cutaneous malignant melanoma and benign melanocytic nevi. Am J Dermapathol 1995; 17:7-11. 13. Rose DS. Nuclear pseudoinclusions in melanocytic naevi and melanomas. J Clin Pathol 1995; 48:676-7.
|
|
|
|
- Dania Ledesma (28/05/2007 4:39:39)
|
|
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 17:19:20
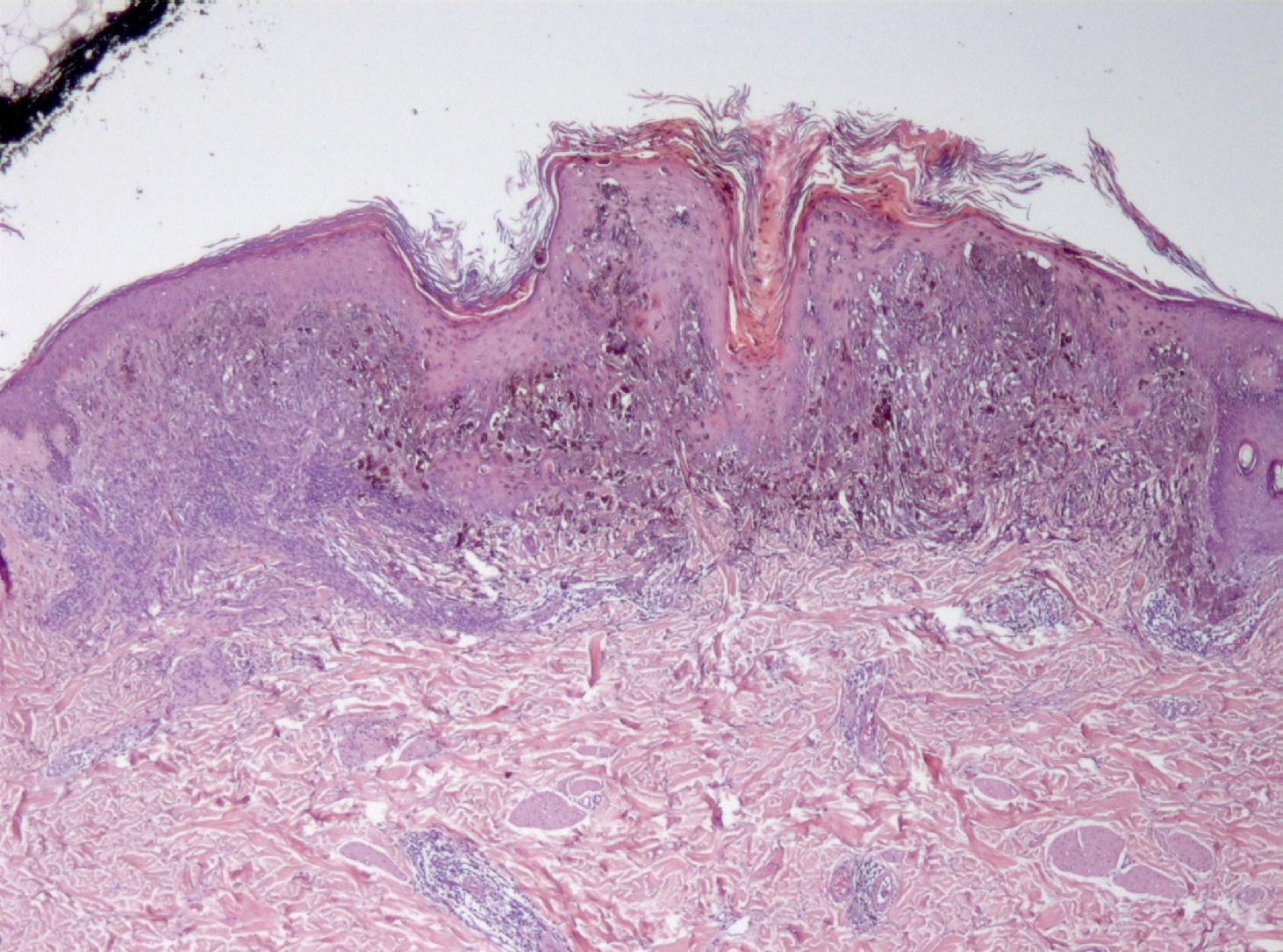
 fiogf49gjkf0dProliferación fusocelular de la unión dermo-epidérmica, con nidos celulares confluentes, de células cargadas de melanina (HE, 100x).">
fiogf49gjkf0dProliferación fusocelular de la unión dermo-epidérmica, con nidos celulares confluentes, de células cargadas de melanina (HE, 100x).">
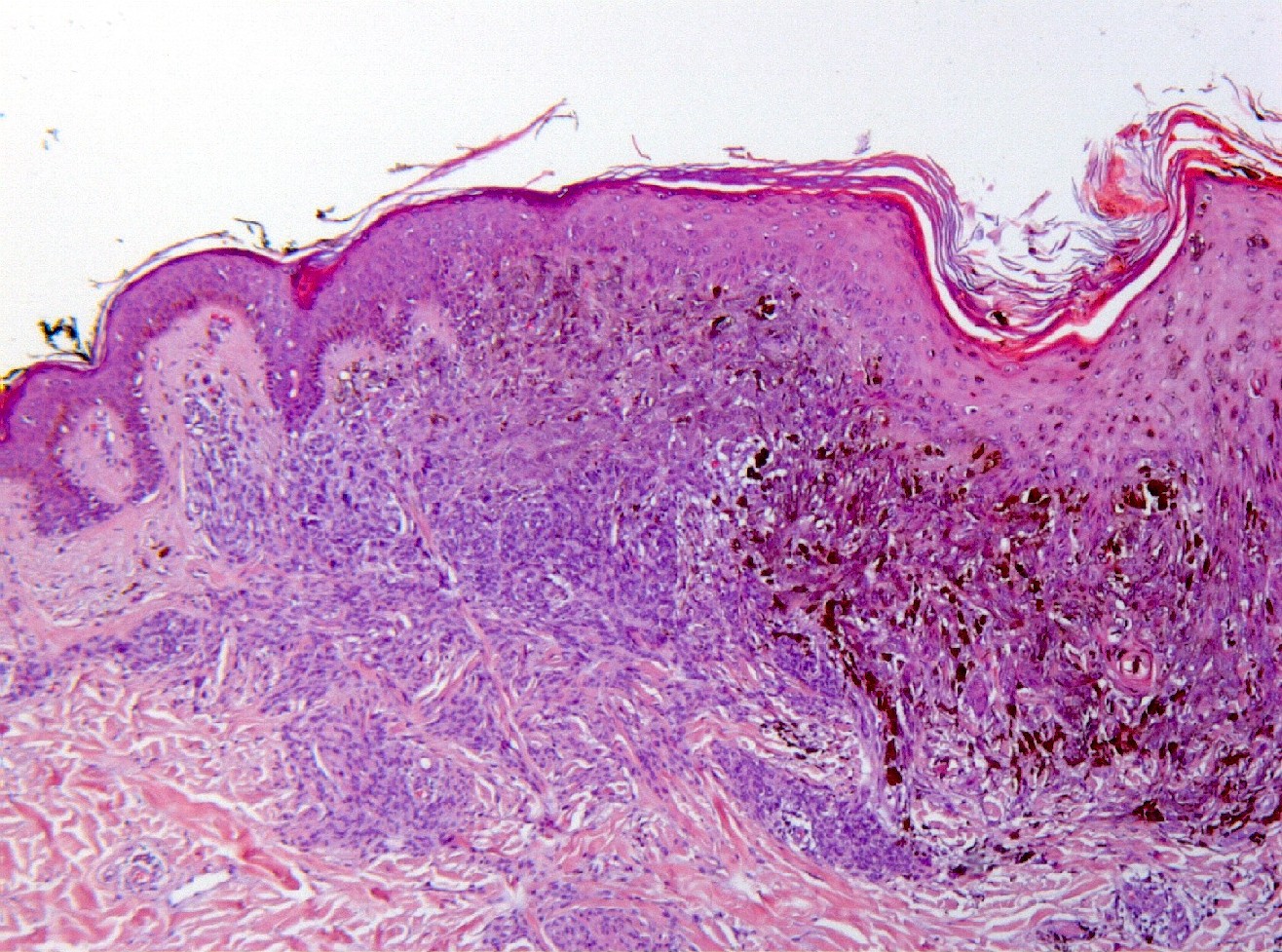
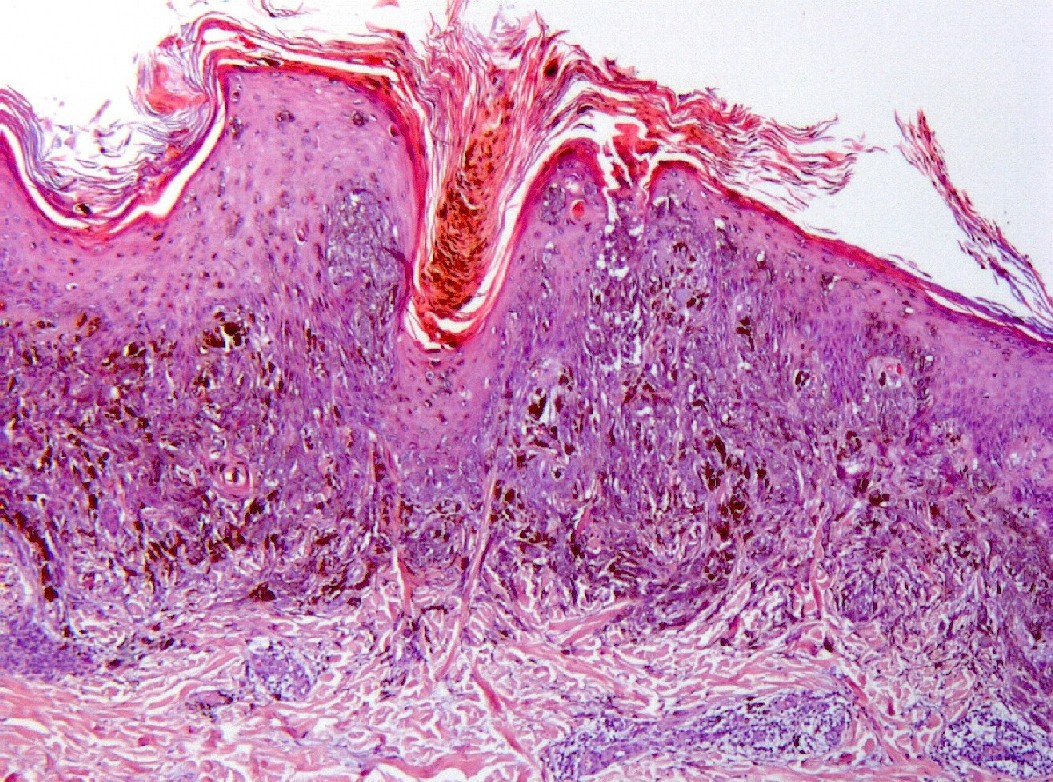
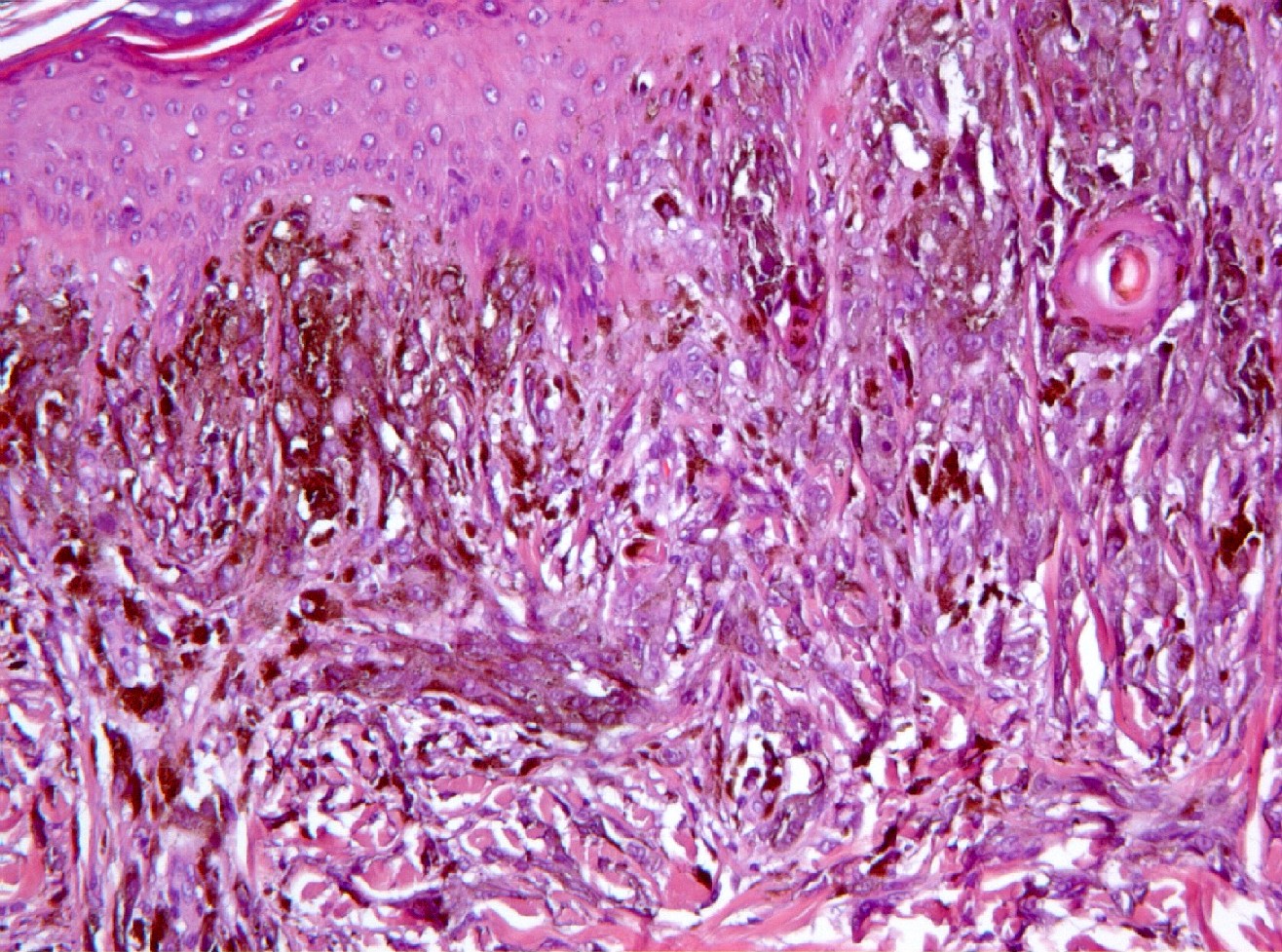 fiogf49gjkf0dLa proliferación fusocelular tiende a disponerse verticalmente, formando haces mal definidos (HE, 200x).">
fiogf49gjkf0dLa proliferación fusocelular tiende a disponerse verticalmente, formando haces mal definidos (HE, 200x).">
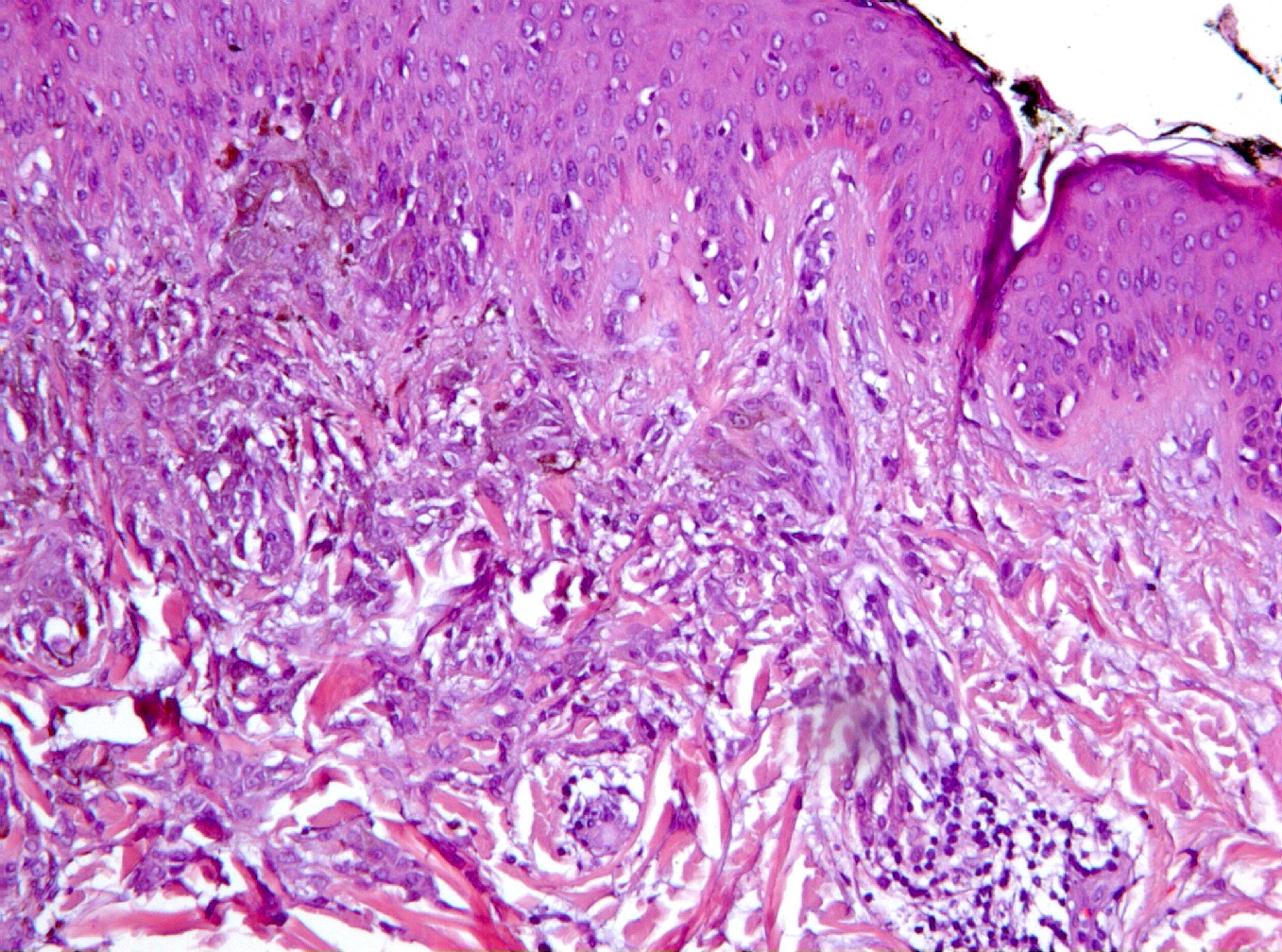
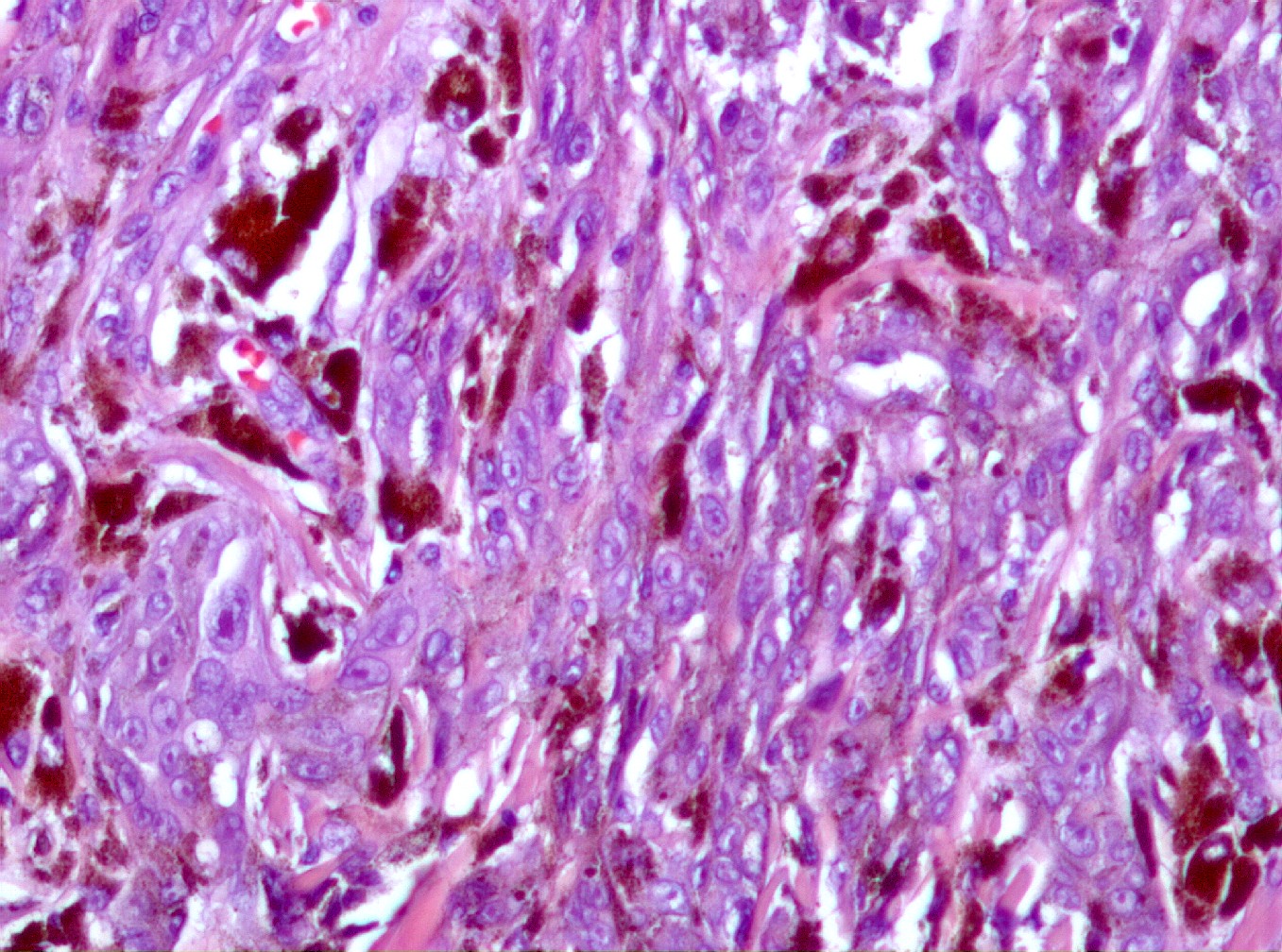
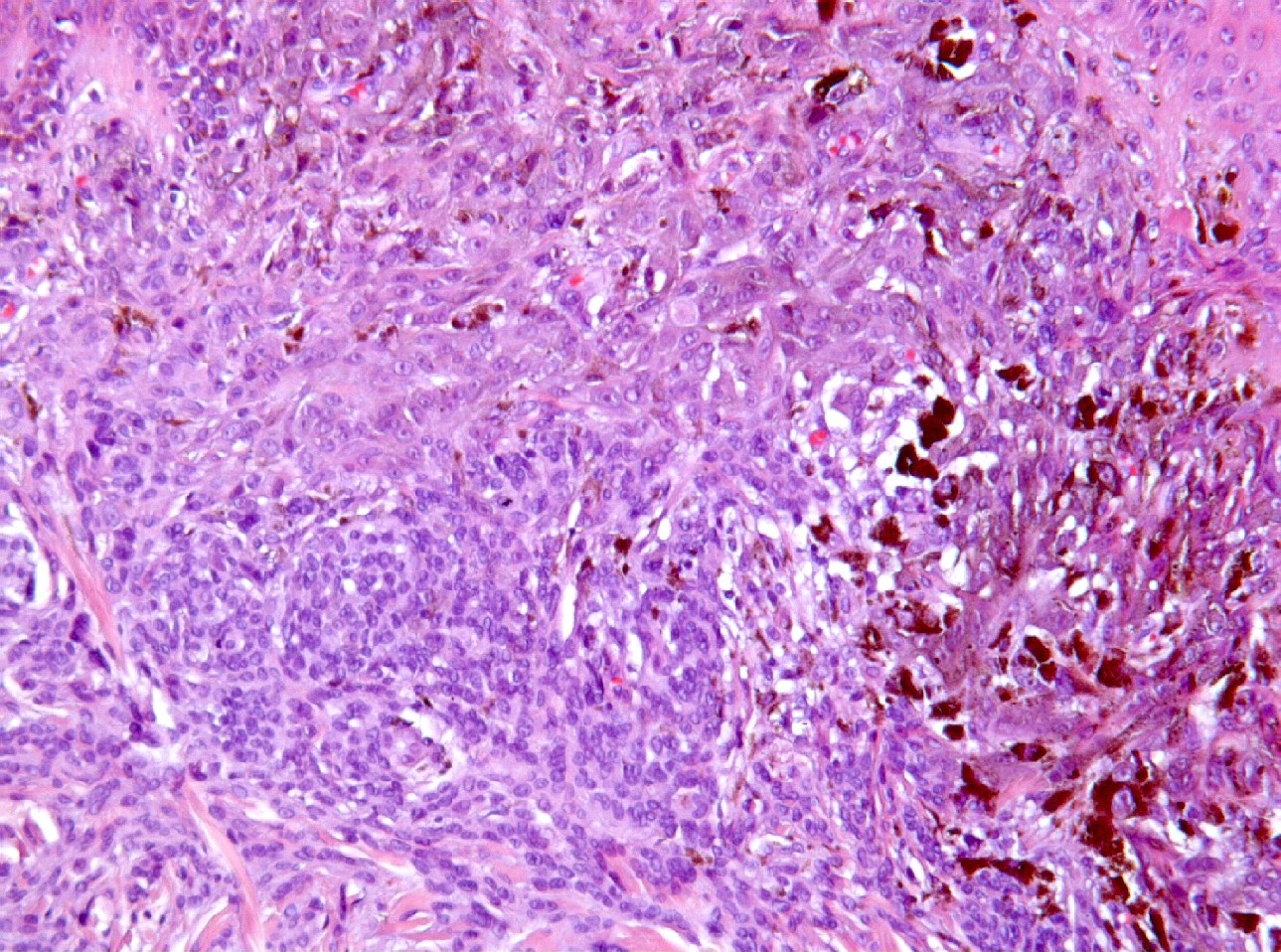 fiogf49gjkf0dSe constata la población celular del nevus fusocelular, con células de mayor tamaño, núcleos más grandes, con evidente nucleolo (mitad superior de la imagen), frente a las células de un nevus convencional de menor tamaño y núcleo sin nucleolo, en la mitad inferior de la imagen (HE, 200x).">
fiogf49gjkf0dSe constata la población celular del nevus fusocelular, con células de mayor tamaño, núcleos más grandes, con evidente nucleolo (mitad superior de la imagen), frente a las células de un nevus convencional de menor tamaño y núcleo sin nucleolo, en la mitad inferior de la imagen (HE, 200x).">
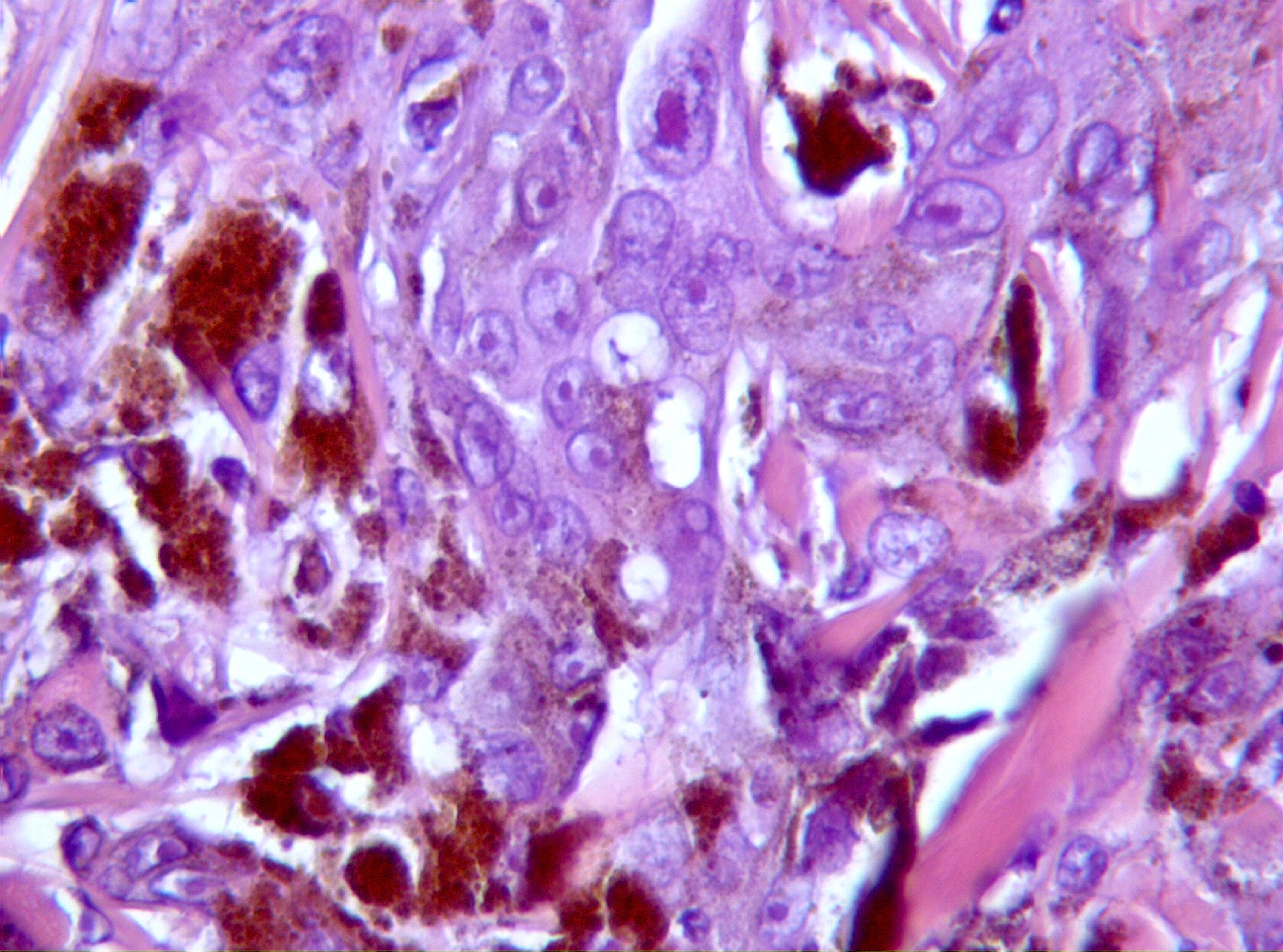
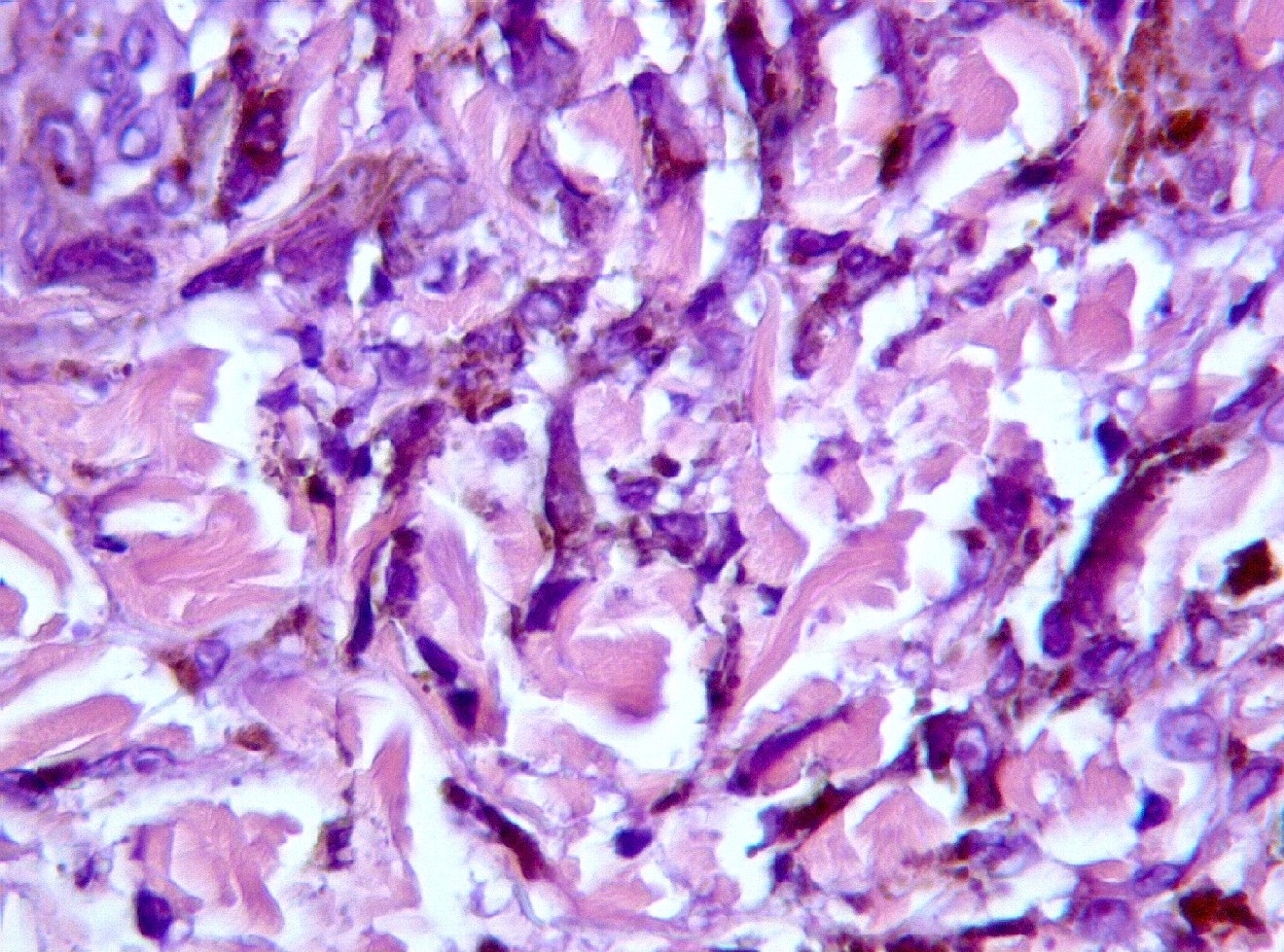 fiogf49gjkf0dProliferación celular situándose entre las fibras de colágeno (HE, 400x).">
fiogf49gjkf0dProliferación celular situándose entre las fibras de colágeno (HE, 400x).">
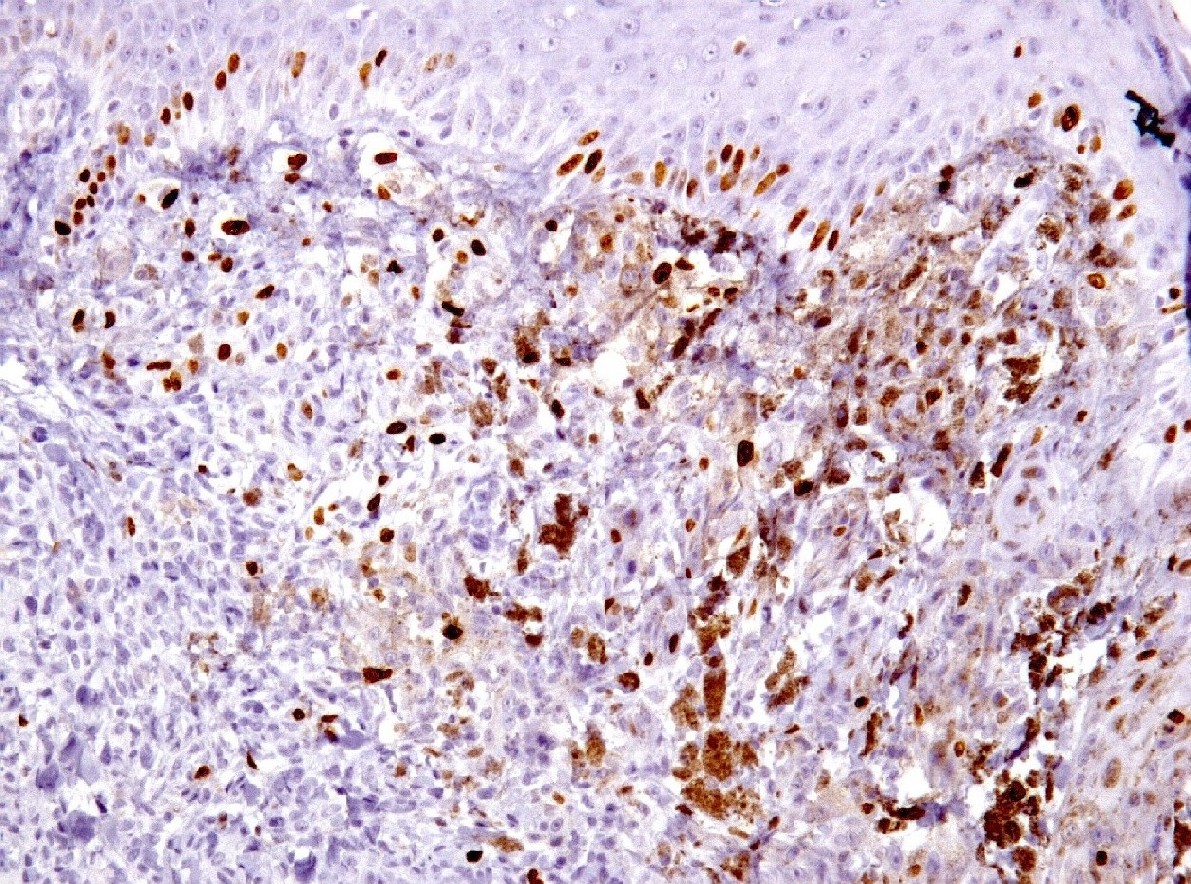
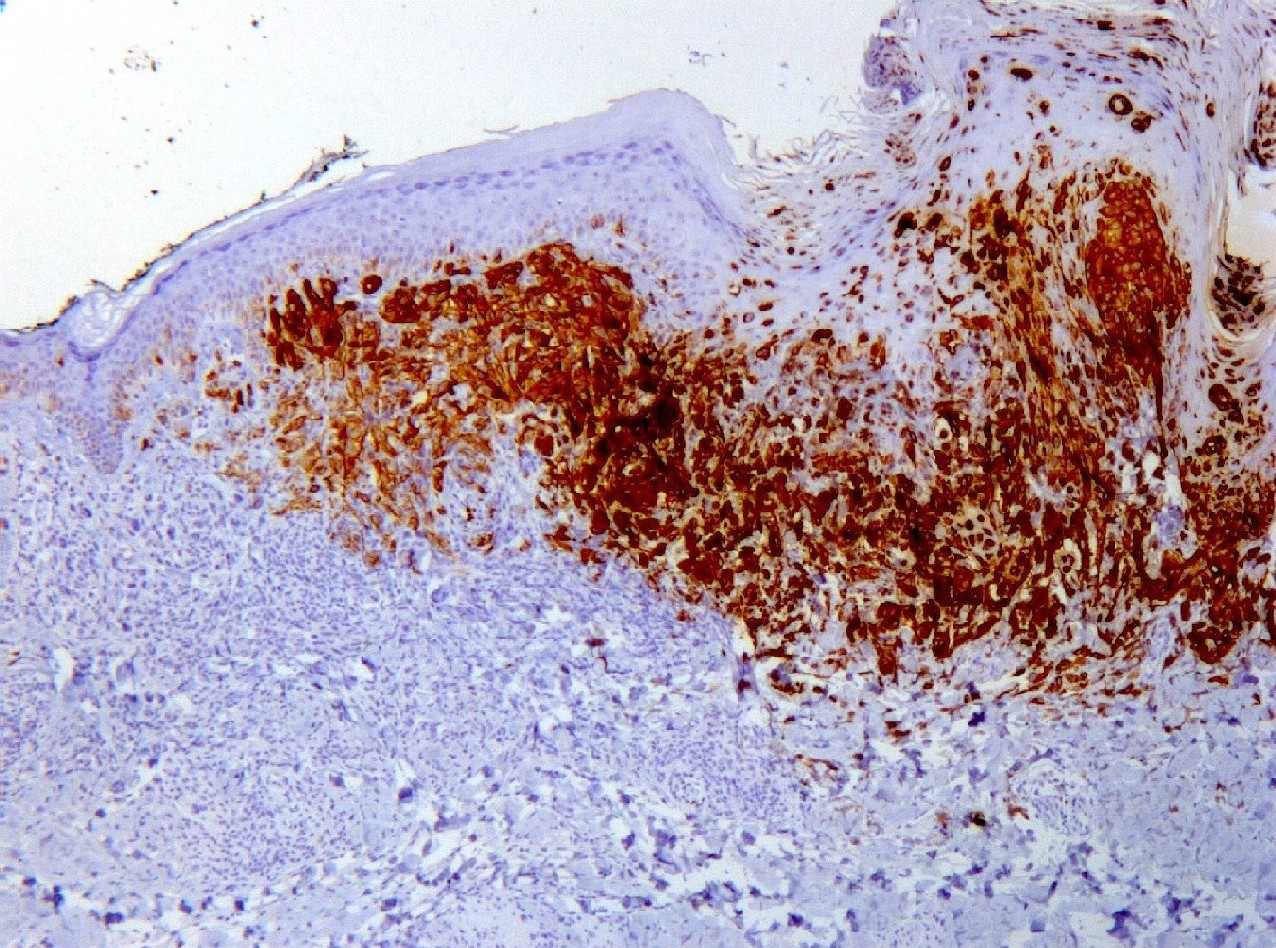 fiogf49gjkf0dEl HMB 45 se expresa de manera uniforme en toda la lesión pero es negativo en las células del nevus vecino, hacia la parte inferior derecha de la imagen (HMB 45, 100x).">
fiogf49gjkf0dEl HMB 45 se expresa de manera uniforme en toda la lesión pero es negativo en las células del nevus vecino, hacia la parte inferior derecha de la imagen (HMB 45, 100x).">