|
Asociaciones entre características patológicas y marcadores inmunohistoquímicos en subtipos de cáncer de mama ductal infiltrante
Cristina Bértolo Martín de Rosales[1], David Guerrero Setas[1], Alicia Córdoba Iturriagagoitia[2], Francisco Vicente García[3], Mercedes Murillo Lalana[1], María Cristina Caballero Martínez[1], José María Martínez-Peñuela Virseda[2], José Miguel Lera Tricas[3]
(1) Centro de Investigación Biomédica, Servicio Navarro de Salud, Pamplona, Navarra. ESPAÑA
(2) Servicio de Anatomía Patológica, Hospital de Navarra, Servicio Navarro de Salud, Pamplona, Navarra. ESPAÑA
(3) Servicio de Cirugía General y Digestiva, Hospital de Navarra, Servicio Navarro de Salud, Pamplona, Navarra. ESPAÑA
|
|
Introduccion
El cáncer de mama constituye el tipo de cáncer más frecuente en mujeres y su alta mortalidad asociada hace necesario el estudio de marcadores que permitan caracterizar en mayor medida dichos tumores (Botha JL, 2003).
La proteína p53, también denominada guardián del genoma, es una proteína alterada en múltiples tipos de tumores con su consiguiente efecto en el control del ciclo celular y apoptosis (Lacroix M, 2006). Es ampliamente aceptado que la proteína bcl-2 tiene un papel antiapoptótico, aunque curiosamente la ausencia de expresión de esta proteína parece estar asociada con un pronóstico más favorable (Thomadaki H, 2007).
La heterogeneidad presente en los distintos subtipos se refleja asimismo en la expresión diferencial de los receptores de estrógeno (ER), c-erbB2 (HER2/neu), citokeratina 5/6 (CK 5/6) y el receptor del factor del crecimiento epidérmico (EGFR1/ HER1) (Nielsen TO, 2004). De esta forma, cuatro subtipos tumorales han sido descritos: Luminal, HER2, basal y normal.
En este estudio analizamos las asociaciones entre las características patológicas y los marcadores inmunohistoquímicos de mujeres con cáncer de mama de los distintos subtipos.
|
|
Material y Métodos
1. Población de estudio: El grupo incluye 60 mujeres diagnosticadas de cáncer de mama ductal infiltrante, de edades comprendidas entre 46 y 94 años (media de edad: 64.5± 15.9). El Comité Ético del Hospital aprobó este estudio, y todas las pacientes fueron informadas y dieron su consentimiento para participar en el estudio. Los tumores se confirmaron histopatológicamente y se clasificaron según el sistema TNM (Greene FL, 2003). El diámetro del tumor está comprendido entre 0.7 y 5 cm. (mean 2.58± 0.13). Los datos patológicos se reflejan en la tabla 1.
2. Immunohistoquímica (IHQ). Los tests se aplican en secciones de 4 μm de grosor una vez desparafinados e hidratados. La recuperación del antígeno se realizó mediante incubación en buffer citrato pH 6.0, a 95ºC para 30 minutos. Después del bloqueo de peroxidasa endógena con 3%, los portas se incuban con los anticuerpo primario contra c-erbB-2, EGFR, cytokeratin 5/6 and p63 para la clasificación de los casos según se describió anteriormente (Nielsen TO, 2004). Los anticuerpos primarios considerados Los anticuerpos y sus diluciones están reflejados en la tabla 1. La visualización se realiza mediante 3,3-diaminobencidina en peróxido de hidrógeno al 3%, y contratinción con H&E. La incubación en PBS en vez de anticuerpo primario constituye el control negativo.
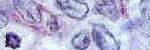
Los resultados de la inmunohistoquímica se valoran independientemente por dos patólogos que evalúan el marcaje de membrana (ER, c-erbB2), citoplasmático (bcl-2) (Figura 1) y el marcaje nuclear (ki-67, p53) (Figura 2). Los resultados de c-erbB2 se cuantificaron: 0= no hay expresión, 1= leve, 2= uniforme, 3= expresión intensa. Los valores considerados para p53, bcl-2 y ER fueron: 0: si no hay marcaje o marcaje menor del 10% de las células, débilmente positivo (1+) si el marcaje está presente en el 10-25% de las células, intermedio (2+) si el marcaje está presente en el 25-75% de las células y fuertemente positivo (3+), si más del 75% de las células están marcadas.
|
Proteína |
Clon |
Dilución |
Tª de incubación |
|
c-erbB-2 |
Clon NCL-CB11 |
1:40 |
37ºC |
|
EGFR |
Clon 2-18C9 |
prediluido |
Tª ambiente |
|
Cytokeratin 5/6 |
Clon D5/16B4 |
prediluido |
Tª ambiente |
|
ER |
Clon PGP-1A6 |
prediluido |
42ºC |
|
ki-67 |
Clon ki-67 |
1:50 |
42ºC |
|
bcl-2 |
Clon 100 |
1:300 |
Tª ambiente |
|
p53 |
Clon BP53-11 |
1:100 |
37ºC |
Tabla 1. Anticuerpos empleados en el estudio inmunohistoquímico.
3. Análisis estadístico: Las comparaciones en la distribución de las variables patológicas se realizaron mediante el test de χ2 o test exacto de Fisher. Se emplea el programa informático SPSS (versión 14.0, Inc., Chicago, USA). El valor de probabilidad estadística significativo fue considerado para valores de P <0.05.
|
|
Resultados
1. Asociaciones entre las variables patológicas y la expresión de proteínas detectada por inmunohistoquímica: En nuestro grupo de estudio, el grado histológico desfavorable (G3) se asocia con la ausencia de expresión de ER (p=0.001), la acumulación de la proteína alterada p53 (p=0.042), la ausencia de expresión de bcl-2 (p=0.047), la expresión elevada del marcador de proliferación ki-67 (p=0.000) y el desarrollo de metástasis durante el periodo de seguimiento (p=0.004).
La acumulación de la proteína p53 se asocia no sólo con grados histológicos desfavorables y a la ausencia de expresión de bcl-2, según se ha mencionado, sino también con niveles altos de ki-67 (p=0.01). La expresión de bcl-2 está asociada claramente con la expresión de ER (p=0.001), con una menor proliferación (p=0.050) y con la ausencia de recidiva, siendo el 90% de las pacientes que no han desarrollado metástasis positivas para esta proteína (p=0.034). Esta expresión también se asocia de manera inversa con la expresión de p53 (p=0.003).
2. Características de los subtipos del cáncer de mama: En nuestro grupo de estudio los cuatro subtipos tumorales se han distribuido de la siguiente manera: 22 casos (36.6%) son luminales, 27 casos (el 45%) son Her2 positivos, 10 casos (el 16%) son basales, y 1 caso (1.6%) es del subtipo normal. Las correlaciones existentes entre el subtipo tumoral y las variables inmunohistoquímicas se muestran en la tabla 2.
El subtipo luminal tiende a ser negativo para p53 (p=0.079). Además existe una clara asociación entre este subtipo tumoral y la expresión de bcl-2, siendo todo los casos luminales positivos para bcl-2 (p=0.003). Un porcentaje del 77% de los pacientes del subtipo luminal es del tipo A (21 pacientes) mientras que el 22% (6 pacientes) corresponden al tipo B.
Los tumores basales presentan un grado histológico alto (p=0.003) y un estado de proliferación intermedio o alto (p=0.049). No existen diferencias en la distribución del resto de variables patológicas o moleculares analizadas.
El grado histológico se distribuye igualmente en el subtipo HER2 y en los casos normales (p= 0.99; p=0.46; respectivamente).
|
|
SUBTIPO TUMORAL DE CÁNCER DE MAMA
|
|
VARIABLE |
Nº pacientes |
Luminal |
HER2 |
Basal |
|
Si
n=27 |
Otros
n=33 |
P* |
Si
n=22 |
Otros
n=38 |
P* |
Si
n=10 |
Otros
n=50
|
P* |
|
Grado de proliferación
Bajo
Intermedio/ Alto |
17
43 |
12 (44.4%)
15 (55.6) |
5 (15.2%)
28 (84.8%) |
0.012 |
5 (22.7%)
17 (77.3%) |
12 (31.6%)
26 (68.4%) |
0.46 |
0 (0%)
10 (100%) |
17 (34%)
33 (66%) |
0.049* |
|
Expresión Bcl-2
Negativo
Positivo |
9
51 |
0 (0%)
27 (100%) |
9 (27.3%)
24 (72.7%) |
0.003* |
5 (22.7%)
17 (77.3%) |
4 (10.5%)
34 (89.5%) |
0.26* |
4 (40%)
6 (60%) |
5 (10%)
45 (909%) |
0.034* |
|
Expresión P53
Negativo
Positivo |
42
18 |
22 (81.5%)
5 (18.5%) |
20 (60.6%)
13 (39.4%) |
0.079 |
13 (59.1%)
9 (40.9%) |
29 (76.3%)
9 (23.7%) |
0.16 |
6 (60%)
4 (40%) |
36 (72%)
14 (28%) |
0.46* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tabla 2: Variables patológicas e inmunohistoquímicas según los diferentes subtipos tumorales. *Test exacto de Fisher
.jpg) fiogf49gjkf0dFigura 1A. Detección inmunohistoquímica de proteína bcl-2. A: categoría 1+ (20x)."> fiogf49gjkf0dFigura 1A. Detección inmunohistoquímica de proteína bcl-2. A: categoría 1+ (20x).">
Figure 1A - fiogf49gjkf0d Figura 1A. Detección inmunohistoquímica de proteína bcl-2. A: categoría 1+ (20x).
.jpg) fiogf49gjkf0dFigura 1B. Detección inmunohistoquímica de proteína bcl-2. B: categoría 3+ (20 x )."> fiogf49gjkf0dFigura 1B. Detección inmunohistoquímica de proteína bcl-2. B: categoría 3+ (20 x ).">
Figure 1B - fiogf49gjkf0d Figura 1B. Detección inmunohistoquímica de proteína bcl-2. B: categoría 3+ (20 x ).
.jpg) fiogf49gjkf0dFigura 2A. Detección inmunohistoquímica de p53. A: caso negativo (20x)."> fiogf49gjkf0dFigura 2A. Detección inmunohistoquímica de p53. A: caso negativo (20x).">
Figura 2A. - fiogf49gjkf0d Figura 2A. Detección inmunohistoquímica de p53. A: caso negativo (20x).
.jpg) fiogf49gjkf0dFigura 2B. Detección inmunohistoquímica de p53. B: categoría 2+ (20x)"> fiogf49gjkf0dFigura 2B. Detección inmunohistoquímica de p53. B: categoría 2+ (20x)">
Figura 2B - fiogf49gjkf0d Figura 2B. Detección inmunohistoquímica de p53. B: categoría 2+ (20x)
|
|
Discusión
El curso clínico y la respuesta al tratamiento de las pacientes con cáncer de mama son muy heterogéneos. La incorporación de nuevos marcadores para la caracterización de estos tumores es útil para la evaluación clínica de las pacientes.
En nuestro estudio, el grado histológico se asocia a la acumulación nuclear de p53 y a la ausencia de la expresión de ER, según lo descrito previamente (Malamou-Mitsi V, 2006). En relación con la metástasis, en nuestro grupo de pacientes hay una asociación muy clara entre el grado histológico y la presencia de metástasis, corroborando resultados descritos previamente (Weigelt B, 2005). A pesar de que el marcador bcl-2 es una proteína antiapoptótica que favorece la supervivencia de la célula tumoral su expresión se ha considerado como un factor de buen pronóstico, apoyando la función de esta proteína de prolongar el ciclo de la célula (Callagy GM, 2006). Aunque la mayoría de los estudios apoyan el papel protector de bcl-2 (Thomadaki H, 2007;), también se ha asociado su expresión a la progresión en las metástasis del cáncer de mama (Planas-Silva MD, 2007). En nuestro estudio no existe tal asociación. La asociación de la expresión de bcl-2 con el grado histológico favorable y la expresión de p53 confirma los resultados previos obtenidos en un conjunto de tumores de mama positivos para bcl-2 y de fenotipo diferenciado, asociados a un mejor pronóstico (Megha T, 2002).
Se ha descrito que la clasificación de los pacientes de cáncer de mama en los subtipos luminal, HER2, basal y normal parece ser esencial debido a su importancia terapéutica (Reis-Filho JS, 2006) y pronóstica (Van de Vijver MU, 2006).
Los tumores IDC de subtipo luminal son los más diferenciados, y su morfología recuerda a la correspondiente del componente luminal del epitelio ductal de la mama (Jones C, 2004). En nuestro grupo de estudio todos los tumores luminales son bcl-2 positivos y esto concuerda con los resultados previos descritos en un grupo de pacientes con DCIS e IDC (Megha T, 2002). Por otra parte, la acumulación nuclear de p53 parece ser una alteración menos frecuente en los tumores luminales, confirmando resultados previos que relaciona un porcentaje bajo de mutaciones p53 en para estos tumores (Sorlie T, 2001). Los tumores de subtipo basal tienden a ser bcl-2 negativos y con una elevada expresión del marcador de proliferación ki-67.
En conclusión, el estudio de marcadores moleculares e inmunohistoquímicos nos ha permitido obtener información adicional para la clasificación de los tumores de mama en subtipos que se diferencian no sólo por morfología sino también por sus características inmunohistoquímicas. Por lo tanto, la confirmación de la implicación de estos marcadores en grupos más numerosos de pacientes puede delimitar de una manera más precisa los subtipos tumorales de cáncer de mama y permite evaluar los factores pronósticos clásicos en este tipo de cáncer tan heterogéneo.
|
|
Bibliografía
Botha JL, Bray F, Sankila R, Parkin DM. Breast cancer incidence and mortality trends in 16 European countries. Eur J Cancer 2003; 39(12):1718-1729.
Callagy GM, Pharoah PD, Pinder SE, Hsu FD, Nielsen TO, Ragaz J, et al. Bcl-2 is a prognostic marker in breast cancer independently of the Nottingham Prognostic Index. Clin Cancer Res 2006;12(8):2468-75.
Greene FL, Page DL, Fleming ID, Fritz AG, Balch CM, Haller DG, Morrow M, eds. AJCC Cancer Staging handbook. TNM classification of malignant tumors, 6th ed. New York: Springer, 2003. 469p.
Jones C, Mackay A, Grigoriadis A, Cossu A, Reis-Filho JS, Fulford L, et al. Expression profiling of purified normal human luminal and myoepithelial breast cells: identification of novel prognostic markers for breast cancer. Cancer Res 2004;64(9):3037-45.
Lacroix M, Toillon RA, Leclercq G. p53 and breast cancer, an update. Endocr Relat Cancer 2006;2(13):293-325
Malamou-Mitsi V., Gogas H, Dafni U, Bourli A, Fillipidis T, Sotiropoulou M, et al. Evaluation of the prognostic and predictive value of p53 and Bcl-2 in breast cancer patients participating in a randomized study with dose-dense sequential adjuvant chemotherapy. Ann Oncol 2006;17(10):1504-11.
Megha T, Ferrari F, Benvenuto A, Bellan C, Lalinga AV, Lazzi S, et al. p53 mutation in breast cancer. Correlation with cell kinetics and cell of origin. J Clin Pathol 2002;55(6):461-6.
Nielsen TO, Hsu FD, Jensen K, et al. Immunohistochemical and clinical characterization of the basal-like subtype of invasive breast carcinoma. Clin Can Res 2004;10:5367-5374.
Planas-Silva MD, Bruggeman RD, Grenko RT, Smith JS. Overexpression of c-Myc and Bcl-2 during progression and distant metastasis of hormone-treated breast cancer. Exp Mol Pathol 2007;82(1):85-90.
Reis-Filho JS, Westbury C, Pierga JY. The impact of expression profiling on prognostic and predictive testing in breast cancer. J Clin Pathol 2006; 59:225-231.
Sorlie T, Perou CM, Tibshrirani R, et al. Gene expression patterns of breast carcinomas distinguish tumor subclasses with clinical implications. Proc Natl Acad Sci USA 2001;98(19): 10869-10874.
Thomadaki H, Talieri M, Scorilas A. Prognostic value of the apoptosis related genes BCL2 and BCL2L12 in breast cancer. Cancer Lett 2007;247(1):48-55.
Van de Vijver MU, He YD, Van´t Veer U, Dai H, Hart AA, Voskuil DW, et al. A gene-expression signature as a predictor of survival in breast cancer. N Engl J Med 2002; 347: 1999-2009.
Weigelt B, Peterse JL, van 't Veer LJ. Breast cancer metastasis: markers and models. Nat Rev Cancer 2005;5(8):591-602
|

 Nº 872. Comunicación libre
Nº 872. Comunicación libre
 Nº 872. Comunicación libre
Nº 872. Comunicación libre