TINCION DE GIEMSA PARA HISTOLOGÍA. DOS PROTOCOLOS DE ACTUACIÓN
El reactivo de Giemsa es un colorante salino formado por eosinatos de azur y de azul de metileno, dando como resultado una coloración polícroma, que permite observar la arquitectura del tejido.
La eosina, como colorante ácido, tiñe el citoplasma celular y las estructuras ácidas hísticas (como los gránulos de los leucocitos polinucleares eosinófilos).Los azures y el azul de anilina, como colorantes básicos, tiñen los núcleos celulares, las estructuras ácidas del tejido y le otorgan un componente metacromático al colorante.
En nuestro servicio utilizamos dos protocolos para la tinción de Giemsa, según el tejido que se vaya a estudiar:
1. Giemsa Modificado:
-Cortes a 4 micras.
-Desparafinar e hidratar.
-Introducir los portaobjetos en solución de Giemsa al 20 % durante 45 minutos.
-Lavar abundantemente en agua corriente.
-Diferenciar en alcohol absoluto, 10 minutos
-Xilol y montar.
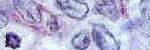
Este protocolo lo utilizamos para las muestras gástricas, pues obtenemos un punto exacto de diferenciación, para observar adecuadamente el helicobacter pilorii
2. Giemsa Directo:
-Cortes a 4 micras.
-Desparafinar e hidratar.
-Teñir con la solución comercial de Giemsa (QCA), directamente sobre el portaobjetos, en horizontal, durante 10 minutos.
-Lavar abundantemente en agua corriente.
-Diferenciar sucesivamente en:
Agua acética (7 gotas de Ac. Acético glacial en 100 cc de agua destilada)
Alcohol de 96
Alcohol isopropílico
Es conveniente controlar la diferenciación al microscopio.
Deshidratar, aclarar y montar.
Este protocolo lo utilizamos para el resto de los tejidos (piel, cilindros de médula ósea, ganglios, incluso en citología, para muestras de orina con sospecha de eosinofilia.)

 Nº 606. Foro técnico
Nº 606. Foro técnico
 Nº 606. Foro técnico
Nº 606. Foro técnico