
 Nº 701. Comunicación libre
Nº 701. Comunicación libre
|
Carcinoma renal asociado a la mutación Xp11.2 Guillermo Muñoz[1], Luis Plaza[1], Francesc Felipo[1], Isabel Marquina[1], Mar Pascual[1], Ana Fuertes[1] |
||
|
lay:none">fiogf49gjkf0dPresentamos el caso de una niña de 9 años con una masa renal izquierda, objetivada mediante técnicas de imagen y posteriormente en la pieza quirúrgica. Ante la histología particular de la lesión y la edad de la paciente, se sospecha un tumor renal asociado a la mutación TFE3. Mediante la detección de la misma por técnicas de inmunohistoquímica, se confirma nuestro diagnóstico de presunción.
|
||
|
|
Se trata de una niña de 9 años que presenta fiebre, vómitos y una masa renal izquierda. En las pruebas de imagen se evidencia dicha masa, localizada en el polo inferior del riñón izquierdo. Se practica una nefrectomía izquierda
|
|
|
|
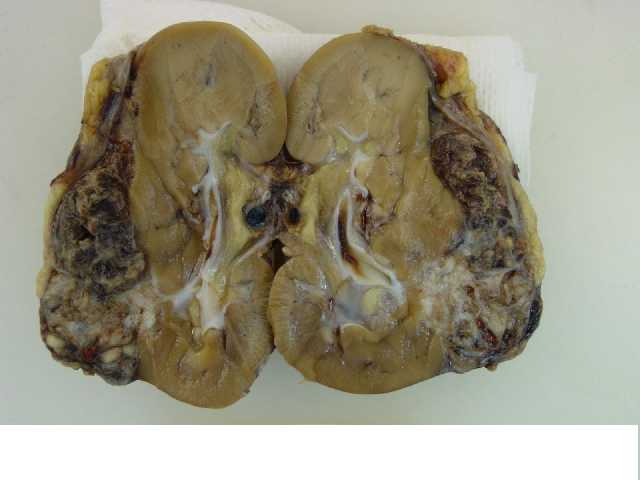
La pieza quirúrgica (riñón izquierdo y uréter) pesa 126 gr. y mide 8 x 5 x 4 cm. Externamente muestra áreas violáceas localizadas en la convexidad. A la apertura, se observa una lesión que se sitúa en su mayor parte en el polo inferior renal y mide 5 cm de diámetro máximo. En la parte superior, la lesión parece despegar la cápsula renal. Presenta una consistencia dura y una coloración marrón negruzca. Está formada por áreas sólidas alternando con otras áreas necrohemorrágicas.
|
|
|
|
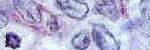
El estudio histológico revela una proliferación celular bien delimitada del parénquima renal normal por una cápsula de tejido fibroconectivo. Las células se disponen en nidos sólidos, separados por finos tractos de tejido fibrovascular. Poseen un voluminoso citoplasma acidófilo, con núcleo grande, cromatina en grumos y nucléolo prominente. Los bordes celulares son netos. En otras zonas, las células forman estructuras tubulares, con una luz central más o menos evidente. También se observan áreas de patrón papilar, con un eje fibrovascular central y células atípicas a ambos lados del mismo. Reseñar también la presencia focal de grupos de células claras, similares a las del carcinoma de células claras convencional. Característicamente, son muy frecuentes los cuerpos de psammoma, distribuidos por todo el tumor.
|
|
|
|
El estudio inmunohistoquímico fue positivo para CD10. Ante la sospecha de un carcinoma renal asociado a la mutación Xp11.2 se realizó inmunohistoquímica para TFE3, que resultó positiva.
|
|
|
|
Se han descrito muy pocos casos de tumores renales asociados a esta translocación, que también se da en el sarcoma alveolar de partes blandas. Deben tenerse en cuenta otros tumores de histología similar, como el angiomiolipoma epitelioide, que está formado por células epiteliales acidófilas, pero que son positivas a MelanA y HMB45. También debe diferenciarse del carcinoma renal asociado a t(6;11), que asimismo posee células similares, pero suelen verse acúmulos de células con núcleo pequeño, escaso citoplasma y un material rosáceo. Otros que deben tenerse en cuenta son el carcinoma papilar y el carcinoma cromófobo.No obstante, todos ellos son TFE3(-). Los carcinomas renales son muy raros en la edad pediátrica. Cuando acontecen, un alto porcentaje está asociado con alguna anomalía genética, incluyendo aquellas que asocian una translocación en el factor de transcripción TF3 en el cromosoma Xp11.2. Dado que los carcinomas renales asociados a esta mutación u otras pueden ser histológicamente indistinguibles de los carcinomas de células claras convencionales, ante cualquier tumor renal en un paciente menor de 25 años, el diagnóstico de carcinoma de células claras deber ser cuestionado.
|
|
|
|
1: Perot C, Boccon-Gibod L, Bouvier R, Doz F, Fournet JC, Freneaux P, Vieillefond A, Couturier J. Five new cases of juvenile renal cell carcinoma with translocations involving Xp11.2: a cytogenetic and morphologic study. Cancer Genet Cytogenet. 2003 Jun;143(2):93-9. 2: Ramphal R, Pappo A, Zielenska M, Grant R, Ngan BY. Pediatric renal cell carcinoma: clinical, pathologic, and molecular abnormalities associated with the members of the mit transcription factor family. Am J Clin Pathol. 2006 Sep;126(3):349-64. 3: Parast MM, Eudy G, Gow KW, Amin M, Shehata B. A unique case of renal carcinoma with Xp11.2 translocations/ TFE3 gene fusions in a 3-year-old child, with coexistent von Hippel-Lindau gene mutation. Pediatr Dev Pathol. 2004 Jul-Aug;7(4):403-6. Epub 2004 Jul 15. 4: Argani P, Lal P, Hutchinson B, Lui MY, Reuter VE, Ladanyi M. Aberrant nuclear immunoreactivity for TFE3 in neoplasms with TFE3 gene fusions: a sensitive and specific immunohistochemical assay. Am J Surg Pathol. 2003 Jun;27(6):750-61. 5: Ladanyi M, Lui MY, Antonescu CR, Krause-Boehm A, Meindl A, Argani P, Healey JH, Ueda T, Yoshikawa H, Meloni-Ehrig A, Sorensen PH, Mertens F, Mandahl N, van den Berghe H, Sciot R, Cin PD, Bridge J. The der(17)t(X;17)(p11;q25) of human alveolar soft part sarcoma fuses the TFE3 transcription factor gene to ASPL, a novel gene at 17q25. Oncogene. 2001 Jan 4;20(1):48-57.
|
|
|
|
- Noemí García Miralles (10/06/2007 13:13:19)
|
|
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 17:19:20
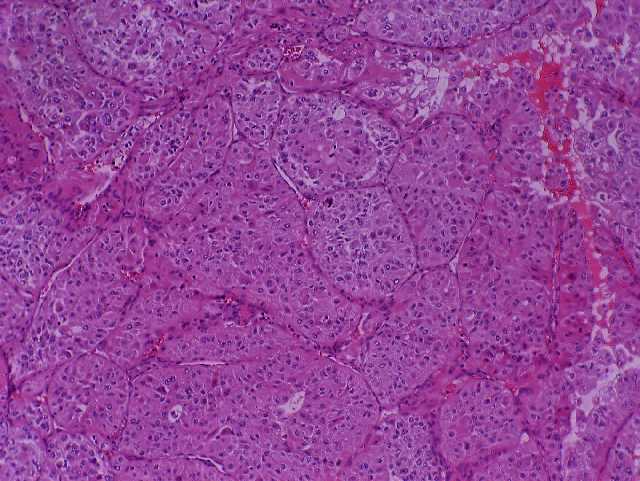 fiogf49gjkf0dNidos sólidos de células atípicas delimitados por tejido fibrovascular.">
fiogf49gjkf0dNidos sólidos de células atípicas delimitados por tejido fibrovascular.">
.jpg) fiogf49gjkf0dCélulas con amplio citolpasma acidófilo, cromatina nuclear en grumos y nucléolo prominente.">
fiogf49gjkf0dCélulas con amplio citolpasma acidófilo, cromatina nuclear en grumos y nucléolo prominente.">
.jpg) fiogf49gjkf0dEn algunas zonas las células se disponen formando túbulos, con una luz central más o menos evidente.">
fiogf49gjkf0dEn algunas zonas las células se disponen formando túbulos, con una luz central más o menos evidente.">
.jpg) fiogf49gjkf0dEn otras áreas, el tumor adquiere un patrón papilar, con un eje conectivo central y células tumorales a ambos lados del mismo.">
fiogf49gjkf0dEn otras áreas, el tumor adquiere un patrón papilar, con un eje conectivo central y células tumorales a ambos lados del mismo.">

.jpg) fiogf49gjkf0dAbundantes cuerpos de psammoma distribuídos por toda la lesión.">
fiogf49gjkf0dAbundantes cuerpos de psammoma distribuídos por toda la lesión.">
.jpg) fiogf49gjkf0dCD10 intensamente positivo">
fiogf49gjkf0dCD10 intensamente positivo">
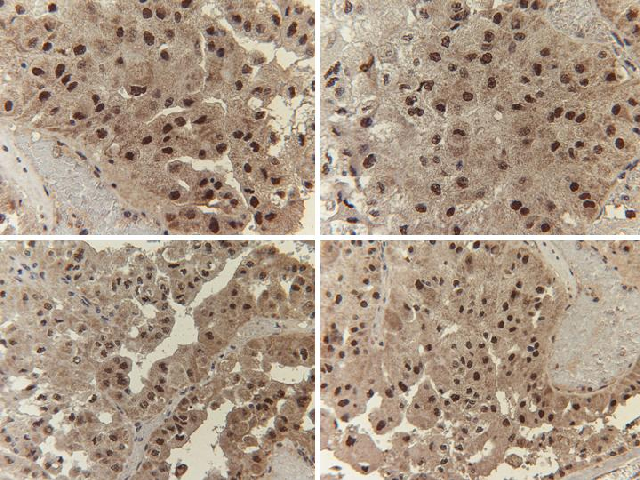 fiogf49gjkf0dTFE3 positiva, lo que confirma el diagnóstico de sospecha">
fiogf49gjkf0dTFE3 positiva, lo que confirma el diagnóstico de sospecha">