|
Miocardiopatía Dilatada Idiopática. Reporte de un caso y breve revisión de la literatura.
Walter Marcial Martínez Rodríguez*, María de los Angeles Milo Anillo*, Magalis Rodríguez Concepción*, Raúl Rua Martínez**, Mayda Martínez Rodríguez***, Raul Rua González****, Olga Forteza Trujillo*
* Hospital Docente "León Cuervo Rubio" CUBA
** Hosp Docente "León Cuervo Rubio" CUBA
*** Poloclínico Docente "Pedro Borras" CUBA
**** Policlínico Docente "Pedro Borrás" CUBA
|
|
Resumen
Paciente masculino, negro, 44 años , municipio San Juan. APP: Miocardiopatía Dilatada desde pequeño. Ingresa con un cuadro de Insuficiencia Cardíaca Congestiva (ICC), soplo sistólico II-III /VI en punta, arritmia, presión venosa central elevada, perfil hepático con muestras de insuficiencia hepática, esputos hemoptoicos, e insuficiencia renal; evoluciona tórpidamente, con un cuadro ICC irreductible, cae en choque y muere. Hallazgos autópsicos: Encéfalo: nada a señalar (n/s); los vasos del polígono de Willis presentaban aterosclerosis ligera; ambos pulmones presentaban infartos hemorrágicos agudos múltiples en lóbulos inferiores, tromboembolismos pulmonares (TEP) de ramas medianas y finas, congestión pasiva crónica pulmonar y esclerosis vascular secundaria; el corazón 1050 gm, presentaba hipertrofia y dilatación global de todas sus cavidades con predominio de los ventrículos, el ventrículo derecho midió (VD) 8 mm y el izquierdo (VI) 12 mm, el Tractus de entrada del VD midió 10 cm y el de salida 13 cm; el Tractus de entrada del VI midió 13 cm y el de salida 15 cms; tricúspide midió 15 cm, pulmonar 9,5 cm, mitral 12 cm, y aorta 9,5 cm, se observó trombosis mural en la orejuela derecha; hígado pesó 2000 gms, presentaba congestión pasiva crónica con necrosis hemorrágica centrolobulillar y cambios grasos a microgoteleta; bazo presentó congestión pasiva aguda, riñones con aspecto característico de riñones de choque. Conclusión: Causa Directa de Muerte: Choque Cardiogénico; Intermedia: Insuficiencia Cardíaca Irreductible; Básica: Miocardiopatía Dilatada; Contribuyente: Tromboembolismos pulmonares múltiples de ramas medianas y finas , con infartos hemorrágicos de ambos lóbulos inferiores. Comentarios: Es la forma más clásica y frecuente de miocardiopatía dilatada. Como posibles factores de riesgos o etiológicos se han sugerido: la existencia de un defecto genético, pues a veces se presenta con carácter familiar; la desnutrición por su frecuencia en países pobres; alguna carencia especifica como la miocardiopatia del Ke-Sahn, de la China, en la que se demostró un déficit de selenio; un factor tóxico como la miocardiopatia de los bebedores de cerveza, debido al cobalto; el alcohol, tabaco, el embarazo y el puerperio, la Diabetes Mellitas y sobre todo las infecciones víricas. Algunos casos de miocardiopatía vírica, clínica o subclínica, pueden pasar a la cronicidad merced a la intervención de un proceso autoinmune o de los factores de riego descritos, dando lugar a la miocardiopatía dilatada después de un período de latencia variable. Teorías actuales atribuyen gran importancia a la posible participación de mecanismos inmunológicos en la patogenia de la MCD, con la miosina como antígeno. La respuesta apoptótica alterada, también ha sido invocada en la etiología de la Miocardiopatía dilatada. En ella se ha demostrado que aproximadamente el 0,2 por ciento de las células tenían características apoptóticas. Esta cantidad aparenta ser poco influyente en la función del corazón, pero si se toma en cuenta que la muerte celular ocurre en cuestión de horas y si se trata de un proceso ininterrumpido sin replicación celular compensadora, alrededor del 50 por ciento de la masa ventricular se perdería en un año.
Por exclusión hemos llegado a pensar que nuestro caso debe caer ; al menos, por el momento; en una Miocardiopatía Dilatada Idiopática, ya que fueron descartadas casi todas las causas conocidas, quedando sólo la posibilidad de una enfermedad inmune o una miocarditis subclínica, pues, el enfermo no reporta ningún cuadro clínico que haga pensar en esa posibilidad; por otra parte no existen antecedentes familiares de MCD. Los hallazgos autópsicos descartaron la posibilidad de una Miocardiopatía secundaria.
|
|
Introduccion
fiogf49gjkf0d La Miocardiopatía Dilatada Idiopática (MDI) es la forma más clásica y frecuente de Miocardiopatía dilatada (MD). Como posibles factores de riesgos o etiológicos se han sugerido: la existencia de un defecto genético, pues a veces se presenta con carácter familiar; la desnutrición por su frecuencia en países pobres; alguna carencia especifica como la Miocardiopatía del Ke-Sahn, de la China, en la que se demostró un déficit de selenio; un factor tóxico como la Miocardiopatía de los bebedores de cerveza, debido al cobalto; el alcohol, tabaco, el embarazo y el puerperio, la Diabetes Mellitas y sobre todo las infecciones víricas. Algunos casos de Miocardiopatía vírica, clínica o subclínica, pueden pasar a la cronicidad merced a la intervención de un proceso autoinmune o de los factores de riesgo descritos, dando lugar a la Miocardiopatía dilatada después de un período de latencia variable. Teorías actuales atribuyen gran importancia a la posible participación de mecanismos inmunológicos en la patogenia de la MCD, con la miosina como antígeno. La respuesta apoptótica alterada, también ha sido invocada en la etiología de la Miocardiopatía dilatada. En ella se ha demostrado que aproximadamente el 0,2 por ciento de las células tenían características apoptóticas. Esta cantidad aparenta ser poco influyente en la función del corazón, pero si se toma en cuenta que la muerte celular ocurre en cuestión de horas y si se trata de un proceso ininterrumpido sin replicación celular compensadora, alrededor del 50 por ciento de la masa ventricular se perdería en un año. Con nuestro trabajo hemos querido contribuir con el conocimiento que se tiene sobre Miocardiopatía Dilatada.
|
|
Material y Métodos
|
|
Presentación de Caso
fiogf49gjkf0d H.Cl: 170553,A-41-05, masculino, de la raza negra, 44 años de edad, del municipio San Juan y Martínez. APP: Miocardiopatía Dilatada desde pequeño con repetidos ingresos y variados tratamientos. Con un ingreso 15 días antes, por marcado edema en miembros inferiores, anorexia, decaimiento. Hace aproximadamente 10 días presenta decaimiento, anorexia y pérdida de peso, edemas en miembros inferiores. Hace más o menos 2 o 3 días presenta dolor epigástrico mantenido que se irradia a hipocondrio derecho; anorexia y marcada astenia, además de presentar tos y expectoración blanquecina con falta de aire a los pequeños esfuerzos y al decúbito. Durante su evolución se mantiene el dolor epigastrio unido al decaimiento marcado. La tos se intensifica y la expectoración se oscurece, mucosas hipocoloreadas, abdomen suave depresible, doloroso en epigastrio e hipocondrio derecho, hepatomegalia, edema en miembros inferiores. Los esputos son hemoptoicos; se acompañan de disnea, dolor en manos, tórax y abdomen. Se traslada a la UCIM donde se recibe con polipnea, mucosas ictéricas; al Examen Físico (EF): crepitantes en ambos campos pulmonares, más marcados en pulmón izquierdo. FR36. Aparato Cardiovascular: Ruidos cardiacos rítmicos taquicárdicos con galope izquierdo; SS III / VI. Abdomen distendido que impresiona presenta ascitis. Edema en miembros inferiores de difícil godet.
Rx Tórax: cardiomegalia global severa lesiones inflamatorias severas en base derecha.
A los 2 días de ingresado se recibió el resultado de un perfil hepático: transaminasa glutámico pirúvica (TGP) 60, transaminasa glutámico oxaloacética (TGO) 90, Timol 14, triglicéridos: 1.43 mmol/L; colesterol 2.3 mmol/L; Bilirrubina: Directa:13, Total:42. A los 9 días de ingresado el paciente se encuentra consciente, orientado, respiración espontánea, abundante esputos hemoptoicos. F.R. 20-24. T.A. 130/70. FC 120-128.T 36 grados C. Mucosa ictéricas y húmedas. A.R: murmullo vesicular disminuido con estertores crepitantes en ambas bases a predominio de la base derecha. A. Cardiovascular: SS II-III/ VI, visible y audible en punta. Abdomen: distendido hígado rebasa el reborde costal 4 dedos, duro, doloroso. Edemas en miembros inferiores +++. Complementarios: Hb: 10. 2 g/l; Leucocitos: 12x 109, Eritro: 5 Mm./h; glicemia: 4.7 ml/l; creatinina 163 mmol/l. Rx de tórax: Cardiomegalia global severa y lesiones inflamatorias y/o congestivas en campo pulmonar izquierdo y base derecha. A los 11 días de ingreso: muy ansioso, intranquilo, polipneíco, taquicárdico, polidipsia, muy escasa diuresis, muy mala ventilación por lo que requiere intubación; abundantes secreciones oro traqueales; se acopla al Mark-8, cae en estupor profundo, reactivo al dolor, al llamado, hipoglicémico (glicemia:1.1 g/l), abundante contenido en la aspiración gástrica, T.A.: 90/40 mm de Hg; Frecuencia cardíaca: 64 por minuto, Frecuencia respiratoria: acoplado, continúa evolucionando tórpidamente y fallece a los 15 días de ingresado en un cuadro de insuficiencia cardíaca congestiva descompensada e irreductible.
Hallazgos Autópsicos.
Macroscópicos:
Cadáver de persona de mediana edad, color de la piel negra, sexo masculino, con ostensible pérdida de peso, presenta edema en miembros inferiores ++.
Por Aparatos:
Sistema Nervioso Central: El encéfalo pesó 1180 Gm. Los vasos del polígono de Willis no presentaron alteración.
Aparato Respiratorio: Congestión pasiva crónica pulmonar. Infartos hemorrágicos pulmonares múltiples, en ambos lóbulos inferiores (Figura1). Tromboembolismos pulmonares (TEP), en ramas medianas de la arteria pulmonar, en ambos lóbulos inferiores.
Aparato Cardiovascular: Cor Bovis (Figura 1), pesó 1050 Gm, el ventrículo derecho (VD) midió 0.8 cm; el ventrículo izquierdo (VI) midió 2.2 cm; el Tractus de entrada del VD (TEVD) midió 10 cm; el tractus de salida del VD (TSVD) midió 13 cm; el Tractus de entrada del VI (TEVI) midió 13 cm.; y el Tractus de salida del VI (TSVI) midió 15 cm. Existía dilatación severa de las 4 cavidades(Figura 2,3). Se apreciaron calcificaciones en dos de las sigmoideas de la válvula aórtica. El sistema valvular presentaba ligera dilatación: la válvula tricúspide (T) midió 15 cm; la válvula mitral (M) 12 cm; la pulmonar (P) 9.5 cm., y la aórtica (A) 9.5 cm. El epicardio no presentó alteración (N/S), el saco pericárdico contenía líquido en cantidad y calidad normal. El pericardio N/S. La aorta y sus ramas mayores presentaban estrías adiposas. Las coronarias presentaban estrías adiposas.
Aparato Digestivo: Esófago, estómago, e intestino: N/S.
Hígado: Aumentado de peso y volumen, con cambios grasos moderados, al corte con aspecto de hígado en nuez moscada.
Vesícula y vías biliares: N/S
Páncreas: N/S
Aparato Génito-Urinario: Riñones de Shock.
Sistema Hemolinfopoyético: Congestión pasiva crónica esplénica
Sistema Endocrino: N/S
Microscópicos:
Se confirman los hallazgos macroscópicos. El miocardio presentó fibras hipertróficas con cariopicnosis y polimorfismo nuclear, como corresponde a los núcleos de las fibras miocárdicas hipertróficas, pero conjuntamente se observaron fibras adelgazadas y estiradas, fibrosis intersticial y endocárdica focal, áreas focales de cicatrización mayor que la que debería corresponder a una simple fibrosis intersticial, sustituyendo a grupos de células. El hígado presentó congestión pasiva crónica hepática con necrosis hemorrágica centrolobulillar, submasiva, con inversión del patrón lobulillar, hecho que explica la insuficiencia hepática demostrada en el perfil hepático realizado al paciente
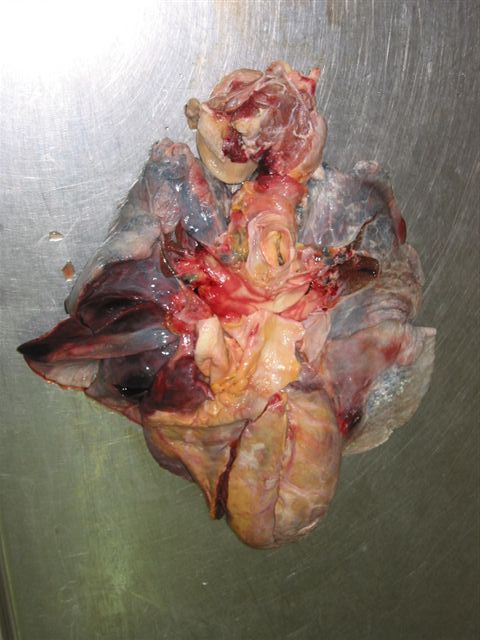 fiogf49gjkf0dEn la imagen apreciamos los infartos hemorrágicos pulmonares y un corazón anormalmente agrandado"> fiogf49gjkf0dEn la imagen apreciamos los infartos hemorrágicos pulmonares y un corazón anormalmente agrandado">
Figura 1 - fiogf49gjkf0d En la imagen apreciamos los infartos hemorrágicos pulmonares y un corazón anormalmente agrandado
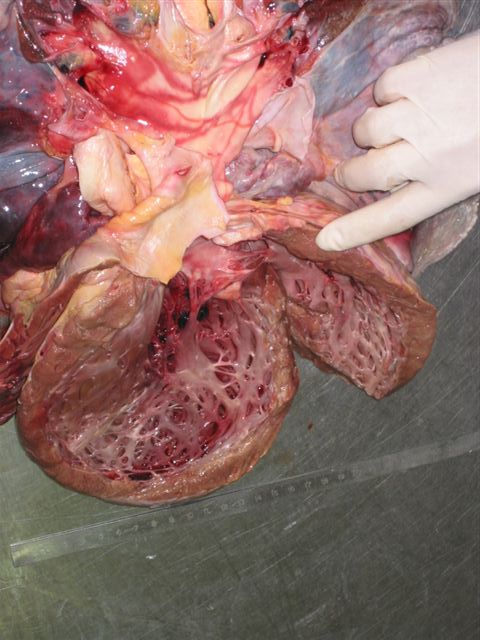 fiogf49gjkf0dApreciamos la dilatación de la cavidad ventricular izquierda"> fiogf49gjkf0dApreciamos la dilatación de la cavidad ventricular izquierda">
Figura 2 - fiogf49gjkf0d Apreciamos la dilatación de la cavidad ventricular izquierda
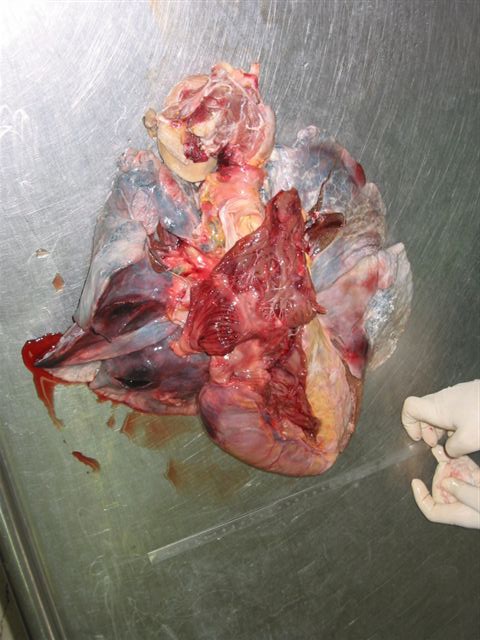 fiogf49gjkf0dDilatación de la cavidad VD"> fiogf49gjkf0dDilatación de la cavidad VD">
Figura 3 - fiogf49gjkf0d Dilatación de la cavidad VD
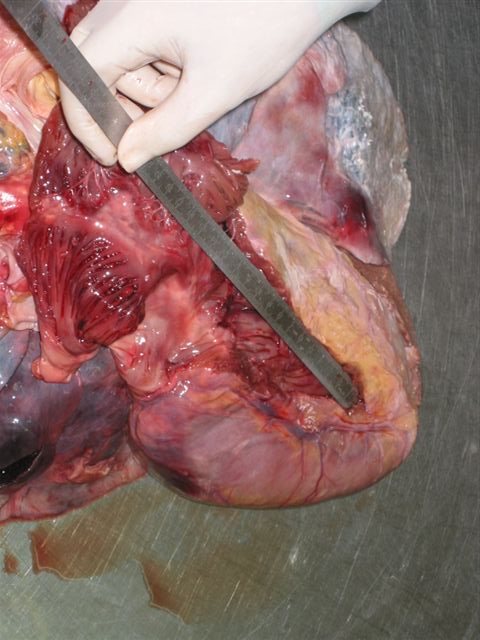 fiogf49gjkf0dTractus de salida del VD (13 cms)"> fiogf49gjkf0dTractus de salida del VD (13 cms)">
Figura 4 - fiogf49gjkf0d Tractus de salida del VD (13 cms)
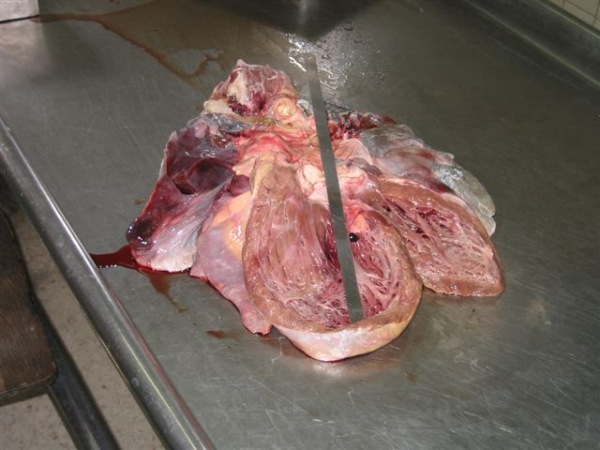 fiogf49gjkf0dTractus de salida del VI (15cm)"> fiogf49gjkf0dTractus de salida del VI (15cm)">
Figura 5 - fiogf49gjkf0d Tractus de salida del VI (15cm)
|
|
Discusión
fiogf49gjkf0d
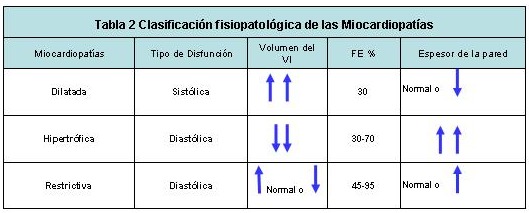
El término Miocardiopatía (literalmente, enfermedad del músculo cardíaco) podría aplicarse casi a cualquier cardiopatía, pero por acuerdo unánime se emplea para designar a las cardiopatías resultantes de alguna afección primaria del miocardio. Es una designación algo arbitraria y a menudo decepcionante cuando se repasan las distintas clasificaciones (1,2) porque algunos autores excluyen de ellas a cualquier proceso miocárdico de causa conocida, mientras que otros, con un criterio más amplio (al que nos sumamos los autores de este trabajo), incluyen a las cardiopatías que se manifiestan primariamente por insuficiencia cardíaca. . En muchos casos las miocardiopatías son idiopáticas, pero también pueden ser secundarias (Tabla I). Ha sido de un gran avance en el conocimiento de las miocardiopatías la demostración de que muchos pacientes considerados anteriormente como idiopáticos tienen en realidad ciertas alteraciones genéticas del metabolismo energético del corazón o de las proteínas contráctiles o estructurales que constituyen el trasfondo de la disfunción miocárdica (3). Por tanto las distinciones etológicas se han convertido en algo difícil. El cuadro clínico de las miocardiopatías está determinado en gran parte por alguna de las tres formas clínicas, funcionales y anatomopatológicas resumida en la Tabla II. Según la alteración funcional predominante, hiposistolia o hipodiastolia, definida en la práctica a partir de la fracción de eyección (FE) y del volumen ventricular (dos datos que se obtienen fácilmente mediante ecocardiograma bidimensional o el ventriculograma isotópico), las miocardiopatías se clasifican en dilatadas y no dilatadas, y estas últimas a su vez, en hipertróficas y restrictivas, mientras que la dificultad de llenado diastólico se debe a la hipertrofia, la infiltración o fibrosis de la pared. De estos tres grupos, la forma clínica más frecuente es la dilatada. Un resumen de las causas más frecuentes de las Miocardiopatías puede ser apreciado en el Cuadro I. La respuesta apoptótica alterada, también ha sido invocada en la etiología de la Miocardiopatía dilatada. En ella se ha demostrado que aproximadamente el 0,2 por ciento de las células tenían características apoptóticas. Esta cantidad aparenta ser poco influyente en la función del corazón, pero si se toma en cuenta que la muerte celular ocurre en cuestión de horas y si se trata de un proceso ininterrumpido sin replicación celular compensadora, alrededor del 50 por ciento de la masa ventricular se perdería en un año.(4)
Miocardiopatía Dilatada O Congestiva.
Constituye un síndrome que refleja depresión intensa de la contractibilidad del Miocardio (FE menor del 30 %) y la dilatación ventricular dilatadora compensadora, cuyas manifestaciones capitales son: la insuficiencia cardiaca congestiva y la cardiomegalia a expensas, sobre todo, del ventrículo izquierdo. Se produce con mayor frecuencia en gente de mediana edad y es más común en los hombres que en las mujeres. Pero la enfermedad ha sido diagnosticada en gente de todas las edades, incluso en niños. La sintomatología de la insuficiencia cardiaca (disnea, fatiga, ingurgitación, yugular, hepatomegalia y edemas) aparece tardíamente, cuando existe ya una gran cardiomegalia, por lo que representa la etapa final de un proceso subclínico cuya antigüedad casi siempre se ignora. La taquicardia sinusal puede ser muy llamativa. El signo auscultatorio más típico es el galope protodiastólico o de sumación; con frecuencia se perciben soplos de insuficiencia mitral funcional, ligera o moderada por disfunción del músculo papilar o dilatación del anillo, o de insuficiencia tricuspidea. El 20 % de los pacientes presenta fibrilación auricular. (5-8) (Cuadro II)
El estudio anatomopatológico(Cuadro III, IV) muestra una importante dilatación de las cuatro cavidades, con predominio del ventrículo izquierdo, cuyas paredes son flácidas y delgadas, aunque el peso total se encuentre aumentado. Se observa trombosis intraventricular en el 75 % de los enfermos, que puede ser fuente de embolias. En el estudio histológico se comprueba hipertrofia de las células musculares y pequeños focos dispersos de fibrosis intersticial cicatrizal, que corresponde al estadio final reparativo de una lesión y las bases iniciales se desconocen. La necrosis o la infiltración celular son escasas o ineficientes (9). Podría tratarse de un proceso de destrucción celular (miocitolisis focal difusa) de origen inflamatorio, quizás vírico o autoinmune, puede ser resultado de la isquemia focal (necrosis celular isquémica) producida por la destrucción de los pequeños vasos lesionados por la inflamación o por un espasmo microvascular a la hiperreactividad micro circulatoria. Como sugiere la Miocardiopatía hereditaria del Hamster Sirio, en el que se ha comprobado la existencia de una sobrecarga intracelular de calcio (7).
Etiología
Como hemos podido apreciar en el cuadro I, dentro de las causas más frecuentes de Miocardiopatía Dilatada tenemos:
Alcohol y otras sustancias tóxicas
Hasta un 30 % de los casos de Miocardiopatía Dilatada están relacionados con el consumo excesivo de alcohol. Después de muchos años de beber en exceso, el corazón puede debilitarse debido al efecto tóxico del alcohol en las células musculares. Además, los bebedores excesivos suelen beber alcohol en lugar de comer alimentos, lo cual deriva en una nutrición deficiente. Otras sustancias tóxicas, incluidas algunas sustancias químicas y pesticidas, y el consumo abusivo de drogas también han demostrado debilitar el músculo cardíaco.
Nutrición deficiente
Si el organismo no recibe una cantidad adecuada de las vitaminas y minerales esenciales que necesita, especialmente, vitamina B1, puede producirse una Miocardiopatía dilatada. Esto es más común en los países en vías de desarrollo que en los Estados Unidos y otros países desarrollados.
Inflamación
En una enfermedad poco común denominada «miocarditis», el músculo cardíaco se hincha o inflama debido a una infección viral, con menor frecuencia una infección bacteriana, u otro proceso infeccioso. El enfermo podría no presentar síntoma alguno. Podría tener una sensación de dolor en el pecho y sentirse cansado como si tuviera un catarro fuerte o gripe. Generalmente, un caso leve de miocarditis desaparecerá sin dejar secuelas. Es más, es posible que una persona padezca de esta enfermedad sin saberlo. Los casos graves a menudo no se diagnostican hasta que no se manifiesten síntomas de insuficiencia cardíaca. Incluso un caso grave podría desaparecer sin ser advertido, pero estos casos graves generalmente ocasionan un daño irreversible y permanente al músculo cardíaco.
Embarazo y parto.
En casos excepcionales, una mujer podría padecer una enfermedad del músculo cardíaco hacia el final de un embarazo o durante los primeros meses después de dar a luz. Esto se denomina «Miocardiopatía periparto». Sufra o no una infección viral o bacteriana, el músculo cardíaco podría inflamarse. Los investigadores no han logrado descubrir el motivo de la inflamación. Se sabe que si una mujer se restablece y vuelve a quedar embarazada, corre el riesgo de sufrirla nuevamente. Además, en los Estados Unidos, las afroamericanas sufren de Miocardiopatía periparto con mayor frecuencia que las otras. (10-22)
Herencia
Aunque los científicos no saben si existe un gen que cause Miocardiopatía Dilatada, muchos creen que existe una predisposición hereditaria. Señalan casos en los que los miembros de la misma familia tienen la enfermedad. Además, algunos trastornos cerebrales de origen genético, tales como la distrofia muscular, están relacionados con una enfermedad del músculo cardíaco.(23-25)
Síndrome de Inmunodeficiencia Adquirida (SIDA)
Los estudios recientes han demostrado que el sida aumenta el riesgo de Miocardiopatía Dilatada. Entre el 1 % y el 8 % de los enfermos con sida sufren de este tipo de daño cardíaco. (26)
La mayoría de los casos de Miocardiopatía dilatada se denominan «idiopáticos», lo cual significa que no puede determinarse exactamente su causa. Algunos médicos piensan que podrían deberse a infecciones virales. Lamentablemente, los virus son difíciles de detectar en muestras de laboratorio. Como la persona pudo haber sufrido la infección meses o incluso años antes de presentar síntomas de un debilitamiento del músculo cardíaco, es difícil determinar exactamente la causa.
La MDI o Miocardiopatía Congestiva Idiopática; es la forma más clásica y frecuente de Miocardiopatía Dilatada. Como posibles factores de riesgos o etiológicos se han sugerido: la existencia de un defecto genético, pues a veces se presenta con carácter familiar (5,6,7); la desnutrición por su frecuencia en países pobres; alguna carencia especifica como la Miocardiopatía del Ke-Sahn, de la China, en la que se demostró un déficit de selenio; un factor tóxico como la Miocardiopatía de los bebedores de cerveza, debido al cobalto; el alcohol, tabaco, la Diabetes Mellitas y sobre todo las infecciones víricas. Algunos casos de Miocardiopatía vírica, clínica o subclínica, pueden pasar a la cronicidad merced a la intervención de un proceso autoinmune o de los factores de riesgo descritos, dando lugar a la Miocardiopatía dilatada después de un período de latencia variable (8,9). Teorías actuales atribuyen gran importancia a la posible participación de mecanismos inmunológicos en la patogenia de la MCD, con la miosina como antígeno (10).
Por exclusión hemos llegado a pensar que nuestro caso debe ser considerado; al menos, por el momento; como una Miocardiopatía Dilatada Idiopática, ya que fueron descartadas casi todas las causas conocidas, quedando sólo la posibilidad de una enfermedad inmune o una miocarditis subclínica, pues, el enfermo no reporta ningún cuadro clínico que haga pensar en otra posibilidad; por otra parte no existen antecedentes familiares de MCD. Los hallazgos autópsicos descartaron la posibilidad de una Miocardiopatía secundaria. Queda por investigar la sensibilidad a algún fármaco tomado por el paciente en algún momento de su juventud.
Tabla 1 Causas importantes de Miocardiopatía y miocarditis
|
1. Inflamatorias.
a) Infecciosas:
Virales
Rickettsias
Bacterianas
Por Micobacterias
Por Espiroquetas
Micóticas
Parasitarias
b) No infecciosas
Enfermedades de la Colágena
Granulomatosis Kawasaki
2. Metabólicas:
a) Nutricionales:
Tiamina
Kwashiorkor
Escorbuto
Hipervitaminosis D
Obesidad
Deficiencia de Selenio
Deficiencia de Carnitina
b) Alteración del metabolismo
Gota
Oxalosis Porfiria
c) Desequilibrios electrolíticos |
3 Infiltrativas:
a) Amiloidosis
b) Hemocromatosis
c) Neoplásicas
d) Trastornos por almacenamiento
de Glucógeno
e) Sarcoidosis
f) Mucopolisacaridosis
g) Enfermedad de Fabry
h) Enfermedad de Whipple
i) Enfermedad de Gaucher
j) Esfingolipidosis
4. Diversas, adquiridas:
a) Miocardiopatía puerperal
b) Obesidad
5. Hipersensibilidad:
a) Metildopa
b) Penicilina
c) Sulfamidas
d) Tetraciclina
e) Fenindiona
f) Fenilbutazona
g) Farmacos antituberculosos
h) Miocarditis por células gigantes
i) Rechazo del corazón trasplantado
|
6. Genéticas:
a) Miocardiopatía hipertrófica
Con gradiente Sin gradiente
b) Neuromusculares
Distrofia muscular de Duchenne Distrofia muscular fascio- escapulohumeral
Distrofia de Erb de cintura escapular y pélvica
Distrofia miotónica
Ataxia de Friedreich
Síndrome Kearns-Saynes
Miocardiopatía por Nemalina
Miocardiopatía multicéntrica
7. Idiopáticas:
a) Miocardiopatía dilatada Idiopática
b) Miocardiopatía restrictiva Idiopática
c) Miocardiopatía; Hipertrófica Idiopática
d) Miocardiopatía Idiopática ventricular derecha.
|
 fiogf49gjkf0d"> fiogf49gjkf0d">
Tabla II - fiogf49gjkf0d
 fiogf49gjkf0d"> fiogf49gjkf0d">
Cuadro I - fiogf49gjkf0d
 fiogf49gjkf0d"> fiogf49gjkf0d">
Cuadro II - fiogf49gjkf0d
 fiogf49gjkf0d"> fiogf49gjkf0d">
Cuadro III - fiogf49gjkf0d
 fiogf49gjkf0d"> fiogf49gjkf0d">
Cuadro IV - fiogf49gjkf0d
|
|
Conclusiones
|
|
Agradecimientos
|
|
Bibliografía
1) Reporte de la OMS/IFSC. Task Force on the definition and classification of cardiomyopathies. Br Heart J 44:672, 1980.
2) Richardson P; et al: Report of 1995 WHO/IFSC Task Force on the definition and classification of cardiomyopathies. Circulation 93:841, 1996.
3) Keating MT, Sanguinetti MC: Molecular genetic insights into cardiovascular disease. Science 272:681, 1996.
4) Narula J, Haider N, Virmani R. Apoptosis in myocytes in stge heart failure. N Engl J Med 1996;335:1182-9
5) Navarro- López F. Miocardiopatías. En: Farreras-Rozman. Medicina Intema. 13era Ed. Barcelona. Doyma Libros, 1996. 557-566.
6)Braunwald E. Miocardiopatias y miocarditis. En- Braunwald E. Tratado de Cardiologia. 4ta Ed Madrid Mc Graw-Hill. Interamericana de España, 1993.1594-1662.
7) Griining E, Brown B, Franz W, Zehelein J, Ro"bauer W, Frey N Clinical aspect and follow up in dilated cardiomyopathy. Z Kardiol, 1995; 84 Suppl 4. 39-40.
8) Strauer BE. Consensus-Konferenz. Myokarditis dilatative Kardiomyopathie. Internist (Bell), 1995.36(5) 484-502
9) Goldman JH, McKenna WJ. Inmunopathogenesis of dilated cardiomyopathies. Curr opin Cardiol, 1995; 10(3).306-11.
10)Demakis JG, Rahimtcola SH. Peripartum Cardiomyopathy. Circulation, 114:964, 1971
11)Friedberg CK. Miocardiopathy. Circulation, 1971, 114:935.
12)Perloff JK. The Cardiomiopathies. Current Perstives. Circulation, 1971, 11:942.
13)Hull E, Hafkesbring E. Toxic postpartal heart disease. New Orleans Med Surg, 1937, 89:550.
14)Seftel Hsusser M. Maternity and myocardial failure in african women. Brit. Heart J., 1981, 23:43.
15)Walsh JJ, Burch GE, Black W, Ferrans V, Hibbs H. Idiopathic Myocardiopathy of the puerperium. Circulation, 1965, 32:19.
16)Valdés EF. Miocardiopatías paraneoplásicas. Rev Clin Esp, 1970, 120:247.
17)Goodwin JF. Congestive and hipertrophic Myocardiopathy. Lancet, 1970, 1:731.
18)Sakakibara S, Sekiguchi M, Konno S, Kusumoto M. Idiopathic postpartum cardiomyopathy: report of a case with special reference to its ultrastructural changes in the myocardium as studied by endomyiocardial biopsy. Amer Heart J., 1970, 80:385.
19)Meadows WR. Idiopathic myocardial failure in the last trimester of pregnancy and puerperium. Circulation, 1957, 15:903.
20)Stuart KL. Cardiomyopathy of pregnancy and puerperium. Quart J Med , 1968, 37:463.
21)Burch GE. The effect of prolonged bed rest on pospartal cardiomyopathy. Amer Heart J, 1981, 81:186.
22)Gouley B, Mc Millan T, Bellet S. Idiopathic Myocardial degeneration associated with pregnancy specially the puerperium. Amer J Med Sci, 1937, 194:185.
23)Johnson JB, Mir GH, Flores P, Mann M. Idiopathic heart disease associated with pregnancy. Am Heart J, 1966, 72:809.
24) Mc Minn TR, Ross J. Hereditary dilated cardiomyopathy. Clin Cardiol, 1995, 18 (1) 7-15.
25) Schowengerdt KO, Towbin JA. Genetic basis of inherited . cardiomyopathies. Curr Opin Cardiol,1995;1J(3):312-21
26) Durand JB, Abchee AB, Roberts R. Molecular and clinical aspecl of inherited cardiomyopathies
27) Cetta F, Michels W. The autoinmune basis of dilated cardiomiopathy. Ann Med, 1995.27 (2): 169-73.
|
|



