
 Conferencia
Conferencia
|
Ernesto García Ureta* |
|
|
La PTB es una técnica broncoscópica de aparición relativamente reciente, utilizada para obtener material diagnóstico citológico y/o histológico de procesos adyacentes al árbol traqueo-bronquial. A pesar de su utilidad diagnóstica exclusiva en algunos aspectos y de evitar otros procedimientos más caros y agresivos, es una técnica infrautilizada, que aún no ha generalizado su uso. La principal razón de esta en el hecho, de que para adquirir una experiencia adecuada el broncoscopista necesite un tiempo prolongado y un número abundante de punciones, junto a ello hay que señalar la falta de programas de entrenamiento, el que transmite cierta sensación de peligro por la proximidad de grandes vasos, la dificultad de obtener unos buenos resultados iniciales y el coste de las agujas, que son desechables, ayudan a ampliar la falta de aceptación del procedimiento.
Este tipo de punciones tiene un bajo porcentaje de complicaciones y en general no son graves. Es remarcable la importancia de la presencia del citopatólogo en el momento de la punción para realizar una valoración rápida con el fin de reducir las muestras insatisfactorias. Variaciones de la técnica como la monitorización mediante tomografía axial computarizada o el empleo de ultrasonidos mejoran la rentabilidad diagnóstica.
La PTB se hace necesaria para aumentar la exactitud en el estadiaje del cáncer de pulmón mejorando así la selección de los pacientes que van a ser sometidos a resección pulmonar, así como para tener el diagnóstico de los recidivas ganglionares con fines preventivos y terapéuticos.
|
||
|
|
La punción transbronquial (PTB) es una técnica broncoscópica de aparición relativamente reciente que permite la obtención de muestras citológicas e histológicas de lesiones adyacentes al árbol traqueobronquial. En la practica las punciones transbronquiales, las que generalmente guardan relación con procesos en los que no se ha conseguido el diagnóstico por otros medios, esta ofreciendo buenos resultados en el diagnóstico y estadiaje del carcinoma de pulmón. Esta técnica es segura y económica y permite el diagnostico y estadiaje del carcinoma de pulmón en una sola sesión broncoscópica.
|
|
|
|
El broncoscopio es introducido en el árbol traqueo-bronquial a través de la cavidad nasal u oral y la PTB ha de hacerse antes que otros procedimientos diagnósticos tales como lavados y cepillados bronquiales o biopsias para minimizar la contaminación con sangre o con células exfoliadas del epitelio respiratorio (Figura 2).
|
|
|
|
Indicaciones. Contraindicaciones y complicaciones INDICACIONES
La PTB aumenta la utilidad de la broncoscopia en el diagnóstico de una gran variedad de procesos. La indicación mas importante y frecuente es la estatificación del cáncer de pulmón, pero también es de utilidad en el diagnostico de lesiones submucosas, lesiones necróticas y lesiones endobronquiales muy vascularizadas, lesiones pulmonares periféricas, masas hiliares mediastínicas, también se ha utilizado para drenaje y estudio del líquido pericárdico.
En los tumores necróticos endobronquiales una delgada aguja puede ir a través de la parte necrótica y obtener células neoplásicas para una evaluación citológica en este contexto la biopsia casi siempre obtiene material no diagnóstico (Figura 5). En caso de los tumores endobronquiales muy vascularizados tales como el carcinoide la aspiración citológica causa mínima hemorragia mientras la biopsia o el cepillado bronquial puede motivar un importante sangrado (Figuras 6 y 7). La PTB obtiene buenos resultados diagnósticos en los tumores peribronquiales y submucosos. Los tumores de localización peribronquial pueden fácilmente ser muestreados por PTB mientras que la biopsia es incapaz de penetrar a través de la pared del bronquio y alcanzar la lesión (Figura 8). Las metástasis tumorales son los tumores más frecuentes de pulmón. Muchos están localizados en la periferia del pulmón como resultado de su extensión hematógena al pulmón aunque también algunos pueden alcanzar el pulmón por vía linfoide, las metástasis endobronquiales son menos frecuentes, el carcinoma renal y el carcinoma de colon tienden a producir metástasis endobronquiales. La correcta tipificación del tumor con el material obtenido por la PTB puede ser alcanzado valorado el aspecto celular la disposición celular y las técnicas de inmunocitoquímica. La presencia de masas mediastínicas puede ser debida a tumores primarios, tumores metastáticos y enfermedades no neoplásicas. Las lesiones no neoplásicas del mediastino son mucho menos frecuentes que los procesos tumorales. La PTB tiene un papel limitado en los procesos no tumorales de mediastino, las referencias bibliográficas están generalmente relacionadas con la sarcoidosis y la tuberculosis. La presencia de células epitelioides y/o la presencia de células gigantes multinucleadas no son específicas y pueden significar ser un componente de algunas neoplasias mediastínicas como seminoma o enfermedad de Hodgkin. En la literatura existen algunas referencias en el diagnóstico de pacientes con SIDA, nosotros también tenemos algunos casos. Entre los linfomas más comunes que podemos encontrar en el mediastino estaría la enfermedad de Hodgkin, particularmente el tipo esclerosis nodular, su diagnóstico está basado en la identificación de la célula de Reed-Stenberg sin embargo es conocido que en diversas situaciones de pueden encontrar células similares a las de Reed-Stenberg. Es de señalar también que la esclerosis nodular de la Enfermedad de Hodgkin motivada por la fibrosis puede obtener muestras escasamente celulares o inadecuadas. La presencia de células epitelioides nos puede hacer malinterpretar la muestra como correspondientes a adenitis granulomatosa. Los linfomas primarios de mediastino no Hodgkin son generalmente linfomas difusos de células grandes, el diagnóstico, como correspondiente a malignidad y la tipificación como correspondiente a linfoma no suele plantear especiales dificultades diagnósticas (Figuras 9 y 10). En cuanto al estadiaje del carcinoma de pulmón no plantea especiales dificultades salvo aquellas que puedan derivarse de la escasez de la muestra, la necrosis y/o la degeneración quística del carcinoma epidermoide puede incidir en este aspecto. En cuanto a la tipificación tumoral, el clínico se encuentra especialmente interesado en que le digamos si se trata de un oat-cell o de otro tipo de tumor, ya que el planteamiento para el tratamiento ha de ser distinto (Figuras 11 y 12). El oat-cell en su presentación clásica no suele plantear especiales dificultades para su reconocimiento, como en otras topográfias, su diagnostico diferencial ha de incluir otros tumores de células pequeñas quizá aquí merezca la pena reseñar que los linfomas centrocíticos por la tendencia de estas células a presentarse agrupadas puede plantear alguna dificultad, la presencia o no de nucleolo junto con la inmunocitoquímica ayuda a resolver este problema. Es de señalar que en pacientes con procesos mediastinitos hay 4 factores que indican un peor pronóstico: ganglios subcarinales positivos, afectación contralateral, afectación ganglionar en diversos niveles y extensión extracapsular del tumor, la PTB proporciona información en 3 de estas categorías. En metástasis en ganglios mediastínicos de otras topografías no pulmonares la PTB también puede mostrar su utilidad (Figura 13). Los derrames pericardicos de localización posterior, presentan dificultad para el drenaje percutaneo, en ellos la PTB es un método seguro y bien tolerado para su evacuación y diagnostico. CONTRAINDICACIONES Y COMPLICACIONES
Trastornos de la coagulación, fallo respiratorio y tos incontrolable pueden ser contraindicaciones relativas de PTB. Pacientes con sospecha de quiste hidatídico tampoco serian candidatos para la PTB.
Este tipo de punciones tiene un bajo porcentaje de complicaciones y en general no son graves Los pacientes pueden presentar una hemoptisis transitoria poco importante. Alrededor de un 10% de los pacientes presentan en discreto aumento de la temperatura pero la bacteriemia aparece muy rara vez. La punción accidental de grandes vasos no se asocia con hemorragia seria. El neumotorax aparece en menos del 1% de los pacientes que han sufrido PTB. En nuestra experiencia con un total de 254.punciones durante un periodo 10 de años no hemos tenido ninguna complicación grave.
|
|
|
|
La rentabilidad diagnóstica está determinada principalmente por la accesibilidad. Es obvio que si el broncoscopio no puede alcanzar la lesión no puede establecerse el diagnóstico. En los resultados ofrecidos en la biblioteca existen variaciones que son atribuidas a la selección del paciente, a la localización y tamaño del tumor y a la habilidad del broncoscopista y a la capacidad del que interpreta los extendidos citológicos.
Uno de los prerrequisitos para una exactitud diagnóstica es una adecuada representación celular de la lesión. Esto depende de forma importante de la habilidad del broncoscopista que realiza la PTB. Abundantes referencias bibliográficas y algunos estudios sobre ello (Hapinik 1995, De Castro 1997, Hsu 2004) destacan la importancia de este apartado, el cual exige un tiempo y un número de realizaciones amplio para alcanzar un nivel de experiencia adecuado.
Hay dos factores importantes que juegan un importante papel en la exactitud diagnóstica, son la localización y el tamaño de la lesión. La rentabilidad diagnóstica aumenta de forma significativa para los nódulos mayores de 2 cm. y disminuye para los nódulos mayores de 6 cm, probablemente por la necrosis o inflamación. En el diagnostico de los nódulos periféricos de pulmón, la rentabilidad diagnostica, esta determinada por la accesibilidad y en este sentido es importante la relación entre la vía aérea y la lesión.
En relación con las distintas topografías existe una amplia bibliografía destacando la importancia de que el patólogo se encuentre en el momento de la punción para realizar una valoración rápida, con el fin de reducir el aumento de muestras insatisfactorias. Las muestras negativas con ausencia de linfocitos deben considerarse como insatisfactorios, un número abundante de linfocitos y ausencia de células tumorales indican un verdadero negativo. El diagnóstico citológico ha de hacerse sobre un número suficiente de células malignas. La presencia del escaso número de células tumorales nos obliga a buscar otros elementos de epitelio respiratorio y/o macrófagos pues puede representar contaminación de secreciones bronquiales conteniendo células malignas, esto ha sido causa de falsos positivos (Figura 14).
En nuestra experiencia hemos valorado 254 PTB (218 hombres y 36 mujeres con una edad media de 57.6 años) en nuestro hospital entre Enero de 1994 y Diciembre de 2004 donde la broncoscopia con PTB es realizada rutinariamente en pacientes con linfodenopatías mediastínicas. Los ganglios linfáticos a puncionar son seleccionados en base a su imagen en el escáner (Figura 15). La valoración rápida de la muestra fue hecha en 178 (70%). Se dispuso del diagnóstico final en 171 casos de 187 pacientes con linfadenopatias mediastínicas. La PTB fue diagnóstica en 120 casos (70%) y no diagnostica en 51 casos (30%). De los 171 casos 123 pacientes (72%) tenían procesos malignos y 48 pacientes tenían procesos benignos. De los 123 procesos malignos, 87 pacientes (71%) tenían estudios citológicos positivos. El empleo de la punción transesofágica con ultrasonidos, inicialmente ideada para el diagnóstico de tumores del aparato digestivo, también es de utilidad para alcanzar algunos grupos ganglionares como los subcarinales, los de la ventana aórtico pulmonar y los paraesofágicos de difícil valoración por la PTB. En este apartado nuestra experiencia es limitada ya que disponemos de la técnica desde hace solo un año.
|
|
|
|
La PTB es una técnica sensible altamente específica, minimamente invasiva que tiene su principal papel en el diagnóstico de las lesiones mediastínicas y en al estadiaje del carcinoma pulmón. Un diagnóstico de PTB positivo obvia la necesidad de otros procedimientos diagnósticos más invasivos y costosos. El principal inconveniente es que la practica de la PTB requiere un broncoscopista altamente especializado en la técnica (Haponik 3años, De Castro 50 punciones).
|
|
|
|
1. Baron, KM, Aranda, CP Diagnosis of mediastinal mycobacterial lymphadenopathy by transbronchial needle aspiration. Chest 1991:100,1723-1724
|
|
|
|
- María Magdalena García Bonafé (02/10/2005 13:56:17)
- Rene Millares López (03/10/2005 20:29:38)
- Mario Alejandro Estrada Verdesoto (03/10/2005 23:22:59)
- Dra Teresa Noto Fernandez (05/10/2005 20:35:15)
- Ernesto García Ureta (06/10/2005 12:40:10)
- Ernesto García Ureta (06/10/2005 12:44:37)
- Mercedes Santamaría (07/10/2005 13:33:20)
- Emilio Mayayo Artal (07/10/2005 19:06:14)
- María Magdalena García Bonafé (08/10/2005 9:37:39)
- NATALIA MARTINEZ CASTILLO (09/10/2005 23:31:56)
- ELSIE BEATRIZ PICOTT RANGEL (16/10/2005 10:51:59)
- Ernesto García Ureta (18/10/2005 9:36:53)
- Ernesto García Ureta (18/10/2005 9:43:12)
- Domingo de Agustín Vázquez (25/10/2005 23:30:59)
- Bayardo Flores (02/11/2005 11:40:22)
- Ernesto García Ureta (02/11/2005 20:23:32)
- Maria Laura Haramboure (09/11/2005 18:28:32)
- Ernesto García Ureta (10/11/2005 11:01:47)
|
|
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 15:10:50
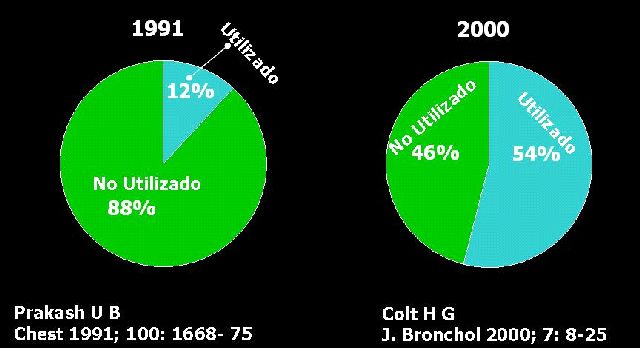 fiogf49gjkf0dFigura 1.">
fiogf49gjkf0dFigura 1.">
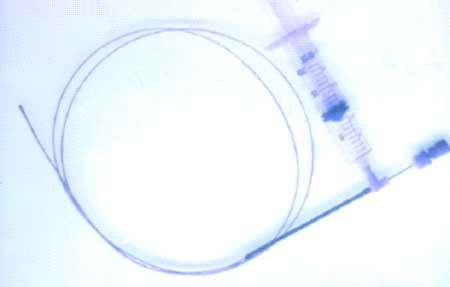 fiogf49gjkf0dFigura 2. El sistema usado es flexible con una longitud de 120 cm con o sin vaina protectora metálica o plástica.">
fiogf49gjkf0dFigura 2. El sistema usado es flexible con una longitud de 120 cm con o sin vaina protectora metálica o plástica.">
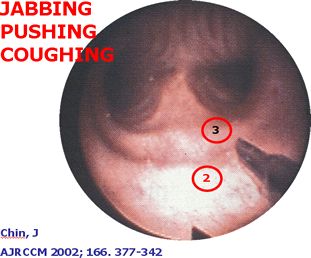 fiogf49gjkf0dFigura 3. PTB. Aguja atravesando la pared bronquial.
Chiin, J
Am J Respir Crit Care Med 2002;166:37
">
fiogf49gjkf0dFigura 3. PTB. Aguja atravesando la pared bronquial.
Chiin, J
Am J Respir Crit Care Med 2002;166:37
">
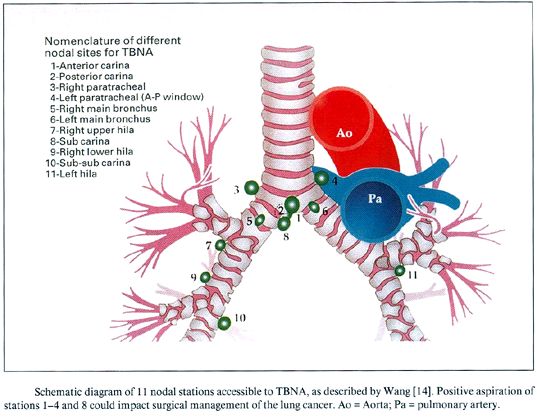 fiogf49gjkf0dFigura 4. Con el fin de estandarizar la técnica y la nomenclatura de la PTB Wang, propuso este esquema en el que se identifican las 11 estaciones ganglionares que también son los lugares más comunes de afectación por metástasis tumorales.">
fiogf49gjkf0dFigura 4. Con el fin de estandarizar la técnica y la nomenclatura de la PTB Wang, propuso este esquema en el que se identifican las 11 estaciones ganglionares que también son los lugares más comunes de afectación por metástasis tumorales.">
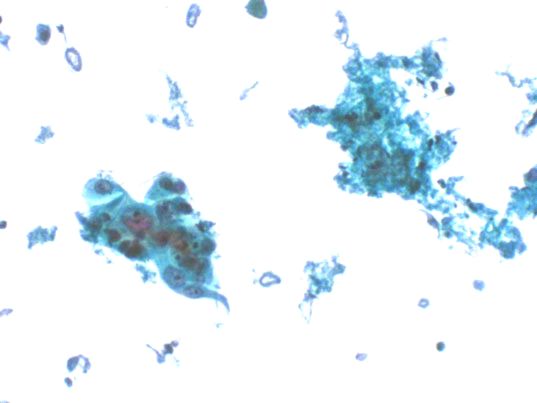 fiogf49gjkf0dFigura 5. Células de un carcinoma epidermoide entremezcladas con restos necróticos.">
fiogf49gjkf0dFigura 5. Células de un carcinoma epidermoide entremezcladas con restos necróticos.">
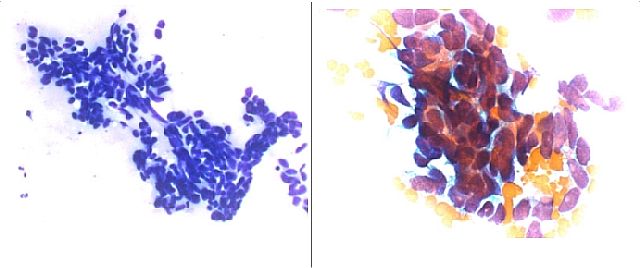 fiogf49gjkf0dFiguras 6 y 7. Grupos de Celulas pequeñas correspondientes a un carcinoide.">
fiogf49gjkf0dFiguras 6 y 7. Grupos de Celulas pequeñas correspondientes a un carcinoide.">
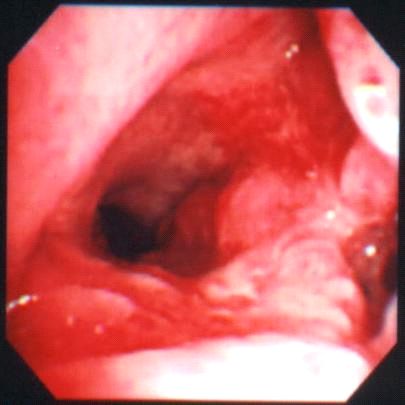 fiogf49gjkf0dFigura 8. Vía aérea con presencia de una lesión submucosa.">
fiogf49gjkf0dFigura 8. Vía aérea con presencia de una lesión submucosa.">
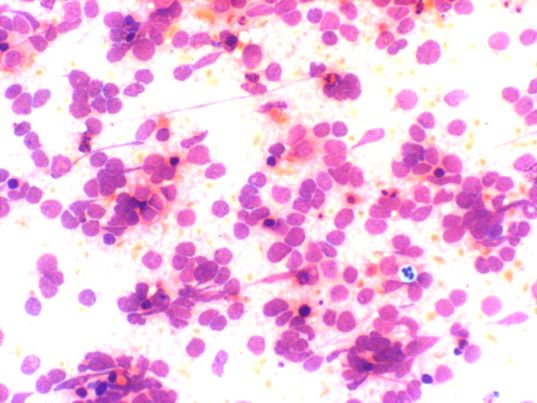 fiogf49gjkf0dFigura 9. Clásica dispersión celular en un linfoma.">
fiogf49gjkf0dFigura 9. Clásica dispersión celular en un linfoma.">
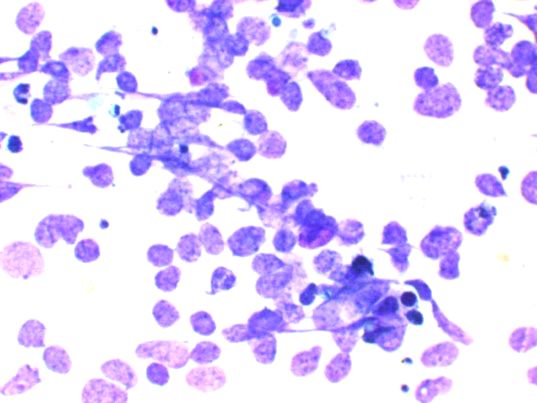 fiogf49gjkf0dFigura 10. Elementos linfoides con marcadas atipias.">
fiogf49gjkf0dFigura 10. Elementos linfoides con marcadas atipias.">
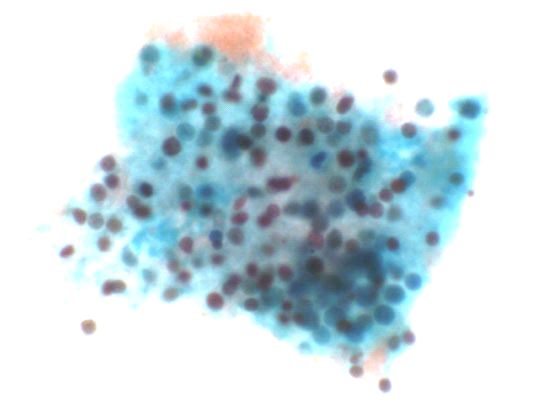 fiogf49gjkf0dFigura 11. Celularidad correspondiente a metástasis por un oat-cell. (Papanicolaou)">
fiogf49gjkf0dFigura 11. Celularidad correspondiente a metástasis por un oat-cell. (Papanicolaou)">
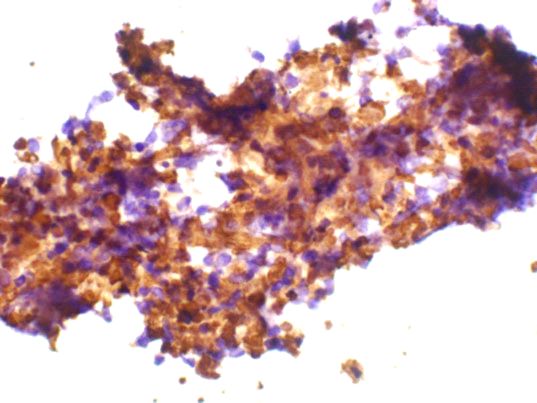 fiogf49gjkf0dFigura 12. Celularidad correspondiente a metástasis por un oat-cell. (Cromogranina)">
fiogf49gjkf0dFigura 12. Celularidad correspondiente a metástasis por un oat-cell. (Cromogranina)">
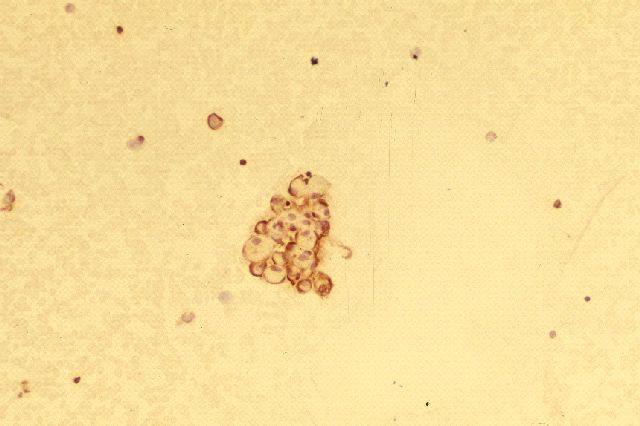 fiogf49gjkf0dFigura 13. Metástasis de un Carcinoma Renal. (Vimentina)">
fiogf49gjkf0dFigura 13. Metástasis de un Carcinoma Renal. (Vimentina)">
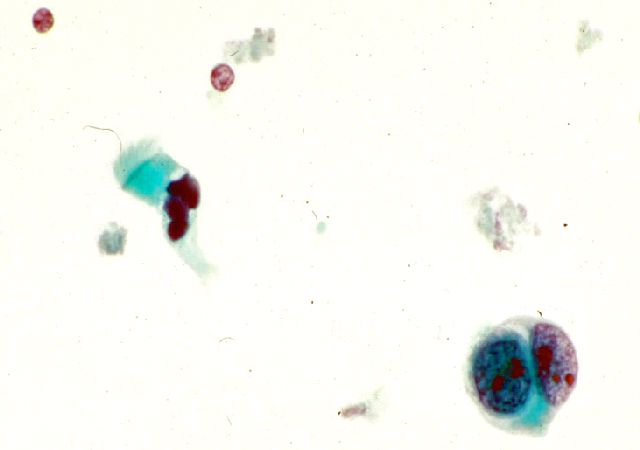 fiogf49gjkf0dFigura 14. Elementos de epitelio respiratorio contaminando una PTB de un adenocarcinoma.
Cropp AJ
Chest 1984; 85: 696-7
Schenk K
Am Rev Respir Dis 1986;134: 377-342">
fiogf49gjkf0dFigura 14. Elementos de epitelio respiratorio contaminando una PTB de un adenocarcinoma.
Cropp AJ
Chest 1984; 85: 696-7
Schenk K
Am Rev Respir Dis 1986;134: 377-342">
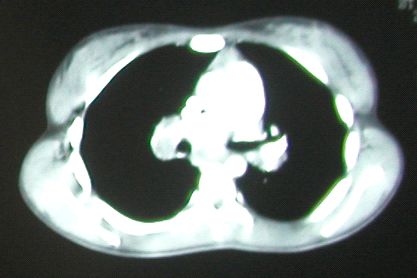 fiogf49gjkf0dFigura 15. Imagen correspondiente a adenopatías hiliares.">
fiogf49gjkf0dFigura 15. Imagen correspondiente a adenopatías hiliares.">
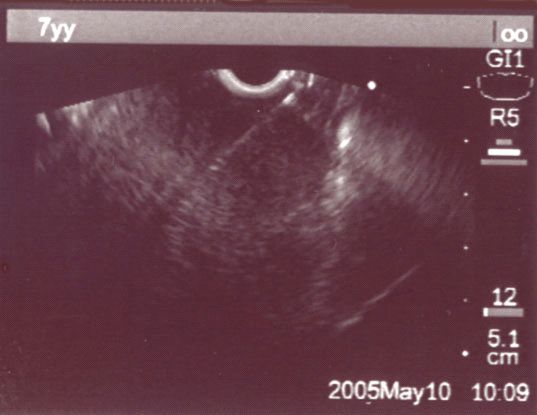 fiogf49gjkf0dFigura 16. Punción transesofágica de una masa mediastinoscopia guiada por ultrasonidos.">
fiogf49gjkf0dFigura 16. Punción transesofágica de una masa mediastinoscopia guiada por ultrasonidos.">