
 Comunciación libre
Comunciación libre
|
Dra. Nancy Rios Hidalgo*, Dra Mercedes Segui Sanchez**, Dr Rodolfo Millan Batista***, Dr Jose Soler Franco****, Estudiante. Juan Manuel Vinardel Lorenzo*****, Estudiante. Euclides Ricardo Feria****** |
|
|
Se efectúa un estudio de serie de casos de pacientes a los cuales se les había realizado biopsia yeyunal en el Hospital Provincial Pediátrico "Octavio de la Concepción y de la Pedraja" de Holguín en el año 2002 con el diagnóstico clínico de casos intolerantes al glúten y con alta probabilidad de ser portadores de una enfermedad celíaca. Se seleccionan al azar mediante el diagnóstico cualitativo 10 biopsias consideradas patológicas y 10 biopsias consideradas como normales, a todas se les calcula mediante el sistema morfométrico: Computer Assited Morphostereologic System Using Digital Image (COMSDI-PLUS) la altura y ancho de las vellosidades intestinales, la profundidad de las criptas intestinales, el conteo de linfocitos intraepiteliales en las vellosidades y el conteo de las mitosis existentes en las criptas. En las biopsias patológicas se encontraron: la menor altura de las vellosidades, la mayor profundidad de las criptas intestinales, la mayor cantidad de linfocitos intraepiteliales y de mitosis en las criptas, las tres primeras variables con diferencia altamente significativa al compararlas con las biopsias normales y la última con diferencia significativa.
email: nancy@cristal.hlg.sld.cu
|
||
|
|
La enfermedad celíaca es un trastorno autoinmune caracterizado por una enteropatía de respuesta mediata del intestino delgado que ocurre en individuos genéticamente predispuestos, quienes al ingerir prolaminas (componentes protéicos insolubles en agua y solubles en alcohol, ricos en glutamina: gliadina o glúten y prolinas) que se encuentran en el trigo, centeno y cebada desarrollan la enfermedad.(1,2,3 )
Aunque los rasgos genéticos de la enfermedad son variables, parece que un heterodímero alfa/beta HLA.DQ específico es el que confiere la susceptibilidad, mediante su interacción con la glutamina (gliadina o glúten). Entre el 90% y 95% de los pacientes expresan el antígeno de histocompatibilidad DQ.W2, sobre todo el heterodímero DQ alfa/beta en el cromosoma 6, además es bien conocida la agrupación familiar de los casos.(2 )
Una interesante hipótesis defiende una reactividad cruzada del glúten con un fragmento de la proteína E1B del adenovirus tipo 12, lo que plantea la posibilidad de que la enfermedad celíaca sea debida, al menos en parte, a la exposición ambiental a este virus.(2 )
Esta enfermedad ha sido descrita en Europa, Rusia, países del Mediterráneo, América del Norte, Sudáfrica, India, Australia, Nueva Zelandia, es rara en países del Africa negra y en nativos de China y Japón.(1,3 )
La prevalencia es actualmente variable, alcanzando desde 1:100 individuos en Europa (su más alta frecuencia) hasta 1:10 000 en otros países.
En Holguín se efectuó en el 2001 un estudio de pesquisaje a los intolerantes al glúten y se detectó una prevalencia de 1 por cada 1000 habitantes.(4 )
En el diagnóstico de la enfermedad se utilizan los test serológicos para medir los anticuerpos antigliadina (AGA), antireticulina (ARA), antiendomisio (EMA) y antitransglutaminasa tisular (tTG), los cuales son de inmenso valor para comprender la enfermedad, para valorar su evolución y monitorear la respuesta al tratamiento, además que al surgir en los años sesenta los mismos se utilizaban para identificar los individuos que necesitaban biopsia yeyunal.(1,2,3,5,6,7,8,9,10,11,12,,13,14,15)
La meta actual es desarrollar test serológicos que sustituyan la biopsia yeyunal como diagnóstico definitivo, la cual es el medio utilizado actualmente para la toma de decisiones con la enfermedad, ya que con la misma se aprecian los cambios ocurridos en la mucosa del intestino delgado producidos por la enteropatía entre los cuales están:
1. Atrofia parcial o total de vellosidades intestinales.
2. Elongación de las criptas.
3. Incremento del índice mitótico de las criptas.
4. Incremento en el número de los linfocitos intraepiteliales.
5. Infiltración de linfocitos, células plasmáticas, mastocitos y eosinófilos en la lámina propia.
6. Pérdida de la polaridad nuclear con seudoestratificación de las células epiteliales.
7. Ausencia del borde en cepillo y anomalías de las células epiteliales( )
Los cambios son progresivos con infiltración inicial de linfocitos intraepiteliales, seguido de hiperplasia de las criptas y finalmente atrofia de las vellosidades. El diagnóstico resulta evidente cuando ya están establecidos los dos últimos cambios histológicos, pero resulta difícil cuando solo está presente el número de linfocitos en las vellosidades.(2,16,17 ) Al observar la biopsia el patólogo normalmente lo hace a través de los métodos cualitativos donde se ve obligado al conteo de las células y al cálculo subjetivo de la altura, ancho de las vellosidades y profundidad de la criptas intestinales, lo que por supuesto puede llevar en ocasiones a diagnósticos inadecuados por exceso o por defecto de una patología que evidentemente necesita de cuantificación.
Teniendo en cuenta la existencia en el campo de la microscopía de la estereología y la morfometría por las cuales a través de la imagen plana de microscopio y de diversos tipos de testajes, técnicas y fórmulas matemáticas, se obtiene indicadores de estructuras tridimensionales a nivel de los tejidos que permiten evaluar una biopsia de forma cuantitativa y por lo tanto llegar a un diagnóstico más certero y completo de la misma(18,19,20,21) y conociendo y utilizando en nuestra institución estos procederse desde hace casi 20 años es que consideramos podría ser de mucha utilidad el estudio morfométrico de las biopsias yeyunales lo que permitiría un diagnóstico más exacto del grado de afectación de la mucosa intestinal, del pronóstico y evolución de los pacientes, por ello es que planteamos la realización de este trabajo investigativo.
|
|
|
|
El presente trabajo es un estudio de serie de casos de pacientes a los cuales se les realizó biopsia yeyunal en el Hospital Provincial Docente Octavio de la Concepción y la Pedraja en el año 2002 con el diagnóstico clínico de casos intolerantes al gúten y con alta probabilida de de ser portadores de una Enfermedad Celíaca. En un universo de 76 biopsias yeyunales, se diagnosticaron en el servicio de Anatomía Patológica de dicho hospital 32 casos patológicos mediante diagnóstico cualitativo y el resto (44) independientemente de algunas alteraciones histológicas fueron concluidos como casos normales desde el punto de vista cualitativo. Nuestra muestra tomada al azar de 10 casos del grupo considerado patológico y 10 casos del grupo considerado normal. Se excluyeron de esta investigación las biopsias que tuvieran menos de 10 vellosidades intestinales. Todas las muestra habían sido procesadas por la técnica clásica de parafina y coloreadas con H y E bajo control del ph para efectuar el diagnóstico cualitativo. Se observaron las preparaciones histológicas, escogiendo en cada una 10 vellosidades intestinales y relizándose tantas mesuraciones como la imagen lo permitió con un sistema morfométrico denominado Computer Assisted Morphostereologic System Using Digital Image (COMSDI-PLUS) diseñado en nuestra institución y soportado por una microcomputadora IBM (USA, 1988) con tarjeta digitalizadora Eye Grabe(USA, 1990) acoplada a un monitor multisincrónico Emerson (SubCorea, 1990) que recoge las imágenes a través de un microscopio Olymphus (Japón, 1985) con cámara de televisión Koyo (Japón, 1990) se procedió a realizar las siguientes opciones apoyadas con un mouse Genius (Taiwán, 1990):
Se determinó el valor promedio, la desviación estándar, el valor máximo y mínimo, varianza, error estándar de la media, coeficiente de variación y test de diferencias entre medias para los indicadores estudiados. Este procesamiento se llevó a efecto con ayuda del paquete estadístico SYSTAT versión 3.0 (España, 1986) y el Med Calc versión 4.16g (Bélgica, 1997)en un microprocesador marca IBM de 640 kb de memoria. Los resultados se muestran en cuadros.
|
|
|
|
CUADRO 1. Altura de las vellosidades intestinales. Biopsias yeyunales normales y patológicas. BIOPSIAS NORMALES BIOPSIAS PATOLOGICAS No. De vellosidades 100 100 Fuente: Datos del autor.
CUADRO 2. TEST DE DIFERENCIA ENTRE MEDIAS. DIF = 31.926 Fuente : Cuadro 1 CUADRO 3. Ancho de las vellosidades intestinales. Biopsias yeyunales y patológicas. BIOPSIAS NORMALES BIOPSIAS PATOLOGICAS
No. De vellosidades 100 100 Fuente: Datos del autor. CUADRO 4. TEST DE DIFERENCIA ENTRE MEDIAS DIF 0.039 Fuente: Cuadro 3 CUADRO 5. Profundidad de las criptas intestinales. Biopsias yeyunales y patológicas. No. De vellosidades 100 100 Fuente: Datos del autor. CUADRO 6. TEST DE DIFERENCIA ENTRE MEDIAS DIF 6.091 Fuente: Cuadro 5 CUADRO 7. Conteo de linfocitos intra epiteliales en las vellosidades intestinales. Biopsias yeyunales normales y patológicas. BIOPSIAS NORMALES BIOPSIAS PATOLOGICAS No. De vellosidades 100 100 Fuente: Datos del autor. CUADRO 8. TEST DE DIFERENCIA ENTRE MEDIAS DIF 23.8 Fuente: Cuadro 7 CUADRO 9. Conteo de mitosis a nivel de las criptas intestinales. Biopsias yeyunales normales y patológicas. BIOPSIAS NORMALES BIOPSIAS PATOLOGICAS No. De vellosidades 100 100 Fuente: Datos del autor. CUADRO 10. TEST DE DIFERENCIA ENTRE MEDIAS DIF 0.28 Fuente: Cuadro 9
DIAGNÓSTICO AAE VARIABLES CUANTITATIVAS Leyenda: a : ancho vellosidades intestinales Fuente: datos del autor
|
|
|
|
Análisis y Discusión de los resultados En nuestro estudio se observaron los siguientes resultados: En el cuadro no.1 se puede apreciar que la altura de las vellosidades intestinales en las biopsias normales muestra un media de 51.795 con un desviación estándar de 19.767 y un coeficiente de variación de 38.164, en las biopsias patológicas la media fue de 19.869 con una desviación estándar de 17.760 y un coeficiente de variación de 89.388, esto último indica que la mayor variabilidad del indicador se obtuvo en este último grupo de casos. Al realizar el test de diferencias entre medias (cuadro no.2) se observa que con un intervalo de confianza de 95% para un valor de t de 12.014 el valor p fue de 0.001 lo que demuestra que la diferencia fue altamente significativa. En el cuadro no.3 se puede observar que el ancho de las vellosidades en las biopsias normales muestra una media de 28.468, con una desviación estándar de 7.6882 y un coeficiente de variación de 27.007, en las biopsias patológicas la media fue de 26.429, con una desviación estándar de 12.125 y un coeficiente de variación de 45.879, también en este grupo se obtuvo la mayor variabilidad del indicador. La mayor media se encuentra en las biopsias normales (28.468) pero es muy ligera la variación con las biopsias patológicas (26.42) aunque se plantea que las vellosidades cuando disminuyen de tamaño se ensanchan en nuestro caso se encontró lo contrario, pero al aplicar el test de diferencias entre medias con un intervalo de confianza de 95% para un valor de t de 0.027,se obtuvo una p de 0.97 lo que demuestra que la diferencia entre nuestros resultados no tiene significación estadística (cuadro no.4) En el cuadro no.5 mostramos los resultados de la profundidad de las criptas intestinales donde en las biopsias normales se encontró una media de 15.079, con una desviación estándar de 11.640 y un coeficiente de variación de 77.195 (en estos casos se obtuvo la mayor variabilidad del indicador) en las biopsias patológicas se obtuvo una media de 21.170, con una desviación estándar de 9.32 y un coeficiente de variación de 44.024. La mayor media se encuentra en las biopsias patológicas (21.170) lo cual está en correspondencia con la mayor profundidad de las criptas de las vellosidades en estos casos, ya que al ocurrir el aplanamiento o atrofia de las vellosidades, las criptas se alargan, se hiperplasian y se hacen tortuosas y es lo que hace que el grosor global de la mucosa intestinal siga siendo el mismo independientemente de la atrofia ocurrida (2 ). Al realizar el test de diferencias entre medias con un intervalo de confianza de un 95% para un t de 4.085, se obtuvo una p de 0.001, por lo que la diferencia en nuestros casos fue altamente significativa (cuadro no.6). En el cuadro no.7 se puede observar que la cantidad de linfocitos intraepiteliales a nivel de las vellosidades intestinales mostró en las biopsias normales una media de 12.300 con una desviación estándar de 13.699 y un coeficiente de variación de 37.947, lo que indica que en este grupo se obtuvo la mayor variabilidad del indicador. En el cuadro no.8 mostramos los resultados del test de diferencia entre medias donde con un intervalo de confianza del 95%, para un valor de t de 17.131, la p que se obtuvo fue de 0.001 lo que demuestra que la diferencia fue altamente significativa. En el cuadro no.9 se observan los resultados del conteo de las mitosis a nivel de las criptas intestinales y así se encuentra que en las biopsias normales la media fue de 1.01, con una desviación estándar de 0.5292 y un coeficiente de variación de 52.915. En el caso de las biopsias patológicas se encontró una media de 1.28, con una desviación estándar de 0.8337 y un coeficiente de variación de 65.135, lo que indica que en este grupo se obtuvo la mayor variabilidad. Se plantea por varios autores que siempre que se encuentren más de 12 mitosis por cripta se hablará de hiperplasia de las mismas , en nuestros casos dadas las escasas diferencias entre los valores y las escasas mitosis en ambos grupos no pensábamos que tenían importancia nuestros datos, pero al aplicar el teste de diferencias entre medias con un intervalo de confianza del 95% para una t de 2.836 se obtuvo una p de 0.005 por lo que se pueden considerar como significativas las diferencias (cuadro no.10). Quisiéramos además comparar de forma individual los diagnósticos cuali y cuantitativos en los 10 casos considerados patológicos y encontramos algunos detalles que vale la pena reflexionar: El caso en que se planteaba una atrofia total de vellosidades fue en el que encontramos la mayor profundidad de las criptas y la mayor cantidad de linfocitos intraepiteliales. También como detalle interesante deseamos añadir que aunque en el hospital Pediátrico no existen test serológicos que pueden ser aplicados al 100% de los casos que se estudian por la intolerancia al glúten, existió la posibilidad en el año 2001 de aplicarles el test para medir la presencia de anticuerpos antiendomisio a algunos de los pacientes en estudio y así encontramos que los 3 casos que dieron positivos a la prueba (2 de ellos hermanos) fueron diagnosticados cualitativamente como atrofia parcial moderada (2) y atrofia parcial ligera (1). Al analizarlos desde el punto de vista cuantitativo uno de ellos fue el caso de menor altura en las vellosidades y los 3 tuvieron más de 20 linfocitos por cada 100 células epiteliales (30; 36; 30, respectivamente). En general para concluir debemos señalar que los 10 casos patológicos están siendo tratados con una dieta exenta de glúten y que varios de ellos ya presentan una respuesta favorable, algunos de los diagnosticados como normales también reciben este tipo de tratamiento y todos los que reciben tratamiento se consideran como intolerantes al glúten, no será hasta dentro de 1 año que sean revaluados que se diagnostiquen como Enfermedad Celíaca o no.
|
|
|
|
1. La menor altura de vellosidades intestinales se muestra en las biopsias patológicas y existieron diferencias altamente significativas al comparar las medias con las biopsias normales.
2. El mayor ancho de las vellosidades intestinales se obtuvo en las biopsias normales pero no existieron diferencias significativas al compararlas con las biopsias patológicas.
3. La mayor profundidad de las criptas se muestra en las biopsias patológicas y existieron diferencias altamente significativas al comparar las medias con las biopsias normales.
4. La mayor cantidad de linfocitos intraepiteliales se observa en las vellosidades intestinales de las biopsias patológicas y se encontraron diferencias altamente significativas al comparar las medias con las biopsias normales.
|
|
|
|
A las autoridades del Hospital Provincial Docente "Octavio de la
Concepción y de la Pedraja" de Holguín por habermos permitido utilizar
las biopsias yeyunales seleccionadas de su Departamento de Anatomía
Patológica necesarias para realizar nuestro trabajo. A los dos estudiantes de Medicina que participaron en la medición de varias de las biopsias y que hoy son médicos graduados.
|
|
|
|
1 - Working Group on Celiac Disease: Revised criteria for diagnosis of coeliac disease. Arch. Dis Child. 60: 816, 2000.
2 - Crawford J,M. El tracto gastrointestinal /RS Cotran, V Kimar, SL Robins EN SU Patología Estructural y Funcional. 6 ed . España: Mc graw Hill-Interamericana, 2000, p. 836-838, 847-848
3 - Working Group of European Society of Paediatric gastroenterology and Nutrition: Revised criteria for diagnosis of coeliac disease. Arch. Dis. Chilsd. 65: 909, 1990.
4 - Soler J. Pesquizaje de los casos intolerantes al glúten en el municipio Holguín. 2000. Trabajo presentado en el 1er Taller Nacional de Enfermedad Celíaca. Holguín, Enero 2001.
5 - Kotze L M, Utivam S R, Nishara R M, Zeni M P, Amarante h m. Antiendomysium antibodies in brazilian patients with celiac disease and their first degree relatives. Arq Gastroenterol. 38(2): 49-103; apr-jun, 2001.
6 - Pecsi G. Genetic association and inmunopathogenesis of coeliac disease. Acta Physiol Hung. 87(4): 339-53, 2001.
7 - Bahia M, Rabello A, Brasileiro Filho g, Penna F J. Serum antigliadina antibody levels as a screening criiterion before jejunal biopsy indication for celiac disease in a developing country. Braz. J. Med. Biol. Res. 34(11): 1415-20; nov, 2001.
8 - Farrace M G, Picarelli A, Di Tola M, Sabbatella L, Marchione O P, Ippolito G, Piacen tini M. Presence of antibodies inflamatory intestinal disease an apoptosis-associated event?. Cell death Differ. 8 (7): 767-70; jul, 2001
9 - Turner L, Hasanglu A, Aybay C. Endomysium antibodies in the diagnosis of celiac disease in short children with no gastrointestinal symptoms. Pediatr Int. 43 (1) 71-3; feb, 2001.
10 - Picarelli A, Sabbatella L, Di Tola M, Gabrielli F, Greco R, Di Cello T, Mastracchio A, Anama M C. Celiac disease diagnosis in misdiagnosed children. Pediatr Res. 48 (5): 590-2; nov, 2000.
11 -Agreus L, Svardsudd K, Tibblin G, Lavo B. Endomysium antibodies are superior to gliadin antibodies in screening for coeliac disease in patients presenting supposed functional gastrointestinal symtoms. Scand J. Prim Health Carc 18 (8):105; jun, 2000.
12 - Reeves G E, Burns C, Hall S T, Gleeson M, Lemmertt K, Clancy R L. The measurement of IgA and IgG transglutaminase antibodies in celiac disease: a comparison with current diagnostic methods. Pathologyy . 32 (3): 181-5; aug, 2000.
13 - Shuppau D. Current concepts of celiac disease pathogenesis. Gastroenterolgy. 119 (1): 234-42: jul, 2000.
14 - Volta V. Celiac disease. Recent findings on its pathogenesis, diagnosis and clinical presentation. Recenti. Prog. Med. 90 (1); 37-44; jan, 2000.
15 - Arencibia M, Castañeda Guillot C, Fragoso Arbelo T, Armas A de, Blanco Rabassa E. Ensayo inmunoenzimático para determinar anticuerpos antigliadina en pacientes Celíacos. Rev. Cub. Pediatr. 64 (1): 38-42, 1999.
16 - Patey- Mariaud D, Serre N, Verkarre V, Celtier C, Cerf-Bennnsussan N, Schmitz J, Brousse N. Etiological diagnosis of villous atrophy.Ann Pathol. 21(4): 319; aug, 2001.
17 - Bagdi E, Diss T C, Munson P, Isaacson P G. Mucosal intraepitelial lymphocytes in enteropathy associated T-cell lymphoma, ulcerative jejunitis and refractory celiac disease constitute a neoplastic population. Blood. 1; 94(1): 260-4; jul, 1999.
18 - Cruz Orive L M, Wetbel E R. Recente stereological methods for cells biology: A brief survey. Am J Physiol 258: 148-156, 1990.
19 - Marcussen N. the double disector: unbiased stereological estimation of the number of particles inside other particles. J. Mic 165 (3): 417-426, 1992.
20 - Gundersen H J G et col. Some new, simple and efficient stereologycal methods and their use in pathologycal research and diagnosis. Acta Pathol Microbiol Inmunol Scabd 96: 379.394, 1988.
21 - Schwartzkopff B et col. Morphometric investigation of human miocardium in arterial hypertension and valvular aortic atenosis. Eur Hearet J 13: 17-23, 1992.
22 - Junqueira L C. Sistema digestivo/ L C Junqueira, J Carneiro. EN SU Histología Básica. 3 ed.(reimp). Barcelona, España: Ed Salvat, 1988.
23 - Ham A W . Intestino delgado y grueso/ A W Ham EN SU tratado de Histología. 8ed. México: Ed. Interamericana, 1983.
24 - Gra Oramas B. Curso nacional actualización patología gastrointestinal. Instituto de Gastroenterología. La Habana. 2000.
|
|
|
|
||
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 15:10:50
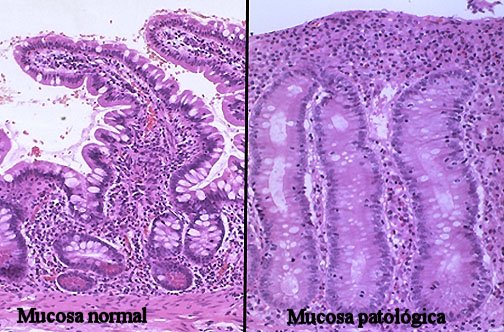 fiogf49gjkf0dComparación de la mucosa intestinal normal y patológica">
fiogf49gjkf0dComparación de la mucosa intestinal normal y patológica">