MATERIAL Y MÉTODOS Pacientes En el estudio se incluyeron 20 pacientes con endometriosis sometidas a laparoscopia o laparotomía. Las muestras de los diferentes tejidos fueron fijadas por inmersión en formaldehído al 10% y posteriormente incluidas en parafina.
Inmunohistoquímica A partir de los bloques de parafina se obtuvieron cortes de 8 mm de espesor. Las secciones, una vez desparafinadas y rehidratadas, fueron tratadas con peróxido de hidrógeno al 0.3% en metanol durante 30 min para bloquear la peroxidasa endógena. Posteriormente las secciones fueron incubadas con anticuerpo monoclonal anti-aromatasa procedente de ratón (DPC Biermann, Germany) a una dilución 1/50 durante toda la noche a 4ºC. Como anticuerpo secundario se utilizó una inmunoglobulina anti-ratón obtenida en cabra (Vector Laboratories, CA) que fue incubado 45 min a Tª ambiente. Por último, las secciones fueron incubadas con el complejo avidina-biotina-peroxidasa (Vector) durante 45 min a Tª ambiente. La reacción fue revelada con una solución de 40 ml de Tris que contenía 5 mg de diaminobencidina (DAB) (Sigma, St Louis, USA) y 10 ml de peróxido de hidrógeno (0.03%). El contraste nuclear se consiguió con hematoxilina de Harris.
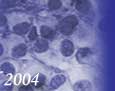
RESULTADOS En ninguna de las secciones de tejido peritoneal y endometrio eutópico de las pacientes analizadas se detectó la presencia de la enzima P450 aromatasa. Seis de las pacientes presentaron leiomiomas, en los que tampoco se observó la expresión de dicha enzima (imágenes no mostradas). El tejido endometriósico (endometriomas) del 60% de las pacientes fue positivo para la expresión de aromatasa, localizada principalmente en la zona fibrótica de la lesión y no en la endometrial. Algunos de estos casos se representan en la
Fig_1,
Fig_2 y
Fig_3.
DISCUSIÓN Y CONCLUSIÓN El desarrollo y crecimiento del tejido endometriósico tiene carácter estrógeno-dependiente, por lo que frecuentemente las pacientes con endometriosis son sometidas a terapia de supresión hormonal con análogos de GnRH. Al eliminar la producción de estrógenos por el ovario, las lesiones endometriósicas se inactivan y atrofian pero, tras el cese del tratamiento, la sintomatología asociada a la enfermedad vuelve a aparecer en un 75% de las mujeres tratadas (
6).
Varios estudios han descrito, mediante inmunohistoquímica y RT-PCR, la presencia de P450 aromatasa en las células glandulares de tejido endometriósico y adenomiótico, y en el endometrio eutópico de pacientes con endometriosis, adenomiosis o leiomiomas, en ambas fases del ciclo. Sin embargo, la enzima no es detectada en biopsias endometriales de mujeres sanas (
5,
7,
8). En nuestro estudio no se detectó aromatasa en el endometrio eutópico de las pacientes analizadas y tampoco en las muestras procedentes de leiomiomas. El tejido peritoneal aparentemente sano también fue negativo en la expresión de dicha enzima (
5). En el tejido endometriósico del 60% de las pacientes incluidas en nuestro estudio se detectó la presencia de aromatasa, localizada principalmente en la pared del quiste y no en la zona endometrial. Dos de estos casos positivos para aromatasa presentaron leiomiomas.
La existencia de actividad aromatasa en los implantes endometriósicos sugiere la idea de que existe una producción local de estrógenos a nivel de la lesión que, junto al aumento de receptores hormonales en dicho tejido (
9), contribuye al desarrollo y mantenimiento de la enfermedad, independientemente de los niveles de estrógenos circulantes. Este hecho puede justificar que el tratamiento con supresores hormonales no es suficiente para eliminar el tejido endometriósico. Por ello, la enzima aromatasa puede considerarse una potencial diana en la búsqueda de nuevas terapias frente a la enfermedad y proponemos como tratamiento eficaz el bloqueo de la actividad aromatasa mediante inhibidores de esta enzima, combinado con tratamiento de supresión hormonal.