ÍNDICE
Paaf de mama: Introducción
Categorías diagnósticas del frotis de la PAAF de
mama
Entidades diagnósticas del frotis de paaf de mama
Problemas diagnósticos en la PAAF de mama
INTRODUCCIÓN
La Punción-Aspiración con aguja fina (PAAF) de mama es un medio diagnóstico
de gran interés dadas la elevada frecuencia de patología mamaria y la importante
tasa de malignidad que esta conlleva, junto a la consideración de método sencillo,
barato y seguro para reconocer dicha patología.
La exposición que vamos a realizar aborda en primer lugar una orientación clínica
del problema, para a continuación ver los criterios diagnósticos en punción
y los problemas más relevantes para el diagnóstico que la propia punción nos
crea.
En una primera aproximación a la técnica, con una perspectiva puramente
clínica, nos debemos preguntar qué podemos esperar del método: ¿qué se
puede o debe pinchar?, ¿cómo, quién y dónde se realiza la prueba? y ¿cuáles
son sus resultados desde el punto de vista práctico?.
Los criterios
que se tienen en cuenta para realizar una PAAF de mama son variados y discutidos
(8). En principio, la punción es necesaria en todos aquellos nódulos palpables
cuyo diagnóstico tiene alguna duda, es muy útil en los quistes (ya que obtiene
un diagnóstico certero y elimina el problema de molestias o dolor) y, además,
puede ser utilizada para tranquilizar definitivamente a la paciente en lesiones,
también palpables, con diagnóstico clínico y/o mamográfico benigno (áreas mastopáticas
y fibroadenomas). Esta última razón, aparentemente más social que médica, está
en franca discusión. Su utilidad también está bien reconocida para el reconocimiento
de posibles recidivas y metástasis.
En las lesiones con diagnóstico cierto de malignidad, y clínicamente inoperables,
se puede hacer PAAF para obtener material con el que realizar un diagnóstico
del tipo tumoral, de la diferenciación nuclear, con o sin morfometría (4), así
como estudios sobre receptores hormonales (de estrógenos y progesterona), índices
de proliferación, colagenasas y sus inhibidores y amplificación de oncogenes,
o contenido nuclear de ADN (citometría de flujo). Todo ello puede ser realizado
con material de punción, incluso con mejores resultados que los obtenidos con
el tejido procesado para histología, al ser menor la manipulación del material,
aunque con las limitaciones que la escasez del material suponen(3,33).
Mucho más discutida es la utilidad de la PAAF en nódulos con un diagnóstico
clínico y/o mamográfico de malignidad, en los que, además, se suele realizar
biopsia peroperatoria. En estos casos se aboga por sustituir el estudio peroperatorio
con la PAAF, lo que no está universalmente aceptado. En cualquier caso, la relación
entre los clínicos y el patólogo suele ser decisiva en el protocolo a seguir.
Sin embargo, para lo que sí puede ser útil la citología (aunque no específicamente
la obtenida por PAAF) en estos casos es para el control peroperatorio de los
bordes quirúrgicos de resección mediante el raspado de los bordes de la pieza
remitida (9).
También puede ser utilizada para el "estudio de extensión" prequirúrgico si
se realiza sobre ganglios axilares, algo que en un futuro puede ser una maniobra
obligada en el protocolo de tratamiento del cáncer de mama (Fig.
1).
En cualquier caso, cada vez es más universal la inclusión de la punción, junto
a la mamografía y la clínica, en un "triple test" necesario para asegurar la
naturaleza de una determinada lesión, de forma que si los tres estudios arrojan
una impresión de malignidad la probabilidad de que el diagnóstico sea correcto
es del 99%, mientras que cuando uno de los tres datos no apoya el diagnóstico,
la certeza diagnóstica baja en un porcentaje importante, y la biopsia puede
llegar a ser necesaria.
Por lo que a la técnica
se refiere, la punción requiere una jeringuilla, una aguja y un "tirador", además
de portas y un fijador. Se puede realizar en la propia consulta. Se utilizan
agujas de 0,6 o 0,8 mm (25-23G) de grosor por 4,5 cm de longitud (obviamente,
de mayor longitud si el tamaño de la mama lo requiere), y jeringuillas de 10
o de 20 c.c. de capacidad. Se debe hacer siempre después de la mamografía, para
evitar "artefactos" en la imagen (aunque esos "artefactos" son discutidos).
La paciente (o el paciente) puede estar sentada, aunque es preferible que se
encuentre en decúbito supino. La punción puede hacerla todo aquel que quiera
y sepa hacerla. Consiste en sujetar la lesión con una mano, pincharla con la
otra, aspirar el embolo de la jeringuilla y realizar pequeños movimientos de
entrada y salida de la aguja en el nódulo sin soltar la aspiración. Finalmente,
soltar suavemente el émbolo para quitar la fuerza de aspiración, sacar la aguja
y expulsar el material obtenido sobre varios portas. El material se extiende,
se fija con alcohol-eter para tinciones con Papanicolaou o se deja secar al
aire para tinciones tipo MGG. La tinción más utilizada es el Papanicolaou, pero
también es muy utilizada la tinción de MGG, o su variante rápida de Diff-Quik.
Esta última se está imponiendo al ser de muy rápida y fácil elaboración, lo
que permite un control casi inmediato sobre la utilidad de la muestra para hacer
un diagnóstico, y con mucha frecuencia el diagnóstico definitivo de la punción
realizada (36). Se puede, e incluso se debe, emplear el control eco o mamográfico
para nódulos de difícil localización y palpación, lo que disminuye el porcentaje
de muestras no útiles. Las lesiones subareolares y la ginecomastia son muy dolorosas,
lo que obliga a un cuidado especial.
Las complicaciones
posibles son hematomas locales, que pueden dificultar estudios radiológicos
posteriores, y muy raros neumotórax en pacientes delgadas con poca mama. Por
otra parte, y como casi en prácticamente cualquier órgano en el que se realizan
PAAFs, está descrita la necrosis de la lesión pinchada, lo que puede dificultar
notablemente el estudio histológico posterior(11).
Los resultados
de la técnica son, en general, muy buenos. No obstante, dependen de muchos factores,
como son el número de pinchazos, el tamaño del tumor, la naturaleza de la lesión
y la experiencia de quien realiza la punción y quien interpreta la muestra.
Por tanto, la variabilidad de los datos que aparecen en la literatura es grande,
y no depende tanto de la técnica en sí como de la población puncionada y de
los criterios de diagnóstico. A modo de resumen, según datos que la Sociedad
Española de Citología (SEC) publicó en 1981(43) la sensibilidad para benignidad
es del 94,43%, para malignidad 93,93%; la especificidad para benignidad 94,37%
y para malignidad 94%, siempre excluyendo las muestras no valorables. Con datos
de la literatura habitual, la precisión diagnóstica general es del 84-96%, obedeciendo
la variabilidad a la inclusión o no de frotis poco o nada valorables y a la
agrupación diagnóstica en diferentes categorías, si bien los resultados son,
en general, satisfactorios(34).
Tanto falsos positivos como falsos negativos llegan al 3%. Los falsos negativos
pueden deberse a errores de muestreo o a errores interpretativos. Provocan errores
interpretativos los cuadros bien diferenciados como son los carcinomas tubular
y lobulillar y las lesiones no infiltrantes; además, las lesiones rodeadas por
una mastopatía, especialmente si esta es florida, pueden presentar un diagnóstico
complicado. Las muestras con insuficiente material suelen proceder de lesiones
difíciles de aspirar por su estructura (carcinoma escirro) o tamaño (a su vez,
el tamaño "pequeño" depende de su comparación con el tamaño de la mama "portadora").
Los falsos positivos se deben a cuadros proliferativos (segunda fase del ciclo,
embarazo - Figs. 2 y 3-, y mastopatías muy floridas), a proliferaciones
papilares, a la atipia provocada por quimio y radioterapia, y a cuadros con
necrosis (abscesos y necrosis grasa). Además, el porcentaje de frotis en los
que hay que hacer reseña de lesión atípica o sospechosa, es cercano al 20%(2,60).
Las muestras insatisfactorias varían mucho, en dependencia de los criterios
para admitir una paciente a punción; con criterios estrictos no debe superar
el 5%(16,54). La punción en el varón admite un mayor porcentaje de muestras
insatisfactorias, ya que la patología más habitual, la ginecomastia, tiene un
importante componente fibroso que dificulta la obtención de material(23).
Así las cosas, cuando una lesión tiene sospecha de malignidad mediante clínica
y/o mamografía, la confirmación con una PAAF se logra en un 60% casos, y con
PAAFs repetidas (hasta lograr un material satisfactorio) en el 90% de las veces.
La realización del bloque celular también mejora los resultados de la simple
extensión citológica(5), si bien a costa de convertir el método sencillo y barato
en algo más complejo. La toma de cilindros-biopsia por punción es más efectiva:
70y 95% respectivamente, pero también más compleja y cara (Figs.
4 y 5). En resumen, la PAAF logra un beneficio evidente, reduciendo de forma
importante el número de pacientes que necesitan una biopsia abierta para confirmar
un diagnóstico, lo que se traduce en una disminución del costo sanitario derivado
del diagnóstico del nódulo de mama. Si además podemos pinchar lesiones no palpables
(21,29) (mediante estereotaxia y/o ecografía sobre focos de microcalcificación),
logramos una precocidad diagnóstica importante. Esto ha permitido que sobre
las piezas quirúrgicas, las lesiones con componente "in situ" pasen del 40%
al 80%. Además, evitamos tener que hacer biopsia abierta sobre todas las pacientes
con focos de microcalcificación, que en más del 75% de casos solo presentan
patología mastopática benigna. Si en una pieza obtenida por estereotaxia se
observa algún grado de atipia epitelial, la toma de biopsia es obligada.
Por último, nos parece importante volver a indicar que no toda punción obtiene
un rendimiento seguro. Uno de los mayores problemas en la práctica diaria de
la PAAF de mama es el alto porcentaje de muestras no útiles para estudio (28).
Los nódulos son difíciles de reconocer e inmovilizar cuando son profundos o
asientan en mamas densas, y, por tanto, difíciles de pinchar con seguridad;
además, es muy frecuente solicitar la punción sobre "áreas" nodulares, cuya
punción "a ciegas" suele ser poco concluyente. Las lesiones fibróticas (tumores
escirros y cuadros esclerosantes) permiten la obtención de muy escaso material.
Por ello no es extraño que en algunas publicaciones se obtengan porcentajes
de muestras inadecuadas tan altos como del 45%, e incluso en grupos con reconocida
experiencia se llegue al 30%. En líneas generales, cuando se es estricto en
los criterios de diagnóstico citológico, el número de muestras insatisfactorias
es alto, y las entidades a diagnosticar resultan limitadas, pero el grado de
certeza que se obtiene cuando una muestra es identificada como maligna es muy
alto, y, al final, el prestigio de la técnica resulta reforzado.
Pero el clínico no sólo debe saber que grado de utilidad representa la PAAF
de mama, también debe estar preparado para conocer las diferentes entidades
diagnósticas que la PAAF de mama permite. En principio, cualquier patología
es susceptible de ser reconocida, pero en la práctica hay ciertas limitaciones,
lo que nos lleva a una segunda parte de esta exposición, más enfocada al patólogo,
y encaminada a exponer los criterios de lectura de un frotis procedente de una
PAAF de mama, y a conocer los diferentes cuadros que podemos reconocer.
CATEGORÍAS
DIAGNÓSTICAS DEL FROTIS DE PAAF DE MAMA:
A la hora de emitir un informe, es fundamental tener unos criterios claros
de lo que se desea conocer: una orientación clínica suficiente para abordar
un determinado problema, o un diagnóstico exacto y lo más completo posible.
Diferentes autores han defendido una u otra postura, y las discusiones continúan(35).
Actualmente, parece haber acuerdo sobre la primera, de forma que se ofrece al
clínico una categoría diagnóstica que implica una postura médica concreta, y
se deja para el estudio sobre la pieza quirúrgica, si la hay, las matizaciones
diagnósticas pertinentes. No obstante, esta norma general se debe saltar cuando
se trata de calificar lesiones inoperables por su estadio clínico, en las que
se debe dar la mayor información posible sobre la lesión; y se puede complementar
con un diagnóstico preciso si la preparación del patólogo lo permite.
A este respecto, se han publicado muchos trabajos que aportan diferentes calificaciones
diagnósticas, aunque sólo algunos de ellos tienen unos subgrupos con la suficiente
utilidad clínica(31,41,51,57). De estos, me permito recomendar el reseñado por
Logrono y cols.(31), que, aunque con matizaciones, tiene amplia aceptación y
parece ser muy útil desde el punto de vista clínico.
I- Frotis
negativo para malignidad. En otras clasificaciones se le denomina simplemente
"benigno". Incluye quistes, abscesos, necrosis grasa, cambios fibroquísticos
sin componente epitelial proliferativo, el fibroadenoma y otros frotis negativos
carentes de especificidad.
Frotis: Poca celularidad en general. Los grupos celulares son
compactos, y con células uniformes de núcleo pequeño sin atipia ni nucléolo.
El fondo suele ser limpio, seroso, con histiocitos, células apocrinas y mioepitelio
(con frecuencia en parejas de núcleos(59)). Naturalmente, los cuadros inflamatorios,
en especial los agudos, tienen otro aspecto que se comentará más adelante (Figs.
6 y 7).
II-
Frotis con células atípicas de significado clínico indeterminado. En
otras clasificaciones tiene denominaciones muy variadas que incluyen "coletillas"
como "con atipia", "con proliferación", "proliferación epitelial con atipia",
"no concluyente",
....
Incluye a los frotis de fibroadenomas muy celulares, papilomas intraductales,
enfermedad fibroquística con cambios proliferativos del epitelio y al adenoma
tubular. Cuando hay una sospecha clínica o radiológica de malignidad, la identificación
de esta categoría de frotis implica la realización de una biopsia. A efectos
de agrupar lesiones para estudios estadísticos, se consideran frotis "benignos".
Es el subgrupo cuya utilización tiene más detractores.
Frotis: Además de los componentes propios de frotis negativo para
malignidad, se observan aislados grupos celulares de morfología muy irregular
o papilar, con elementos que presentan nucléolo, o con cierto amontonamiento
de los núcleos (Fig. 8).
III- Frotis
sospechoso de malignidad. En otras clasificaciones, se le señala como
"sospechoso", "sugerente de malignidad", y también "no concluyente".
Incluye a frotis de enfermedad fibroquística cuyo componente epitelial proliferativo
presenta algún grado de atipia (hiperplasia ductal atípica) y al fibroadenoma
atípico-tumor fillodes. Un frotis incluido en esta categoría requiere siempre
estudio del cuadro mediante biopsia. A efectos de agrupar lesiones para estudios
estadísticos, se consideran frotis "malignos".
Frotis: Grupos con rasgos de malignidad (tridimensionalidad, anisonucleosis,
nucléolos) entre algunas placas de aspecto benigno y/o un fondo con "mioepitelio"
(Fig. 9).
IV- Frotis
positivo. En otras clasificaciones es denominado "maligno". Se incluyen
aquí los frotis con malignidad obvia.
Frotis: Celularidad abundante en grupos irregulares, tridimensionales, con células
que se desprenden de los bordes y elementos sueltos ("disgregación"). En tumores
escirros la celularidad puede ser muy escasa, e incluso proporcionar, repetidamente,
"material insuficiente". Los núcleos son grandes, están amontonados, y presentan
amoldamientos entre ellos. La atipia es variable, pero hay polimorfía y anisonucleosis,
núcleos de cromatina gruesa y nucléolos. Puede haber multinucleaciones y un
número muy variable de mitosis, a veces atípicas. Los citoplasmas están mal
definidos, y a veces son vacuolados; las luces intracitoplasmáticas con secreción
("cuerpos magenta") son mucho más frecuentes en las lesiones malignas, pero
no son exclusivas ni de malignidad ni de patología de mama. El fondo de las
tomas suele ser sucio, serohemorrágico, necrótico o inflamatorio. Normalmente,
no debe haber mioepitelio ni grupos "benignos". Es un rasgo muy fiable de malignidad
la existencia de grupos de estroma adiposo adheridos a grupos con atipia citológica
(Fig. 10).
Además,
se incluye una categoría, de "muestra insatisfactoria" cuando
no hay en el frotis un mínimo de celularidad. Este "mínimo" también está discutido,
y en cualquier caso depende de la lesión a estudiar: para una mastopatía, escasos
histiocitos y un grupo fibroadiposo puede ser suficiente; para un cáncer de
mama dudoso, no. Como norma general, se puede considerar como muestra mínima
seis grupos epiteliales cohesivos, cada uno de ellos con un mínimo de cinco
células ductales (31,52). Evidentemente, es necesario reconsiderar estas limitaciones
cuando se valoran mamas muy fibrosas, nódulos fibroadiposos o la punción de
un quiste, que, lógicamente, no proporcionan, normalmente, los grupos epiteliales
que la norma pretende controlar.
No obstante, todas estas calificaciones diagnósticas genéricas agrupan a una
serie de cuadros cuyo reconocimiento en PAAF suele ser posible y, por tanto,
deben hacerse constar en el informe citológico para proporcionar al clínico
la mayor información posible con el fin de facilitar la decisión terapéutica
más apropiada. A continuación se especifican los rasgos citológicos de las lesiones
mamarias. En general, los cuadros con una cierta frecuencia presentan rasgos
citológicos que han sido suficientemente contrastados, sin embargo, las lesiones
menos habituales sólo contienen algunas referencias bibliográficas que hemos
procurado aportar. A falta de una "citopatología por PAAF basada en la evidencia"
hemos intentado exponer criterios sólidos y referencias fiables que permitan
ayudar en la práctica diaria.
ENTIDADES DIAGNÓSTICAS
DEL FROTIS DE PAAF DE MAMA
Frotis de una mama sin patología (frotis negativo NOS):
- Fondo seroso, azulado, con núcleos pequeños y ovoides de mioepitelio-células
estromales (el verdadero origen de los núcleos desnudos del fondo de los frotis
es discutido, aunque parece que corresponden a ambos tipos celulares: mioepitelio
y fibroblastos del estroma), algún polimorfonuclear neutrófilo y hematíes.
- El epitelio ductal es muy escaso, en grupos-placas de células monocapa, de
núcleos uniformes, con ligera variación del tamaño, redondos u ovoides y pequeños,
sin nucléolo visible. La actividad hormonal determina citoplasmas vacuolados
y núcleos rechazados a la periferia con nucléolo prominente (Fig.
3 y 6).
- En el embarazo hay "cuerpos del calostro": células espumosas con núcleo periférico,
gránulos eosinófilos de proteína y espacios claros correspondientes a gotas
de lípidos (18).
- Ocasionalmente, algún grupo acinar de pequeñas luces con epitelio periférico,
cúbico y uniforme.
- Normalmente grupos de tejido adiposo maduro y rara vez fragmentos de estroma
conectivo, metacromáticos, con células de núcleo alargado (Figs.
7 y 23).
GALACTOCELE
Se produce tras una supresión brusca de la lactancia que determina la formación
de espacios quísticos en los conductos galactóforos, ocupados entonces por un
material lacteo. Puede complicarse con un proceso inflamatorio sobreañadido:
galactoforitis.
Frotis: fondo lactescente con abundantes células espumosas en
diferentes grados de degeneración. El componente inflamatorio depende del estado
de la lesión, pudiendo ser muy rico en polimorfonucleares neutrófilos cuando
se transforma en una galactoforitis (Fig. 11).
GALACTOFORITIS
Es un proceso inflamatorio que afecta a los conductos galactóforos. Puede asentar
sobre un galactocele o no. Cuarsa con fiebre y dolor local.
Frotis: Fondo lactescente con células espumosas, parcialmente
rotas y degeneradas, polimorfonucleares neutrófilos y un moderado número de
linfocitos.
MASTITIS AGUDA
Es un cuadro infrecuente, que normalmente se da durante la lactancia, y que
generalmente es debido al Stafilococo aureus. Si se reconoce su naturaleza,
no se debe pinchar.
Frotis: fondo inflamatorio, con fibrina y restos necróticos, polimorfonucleares
neutrófilos, linfocitos, células plasmáticas, histiocitos y células gigantes,
así como epitelio degenerado que puede presentar rasgos de atipia. Puede haber
material cálcico (Fig. 12).
En el Absceso retroareolar
(32) hay, además, muchas escamas anucleadas y cristales de colesterol (Fig.
13).
Diagnóstico diferencial: carcinomas con necrosis y especialmente el carcinoma
medular, debido al epitelio degenerado y a las agrupaciones de histiocitos.
La historia clínica y el fondo inflamatorio, predominantemente necrótico y agudo,
deben ser de suficiente valor, además las células epiteliales presentan rasgos
degenerativos más que verdadera atipia.. El absceso se diferencia de la galactoforitis
en que en ésta hay menos necrosis y el fondo de las tomas incluye células espumosas.
MASTITIS DE CÉLULAS PLASMÁTICAS
Parece ser una ectasia ductal, con respuesta inflamatoria crónica alrededor
del ducto. Es rara, suele darse en pacientes mayores, multíparas, cursando con
galactorrea intermitente.
Frotis: fondo necrótico con histiocitos en las fases con mucha ectasia;
escasa celularidad, entre la que destacan las células plasmáticas, con epitelio
que puede mostrar mucha atipia, en las fases de estado.
MASTITIS TUBERCULOSA
Es una lesión muy rara en nuestro medio, aunque los trabajos publicados le
dan una incidencia del 1% de los nódulos que se pinchan en los países desarrollados.
La inmunosupresión y las malas condiciones higienicosanitarias aumentan esa
incidencia.
Frotis: grupos de células epitelioides sobre un fondo de polimorfonucleares
neutrófilos y linfocitos. Además, suelen verse células gigantes, pero sólo en
la mitad de los casos hay necrosis. La tinción de Zielh-Neelsen es definitiva
para el diagnóstico cuando demuestra la existencia del bacilo, pero su efectividad
es limitada.
Diagnóstico diferencial: otros procesos inflamatorios granulomatosos, cuya expresión
en PAAF es similar. Sólo la necrosis permite orientar el cuadro hacia un origen
fímico (19).
NECROSIS GRASA
Puede ser de origen traumático, quirúrgico o accidental, aunque en más de la
mitad de los casos falta este dato clínico. Son nódulos dolorosos en su inicio
y duros en la fase cicatricial, ya que el proceso supone un cuadro inflamatorio
con las fases aguda (necrótica) y crónica (de tipo reparativo). La radiología
y la clínica pueden ser sugerentes de malignidad.
Frotis: fondo serohemorrágico con vacuolas ópticamente vacías,
histiocitos espumosos y microvacuolados, cristales de colesterol, polimorfonucleares
y epitelio degenerado, en la fase aguda. Células gigantes y fibroblastos activados,
en la fase de estado, o crónica. En ambas fases hay, además, mioepitelio-células
estromales en el fondo de los frotis (Fig. 14).
Diagnóstico diferencial: Carcinomas con necrosis, en particular
en la fase aguda, pero los histiocitos espumosos y el componente inflamatorio
mixto deben orientar hacia la necrosis grasa.
MASTOPATÍA FIBROQUÍSTICA
Es la patología que con más frecuencia resulta susceptible de punción. Afecta
a un 40% de mujeres entre los 30 y 50 años. Suele ser bilateral y cursa con
clínica de dolor y mamas tensas y multinodulares, con oscilaciones del cuadro
clínico relacionadas con las fases del período menstrual. Histológicamente,
es un cuadro de difícil definición, que agrupa muy diversas y diferentes imágenes
histológicas: fibrosis más o menos densa, quistes con o sin metaplasia apocrina
y ectasia canalicular, algún grado de inflamación y algún grado de hiperplasia
del epitelio ductal (epiteliosis-papilomatosis) o lobulillar (adenosis, adenosis
esclerosante y proliferaciones del mioepitelio). Sólo las proliferaciones del
epitelio están relacionadas con un incremento en la incidencia del cáncer de
mama (aproximadamente, el doble).
Frotis: Es muy habitual el frotis limpio, con "material insuficiente"
por la punción a ciegas sobre un área fibrosa. A veces sólo se obtiene tejido
fibroadiposo en pequeños grupos, o pequeños grupos de epitelio, escaso mioepitelio
(núcleos desnudos oscuros y alargados), y aislados histiocitos-células espumosas.
Pero, además, si se punciona alguno de los cuadros histológicos arriba señalados
podremos ver :
- QUISTE: Tiene tamaños
muy variables, y permiten obtener un líquido en cantidad y aspecto igualmente
variable, normalmente turbio y pardo-verdoso, y lechoso en el galactocele.
Los frotis tienen un fondo seroso con detritus, polimorfonucleares, linfocitos
e histiocitos con citoplasmas oscuros o claros según tengan o no material
fagocitado, así como placas o grupos papilares de epitelio apocrino (límites
citoplasmáticos netos, núcleo redondeado y nucléolo pequeño y marcado) (Fig.
15, 16 y 17). En
el epitelio apocrino no son raras las células multinucleadas con citoplasma
amplio y rosado, procedentes de la pared del quiste, e incluso células con
cierta atipia que no deben ser tenidas como sospechosas. A veces, se ven escasas
y aisladas células ductales, y, ocasionalmente, algún grupo estromal. Los
cristales de colesterol indican un quiste de larga evolución.
La punción de los quistes de mama suele ser agradecida, ya que la paciente
tiene una sensación casi inmediata de solución de su problema, y nosotros
tenemos un diagnóstico fácil. Por contra, no es rara la "recidiva" o la aparición
de nuevos quistes, y habrá que tener especial cuidado en que no se nos pase
por alto un tumor maligno quístico (<1% de cáncer de mama), pinchando de nuevo
si tras "vaciar" el quiste persiste algún nódulo.
- ADENOSIS: pequeños
grupos de disposición acinar, que tienen células pequeñas, uniformes y muy
agrupadas, con pequeño nucléolo (Fig. 18 y 19).
- FIBROADENOMATOSIS: placas como en un fibroadenoma (ver más adelante).
- PAPILOMATOSIS:
placas densas de elementos pequeños y regulares sin atipia, sobre un fondo
albuminoso característico, que corresponde a contenido ductal (Fig.
20).
- HIPERPLASIA DUCTAL:
grupos epiteliales cohesivos con espacios intercelulares irregulares y núcleos
amontonados. Hay leve variabilidad en el tamaño nuclear y cromatina con pequeñas
condensaciones (Fig. 21).
- PROLIFERACIÓN
DUCTAL ATÍPICA: Grupos irregulares, laxos, papilares o cribiformes, con
núcleos hipercromáticos, y elementos sueltos con alta relación núcleo/citoplasma.
El fondo suele tener células mioepiteliales, peros éstas son raras dentro
de los grupos epiteliales (Fig.22).
- MASTOPATÍA FIBROSA
FOCAL: son áreas densas mal definidas que descaman con pequeños grupos
de estroma poco celular entre los que a veces destacan estructuras ductales
o lobulares (42).
FIBROADENOMA (FA)
Es un nódulo bien delimitado, firme, no adherido, normalmente de pequeño tamaño
(alrededor de 3 cm de diámetro). Tiene lugar en un 25% de las mujeres, preferentemente
entre los 20-30 años. Presenta un crecimiento muy irregular y en un 20% de casos
es múltiple.
Frotis: Abundante o moderada celularidad en placas grandes y cohesivas,
de morfología muy variada (en "cuerno de alce"), con mioepitelio en su periferia
y dentro de las placas. El fondo es serofibrinoso, limpio, con los pequeños
núcleos de mioepitelio-estroma desnudos. El epitelio de las placas es muy regular,
con citoplasmas bien delimitados, núcleos redondeados y, a veces, un nucléolo.
Suele haber fragmentos de estroma. No son nada raros los cambios mucinosos o
mixoides en el estroma, y a veces se observan células gigantes multinucleadas
(Fig. 23, 24 y 25).
En las formas juveniles,
ese mismo epitelio aparece más agrupado, con una cierta tridimensionalidad,
pero conservando mioepitelio, junto a mayor componente estromal en grupos laxos.
La celularidad es mayor y puede verse cierta falta de uniformidad celular. Son
lesiones relativamente grandes que se dan en mujeres menores de 20 años.
El Adenoma tubular,
que posiblemente corresponde a una variante de FA pericanalicular, presenta
cierta similitud citológica, aunque tiene grupos redondeados más que placas
epiteliales, y además son grupos más pequeños que las placas del FA típico.
El epitelio puede tener cierta anisonucleosis y nucléolos más llamativos, aunque
predomina la uniformidad. Hay abundante mioepitelio, pero el estroma es muy
escaso, si lo hay (Fig. 26).
En el denominado Fibroadenoma
atípico, la celularidad del frotis es muy abundante, tanto en el componente
estromal como en las placas epiteliales, ambos con celularidad más cohesiva
y cierta atipia nuclear. A veces, incluso se ven mitosis.
Diagnóstico diferencial: El FA está considerado como una de las lesiones
más fáciles de identificar en PAAF, no obstante siempre es necesario descartar
un tumor fillodes, que tiene placas estromales más densas en celularidad, y
no olvidar que un FA puede tener un epitelio muy activo (7,48) capaz de sugerir
un carcinoma (el mioepitelio de fondo y un aspecto general del frotis de FA,
deben resolver la duda). Por el contrario, en las mujeres por encima de los
45 años los frotis sugerentes de FA deben ser cuidadosamente revisados para
evitar falsos negativos.
ADENOMA DEL PEZÓN
Es una lesión nodular, que provoca telorragia, y con frecuencia ulcera el pezón.
Frotis: fondo serohemorrágico, con mioepitelio, células espumosas y apocrinas,y
grupos de epitelio de morfología variada (papilas, mórulas y placas). La celularidad
carece de atipia franca, pero puede presentar núcleos oscuros y a veces nucléolos.
A veces hay metaplasia pavimentosa.
Diagnóstico diferencial: el carcinoma papilar tiene más atipia celular
y carece del mioepitelio del fondo de las tomas, además de que los grupos papilares
presentan un eje fibrovascular destacado. El papiloma intraductal suele tener
un fondo más sucio y mayor componente pavimentoso, pero su diferenciación es
muy difícil,
PAPILOMA INTRADUCTAL
Es una lesión nodular subareolar, grande y única, que suele cursar con telorragia.
La edad media de presentación es de 50 años.
Frotis: fondo serohemorrágico en el que destacan grupos de epitelio ductal
ramificados y cohesivos con la celularidad más marcada en sus bordes, entre
histiocitos, mioepitelio y placas de metaplasia apocrina. El epitelio de los
grupos tiene cromatina fina y nucléolo poco llamativo. A veces hay fondo necrótico,
macrófagos con hemosiderina y epitelio con metaplasia pavimentosa o con rasgos
degenerativos (citoplasmas muy vacuolados) (Fig. 27).
Diagnóstico diferencial: al igual que con la entidad anterior, el carcinoma
papilar tiene más atipia celular y carece del mioepitelio del fondo de las tomas,
además de que los grupos papilares presentan un eje fibrovascular destacado.
La diferenciación con el adenoma del pezón es muy difícil.
CÁNCER DE MAMA
El cáncer de mama tiene una elevada frecuencia en nuestro medio, supone casi
el 20% de todos los cánceres, y en el año 92 fue "responsable" de 30 muertes
por cada 100.000 mujeres en nuestro país. La tasa actual en España es de 30-35
casos nuevos por cada 100.000 mujeres y año. Su incidencia va en aumento, hoy
se calcula que alrededor de 1 de cada 14 mujeres puede padecer la enfermedad,
y para el año 2.000 la proporción será menor. Tiene su pico de incidencia entre
los 45 y 55 años. La mitad de los casos se dan en el cuadrante superoexterno
de la mama, y con frecuencia son bilaterales. Se le conocen relevantes relaciones
genéticas y hormonales, que permiten seleccionar mejor a las pacientes merecedoras
de programas de prevención, en los que la PAAF puede jugar un importante papel.
Con la PAAF podemos lograr tres objetivos: 1- establecer la malignidad, 2- identificar
el tipo histológico, y 3- estudiar factores pronósticos.
Por lo que se refiere al tipo histológico, puede ser muy difícil de establecer,
y es poco relevante si se va a proceder a una resección quirúrgica de la lesión.
Entre los factores pronósticos puede ser muy bien establecido el grado nuclear,
y es posible emplear el material de punción para estudiar factores de proliferación,
grupos genéticos y comportamiento hormonal; datos que normalmente se estudian
en el material de biopsia, más abundante aunque no mejor. La mayor utilidad
se enfoca, por tanto, a establecer el carácter de la lesión, y para ello, la
malignidad del frotis tiene unos criterios establecidos, referidos al
carcinoma ductal infiltrante,
que constituye un 50% de las lesiones de la mama en forma pura, y un 20% como
parte de un tipo histológico mixto (con ca. tubular, lobulillar, mucinoso,...):
- Celularidad abundante, en grupos y en elementos sueltos (Fig.
28).
- Tridimensionalidad en los grupos, con células desprendidas en sus bordes
(Fig. 29).
- Células de talla variable, con bordes angulosos y moldeamientos o verdaderas
figuras de "canibalismo". Aumento en la relación nucleo-citoplasma (Fig.
30).
- Atipia nuclear franca, con anisonucleosis, cromatina gruesa y nucléolos.
Multinucleaciones. Mitosis (Fig. 31).
- Citoplasmas mal definidos, a veces vacuolados.
- Fondo sucio, serohemorrágico, necrótico o inflamatorio. Falta el mioepitelio.
- Grupos de estroma adiposo adherido a grupos tumorales.
- En las formas mixtas, grupos de la porción no ductal.
Además, algunas variantes del carcinoma ductal también se pueden reconocer.
Así, las lesiones con crecimiento comedo
suelen ofrecer grupos irregularmente redondeados con tridimensionalidad, en
cuyo centro se puede ver en polvillo nuclear de la necrosis y cariorrexis (Fig.
32). Los carcinomas ricos
en glípidos muestran una celularidad con citoplasmas amplios y claros y
núcleos rechazados a la periferia de la célula (Fig. 33).
El carcinoma cribiforme
presenta grupos tridimensionales con espacios redondeados vacios en su interior
(6).
En el carcinoma lobulillar
(10% de los cánceres de mama), la celularidad es más pequeña, en conglomerados
densos, "tubos" celulares e hileras. Los núcleos son algo más pequeños y uniformes,
y abundan los núcleos desnudos. Son muy frecuentes las vacuolas intracitoplásmicas
(hay una variante en que casi todas las células presentan vacuola grande PAS+
y núcleo rechazado: carcinoma de células en "anillo de sello"). Las células
en "anillo de sello" sin clara vacuola citoplasmática son más propias de un
carcinoma ductal (24). Puede precisar la diferenciación con la adenosis (núcleos
menos uniformes, en disposición más anular sobre una "luz" central, que a veces
es sólo una hendidura) y con linfomas (sólo se ven elementos sueltos, sin grupos,
de ribete citoplásmico muy delgado y muy azul) (Figs.
34 a 38).
En el carcinoma medular
(1-6%), los conglomerados son más laxos, con abundantes células aisladas. Son
células grandes, muy atípicas, de cromatina gruesa y nucléolo muy llamativo.
El fondo suele tener abundantes linfocitos y células plasmáticas, lo que obliga
a descartar un linfoma (Figs 39 y 40).
El carcinoma coloide
de mama (2,5%), presenta en el fondo de las preparaciones un material metacromático
con MGG y rojo con PAS, entre el que destacan grupos celulares de escasa atipia,
núcleo redondeado y citoplasma amplio y eosinófilo, sólo a veces vacuolado (15).
Quizá su mayor problema diferencial sea descartar lesiones benignas que incluyan
áreas de tipo mucocele, que normalmente presentan frotis en los que el mioepitelio
y otros componentes de la patología benigna acompañante permiten una diferenciación
aceptable (45) (Fig. 41).
El carcinoma papilar,
es una lesión rara (<1%) fácil de sospechar en citología. Tiene abundante celularidad
en conglomerados muy grandes y muy densos, con bordes marcados, en empalizada,
y eje fibrovascular central. La celularidad presenta cromatina gruesa y atipia
leve o moderada. El fondo es muy hemático y hay histiocitos con hemosiderina,
además, con frecuencia, se observa calcio. Precisa diferenciación de las lesiones
papilares benignas, en las que hay mioepitelio y más uniformidad nuclear, así
como epitelio apocrino y células espumosas (Figs. 42 y 43).
Quizá la lesión más difícil de identificar como carcinoma sea la forma tubular
(2%), ya que la atipia es muy escasa (47). La celularidad se encuentra conformando
"tubos" rectos o doblados, con sus extremos angulados. La celularidad de los
tubos es muy densa y los núcleos presentan cromatina borrosa, mal definida.
El fondo de las muestras carece del mioepitelio característico del frotis "benigno".
Como diagnóstico diferencial, el adenoma tubular presenta los grupos más placulares
y acinares que tubulares (Fig. 44).
Igualmente raro es el carcinoma apocrino,
caracterizado por células aisladas o en pequeños grupos, de citoplasma amplio
y granular, azulado con MGG y rosado con PAP, de borde mal definido. Hay anisonucleosis
marcada, núcleos voluminosos, cromatina gruesa y nucléolo prominente, en un
fondo con mayor o menor componente necrótico. Necesita ser diferenciado del
epitelio apocrino benigno procedente de quistes, que descama en placas más uniformes
sobre un fondo seroso. Cuando forma parte de un cuadro más complejo, como es
una mastopatía fibroquística, presenta un fondo con mioepitelio, sin necrosis
y con epitelio ductal benigno (58) (Fig. 45).
Hay otras variantes mucho menos frecuentes de las que están publicados los criterios
para su orientación diagnóstica. En esta revisión sólo se mencionan las lesiones
con bibliografía más reciente: carcinoma ductal hipersecretor
(25), carcinoma anaplásico
de células pequeñas (46) y carcinoma neuroendocrino
(12). Las lesiones "in situ" tienen un diagnóstico diferencial con las infiltrantes,
e incluso con proliferaciones benignas atípicas, muy complejo (38).
Por último, hay lesiones, raras, con
metaplasia, de difícil valoración citológica. Suelen hacer la metaplasia
hacia un carcinoma epidermoide, pero puede verse cualquier tipo de sarcoma,
lo que provoca cuadros muy difíciles de interpretar, y en los que buscaremos
siempre el componente "ductal". Son tumores, en general, con muy mal pronóstico.
TUMOR FILLODES
Son lesiones que pueden alcanzar un gran tamaño, y cuya benignidad o malignidad
es difícil de confirmar incluso con material histológico, por lo que la citología
tiene un importante reto en este campo.
Frotis: placas de epitelio muy similares a las del fibroadenoma, con
mioepitelio, y placas de estroma. Cuanto más estroma y mayor anaplasia haya
en él, las posibilidades de que la lesión sea maligna son más altas. A veces
se asocia atipia del epitelio glandular.
Diagnóstico diferencial: el propio fibroadenoma, especialmente formas
juveniles, ricas en estroma, que suelen tener más uniformidad en las placas
de epitelio y menos densidad celular en los grupos estromales (Figs.
46 a 48). Los verdaderos sarcomas, que también pueden darse en la mama,
carecen del componente epitelial.
GINECOMASTIA
Es un aumento del tamaño de la mama masculina, que suele cursar con dolor (la
propia punción de la ginecomastia suele ser muy dolorosa) y que suele aparecer
como respuesta a estímulos metabólicos y hormonales.
Frotis: abundantes láminas y grupos tridimensionales de celularidad uniforme,
aunque hay amoldamientos y células hipercromáticas. El fondo tiene pequeños
fragmentos de tejido conectivo con fibroblastos fusocelulares (13,30).
Existen, además, varios cuadros muy infrecuentes cuya existencia conviene,
al menos, conocer:
- Adenoma de la lactancia:
Presenta una gran celularidad, con frecuencia en elementos aislados, de núcleo
grande con nucleólo y cromatina gruesa ("cuerpos del calostro") en un fondo
sucio con necrosis y detritus celulares. El frotis puede sugerir malignidad
si no se conoce la circunstancia clínica de embarazo (18).
- Tumores mioepiteliales.
Los sospecharemos cuando el frotis presente células con citoplasma amplio
y claro, similares a los tumores de "células claras" (Fig. 49).
- Tumor de células granulares
(10,49): células aisladas de amplio citoplasma con borde mal definido y fina
granulación PAS+; el núcleo es redondeado, "benigno" y excéntrico. Pueden
ser difíciles de diferenciar de lesiones con histiocitos, que hay que tener
en cuenta, si bien estas últimas suelen tener historia quirúrgica-traumática
previa.
- Hamartoma. Se presenta como un nódulo bien definido, en pacientes
jóvenes. La celularidad obtenida no difiere de la que se encuentra en la mama
normal: acinos, ductos y estroma fibroadiposo, sin rasgos de atipia.
- Tumores de anejos cutáneos. Son muy raros. En lesiones de localización
superficial, preferentemente periareolar, deben ser tenidos en cuenta.
- Tumores de "partes blandas". Son menos del 1% de los tumores de
la mama, y el más frecuente es el angiosarcoma, reconocible cuando el aspirado
obtiene "luces" amplias ocupadas por material hemático.
- Carcinoma adenoquístico.
La celularidad descama en grupos de células pequeñas entre los que destacan
espacios vacíos y ocupados por "bolas" de material metacromático con MGG (20).
Igualmente, en la mama son posibles tumores similares a los de las glándulas
salivales, como el adenomioepitelioma
(27,40), el carcinoma mucoepidermoide o el tumor mixto-adenoma pleomorfo.
- Linfomas.
Quizá no sea difícil su sospecha, pero sí definirse con certeza sobre su existencia
y tipo. Suelen ser linfomas no Hodgkin, de bajo grado de malignidad. Hay que
advertir que en la mama, aunque raro, puede haber ganglios, especialmente
en su cuadrante superoexterno, cerca de la axila. Su punción puede llevarnos
a un diagnóstico erróneo de linfoma si no reparamos en la polimorfía de la
población linfoide aspirada. Además, la lobulitis linfocitaria esclerosante
de la mama, así como diversos cuadros inflamatorios, cuyas PAAFs pueden ser
muy ricas en linfocitos, deben ser convenientemente descartadas (22,37).
- Metástasis. La lesión
"metastásica" más frecuente es la procedente de un carcinoma de la mama contralateral,
seguida de los tumores de pulmón, el melanoma y cuadros de origen en ovario
y aparato digestivo. La melanina, los cuerpos de psammoma y las empalizadas
celulares periféricas, pueden ayudar a identificar el origen, respectivamente,
en los tres últimos casos, pero con frecuencia es difícil incluso "hablar"
de metástasis (48).
PROBLEMAS DIAGNÓSTICOS
EN LA PAAF DE MAMA
No obstante, la práctica diaria va determinando una problemática cuya resolución
suele incluir la colaboración del clínico y el radiólogo, así como la de otros
compañeros y la bibliografía al uso:
- El diagnóstico
en el lecho tumoral: recidivas VS focos de necrosis postradiación.
Las atipias que pueden verse se intentan dilucidar mediante inmunocitoquímica
(ICQ), pero en las lesiones recidivadas los factores de proliferación se ven
modificados al alza o a la baja, según casos, y, a veces, el tumor pierde
toda referencia ICQ. Tras la radioterapia hay una importante necrosis grasa
de difícil resolución, y tras la colocación de prótesis, la reacción cicatricial
puede incluir fibroblastos activados con núcleos muy irregulares, por lo que
en ambos casos hay que ser muy cautos antes de dar un diagnóstico de recidiva.
Como norma, el fondo inflamatorio y las grandes atipias, con células gigantes,
indican benignidad y la atipia nuclear franca es más sugerente de malignidad.
- Hiperplasia
epitelial VS carcinoma ductal bien diferenciado (1,2,44,50). Es un problema
serio que se plantea en un importante número de punciones (5-20%, según las
series). Son rasgos orientadores de malignidad:
- Predominio de grupos sobre placas.
- Grupos grandes con arquitectura cribiforme: figuras en arco y "puente
romano", o espacios claros y redondeados en el seno de grupos tridimensionales.
Este rasgo parece especialmente indicador de un carcinoma de tipo cribiforme
(6) (Fig. 50).
- Amontonamiento nuclear y pérdida de la polaridad de los núcleos.
- Membrana nuclear gruesa y nucléolos.
- Mitosis.
El estudio de DNA mediante citometría de flujo, si bien no resulta definitorio,
sí puede emplearse en el diagnóstico diferencial de cuadros benignos VS
malignos, ya que una aneuploidia alta es muy sugerente de corresponder a
un cuadro maligno, aunque en estos casos la morfología celular también suele
ser suficientemente clara. Igualmente útiles parecen ser los organizadores
nucleolares (AgNORs), que incluso tienen relación con el grado de diferenciación
según varios autores.
- Carcinoma "in situ"
VS Carcinoma infiltrante (38,53,56). Es prácticamente imposible hacer
una diferenciación, con material de punción, entre las células procedentes
de un tumor "in situ" y de un proceso infiltrante. No obstante, las lesiones
"in situ" con necrosis tipo comedo proporcionan tal suciedad en el fondo del
frotis, con un aspecto tan "epidermoide", que, según algunos autores, a veces,
puede sugerirse.
- Las
proliferaciones papilares suelen ser muy difíciles de calificar, y
ante la menor duda es aconsejable realizar una biopsia. Los rasgos que favorecen
la idea de malignidad son la uniformidad celular, especialmente si hay rasgos
neuroendocrinos, y la actividad mitótica. Las papilas del carcinoma papilar
pueden tener un eje fibrovascular del que carecen las pseudopapilas de los
procesos benignos. La expresión de ciclina-D1 también orienta hacia un carácter
maligno (26,50).
- El Tumor fillodes presenta una dificultad particular tanto en su
reconocimiento como en indicar su naturaleza. Las formas "benignas" precisan
diferenciarse del fibroadenoma, especialmente del "juvenil". El T. fillodes
se da en edad mucho más avanzada, con placas epiteliales más "blandas" y grupos
estromales más densos. Las formas malignas pueden plantear problemas con los
sarcomas, que suelen ser más "atípicos" en sus elementos estromales y suelen
carecer de componente epitelial. Además, ante una lesión con elementos fusocelulares,
hay que descartar un carcinoma con crecimiento fusocelular, una neoplasia
mioepitelial, y una lesión proliferativa, no sarcomatosa, de "partes blandas"
(17).
BIBLIOGRAFÍA
- Abendroth CS, Wang HH, Ducatman BS. Comparative
features of carcinoma in situ and atypical ductal hyperplasia of the breast
on fine needle aspiration biopsy specimen. Am J Clin Pathol 1991; 96:654-659.
- Al Kaisi N. The spectrum of "gray zone" in breast
cytology: A review of 186 cases of atypical and suspicious cytology. Acta
Cytol 1994; 38:898-908.
- Antúnez J, García-Caballero T, Abdulkader I, Caparrini
A, Pintos E, Fraga-Rodríguez M, Beiras-Iglesias A, Forteza J. Aplicaciones
de la inmunohistoquímica y la microscopía electrónica en el diagnóstico
citológico por punción con aguja fina. Rev Esp Pat 1998; 31:435-459.
- Antúnez-Potashkina I, Coro-Antich RM, Rodríguez
-Ceballos S. Morfometría computerizada en aspirados celulares del carcinoma
ductal infiltrante de la mama. Modelo de estadística multivariada. Rev Esp
Patol 1997; 30:193-199.
- Arisio R, Cuccorese C, Accinelli G, Mano MP, Bordon
R, Fessia L. Role of fine-needle aspiration biopsy in breast lesions: analysis
of a series of 4.110 cases. Diagn Cytopathol 1998; 18:462-467.
- Barredo Santamaría I, Burgos Bretones JJ, García
Riego A, Rivera Pomar JM. Carcinoma cribiforme infiltrante de la mama: aspectos
citológicos. Rev Esp Patol 1999; 32:529-533.
- Benoit JL, Kara R, McGregor SE, Duggan MA. Fibroadenoma
of the breast: Diagnostic pitfalls of fine-needle aspiration. Diagn Cytopathol
1992; 8:643-648.
- Bibbo M, Abati A. Editorial: The Uniform Approach
to Breast Fine Needle Aspiration Biopsy. A synopsis. Acta Cytol 1996; 40:1119-1126.
- Cardiel -García MJ, Ríos-Mitchell MJ, Valero-Palomero
MI, Del Agua-Arias C, Sanz-Moncasi P. Utilidad de la citología por raspado
de bordes como técnica intraoperatosia de detección de márgenes quirúrgicos
positivos en biopsias de mama. Rev Esp Pat 1997; 30:112-116.
- Chachlani N, Yue ChT, Gerardo LT. Granular cell
tumor of the breast in a male. Acta Cytol 1997; 41:1807-1810.
- Choreutaki T, Scarpellini F, Eusebi V. Breast cancer
necrosis following fine needle aspiration biopsy. Tumori 1996; 82:242-244,
abst.
- Chua RS, Torno RB, Vuletin JC. Fine needle aspiration
cytology of small cell neuroendocrine carcinoma of the breast: a case report.
Acta Cytol 1997; 41:1341-1344.
- Das DK, Junaid TA, Matheus SB, Ajrawi TG, Ahmed
MS, Madda JP, Mirza K. Fine needle aspiration cytology diagnosis of male
breast lesions: A study of 185 cases. Acta Cytol 1995; 39:870-876.
- Dawson AE, Mulford DK, Sheils LA. The cytopathology
of proliferative breast disease: comparison with features of ductal carcinoma
in situ. Am J Clin Pathol 1995; 103:438-442.
- Dawson AE, Mulford DK. Five needle aspiration of
mucinous (coloide) breast carcinoma. Nuclear grading and mammographic and
cytologyc findings. Acta Cytol 1998; 42:668-672.
- De Souza Rocha P, Nadkarni NS, Menezes S. Fine
needle aspiration biopsy of breast lesions and histopathologic correlation.
An analysis of 837 cases in four years. Acta Cytol 1997; 41:705-712.
- Deen SA, McKee GT, Kissin MW. Differential cytologic
features of fibroepithelial lesions of the breast. Diagn Cytopathol 1999;
20:53-56.
- Finley JL, Silverman JF, Lannin DR. Fine needle
aspiration cytology of breast masses in pregnant and lactating women. Diag
Cytopath 1989; 5:255-259.
- Gupta D, Rajwanshi A, Gupta SK, Nijhawan R, Saran
RK, Rajendra S. Fine needle aspiration cytology in the dignosis of tuberculous
mastitis. Acta Cytol 1999; 43:191-194.
- Gupta RK, Green C, Naran S, Lallu S, Franck R,
Dowle C, Simpson J. Fine-needle aspiration cytology of adenoid cystic carcinoma
of the breast. Diagn Cytopathol. 1999; 20:82-84.
- Head JF, Haynes AE, Elliott MC, Elliott RL. Stereotaxic
localization and core needle biopsy of nonpalpable breast lesions: two-year
follow-up of a prospective study. Am Surg 1996; 62:1018-23.
- Hernández-Ortiz MJ, Amengual-Antich I, Torrecabota-Pages
J, Canet-Ribas de la Pina R. Mastitis linfocitaria: un diagnóstico difícil
en la punción aspiración con aguja fina. Rev Esp Patol 1998; 31:313-316.
- Joshi A, Kapila K, Verma K. Fine needle aspiration
cytology in the management of male breast masses. Nineteen years of experience.
Acta Cytol 1999; 43:334-388.
- Kamiya M, Mizuguchi K, Yoshimoto M, Tanaka M, Moteji
S, Matushima H, Ishizawa M, Nakamura K. Cytologic diagnosis of signet-ring
cell carcinoma of the breast. Acta Cytol 1998; 42:650-656.
- Kratzer SS, Cramer HM, Reynolds HE, Seo IS, Canal
DF. Fine-needle aspiration cytology of cystic hypersecretory ductal carcinoma
in situ of the breast: a case report. Diag Cytopathol 1999; 20:160-163.
- Kumar PV, Talei AR, Malekhusseini SA, Monabati
A, Vasei M. Papillary carcinoma of the breast. Cytologic study of nine cases.
Acta Cytol 1999; 43:767-770.
- Laforga TB, Aranda FI, Sevilla F. Adenomyopithelioma
of the breast: report of two cases with prominent cystic changes and intranuclear
inclusions. Diagn Cytopathol 1998; 19:55-58.
- Lazda EJ, Kocjan G, Sams VR, Wotherspoon AC, Taylor
I. Fine needle aspiration (FNA) cytology of the breast: the influence of
unsatisfactory samples on patient management. Cytopathology 1996; 7:262-7.
- Liberman L, LaTrenta LR, Dershaw DD, et al.Impact
of core biopsy on surgical management of impalpable breast cancer. Am J
Roentgenol 1997; 168:495-499; abst.
- Lilleng R, Paksoy N, Vural G, Langmark F, Hagmar
B. Assesment of fine needle aspiration cytology and histopathology for diagnosisng
male breast masses. Acta Cytol 1995; 39:877-881.
- Logrono R, Kurtycz DF, Inhorn SL. Criteria for
reporting fine needle aspiration on palpable and nonpalpable masses of the
breast. Acta Cytol 1997; 41:623-627.
- López-Ríos F, Dhimes P, De Agustín PP. Subareolar
abscess of the breast in a male. A report of two cases with fine needle
aspiration cytology diagnosis. Acta Cytol 1997; 41:1819-1822.
- Lozano MD, Panizo A. Papel de la inmunohistoquímica
en citología. Rev Esp Patol 1998; 31:63-66.
- Martins Collaço L, Silveira de Lima R, Werner B,
Bleggi Torres LF. Value of fine needle aspiration in the diagnosis of breast
lesions. Acta Cytol 1999; 43:587-592.
- Massod S. Editorial: Fine needle aspiration of
a breast: a practical approach to diagnosis of carcinoma. Acta Cytol 1998;
42:283-284.
- Medina-Pérez M, López-Hidalgo J, Oliva-Mompeán
F, Acedo-Díaz F. Diagnóstico inmediato por PAAF del carcinoma de mama palpable.
Rev Esp Patol 1999; 32:35-40.
- Miralles TG, Gozalbez F, Menéndez P, Monjón JA,
Sampedro A. Fine-needle aspiration of sclerosisg limphocytic lobulitis of
the breast. A report of two cases. Acta Cytol 1998; 42:1447-1450.
- Moriya T, Job MK, Silverberg SG. Detection of ductal
carcinoma in situ of the breast in cytologic samples. Acta Cytol 1992; 37:767-768.
- Nada R, Ganguli M, Dey P. Reactive limphoid hyperplasia
presenting as a palpable nodule in the breast. Acta Cytol 1997; 41:1868-1869
(letter).
- Niemann TH, Benda JA, Cohen MB. Adenomyoepithelioma
of the breast: fine-needle aspiration biopsy and histologic findings. Diagn
Cytopathol 1995; 12:245-250.
- Page DL, Johnson JE, Dupont WD. Probabilistic approach
to the reporting of fine-needle aspiration cytology of the breast. Cancer
(Cancer Cytopathol) 1997; 81:6-9.
- Rivera-Pomar JM, Vilanova JR, Burgos-Bretons JJ;
Arocena G. Focal fobrous disease of the breast: A common entity in young
women. Wirchows Arch. 1980; 386:59-64.
- Rivera Pomar JM, Santamaría Martínez M. Mama femenina,
En Rodríguez Costa J , De Agustín Vázquez D (ed.). Punción Aspiración con
aguja fina de órganos superficiales y profundos. Madrid, Díaz de Santos,
1997, pp 161-207.
- Rogers LA, Lee KR. Breast carcinoma simulating
fibroadenoma or fibrocystic change by fine-needle aspiration: A study of
16 cases. Am J Clin Pathol 1992; 98:155-160.
- Rosen PP. Mammary mucocele-like lesions. Benign
and malignant. Am J Surg Pathol 1996; 20:1081-1085.
- Sebenik M, Nair SG, Hamati HF. Primary small cell
anaplastic carcinoma of the breast diagnosed by fine needle aspiration cytology:
a case report. Acta Cytol 1998; 42:1199-1203.
- Shet TM, Rege JD. Aspiration cytology of tubular
adenomas of the breast: an analysis af eight cases. Acta Cytol 1998; 42:657-662.
- Silverman JF, Feldman PS, Covell JL, Frable JW.
Fine needle aspiration cytology of neoplasm metastatic to yhe breast. Acta
Cytol 1987; 31:291-300.
- Sirgi KE, Sneige N, Fanning TV et al. Fine-needle
aspirates of granular cell lesions of the breast: report of three cases,
with emphasis on differential diagnosis and utility of immunostaining for
CD68 (KP1). Diagn Cytopathol 1996; 15:403-8.
- Sneige N. Fine-needle aspiration of the breast:
A review of 1995 cases with emphasis on diagnostic pitfalls. Diagn Cytopathol
1993; 9:106-112.
- Sneige N, Staerkel GA, Caraway NP, Fanning TV,
Katz RL. A plea for uniform terminology and reporting of breast fine needle
aspirates: The M.D. Anderson Cancer Center Proposal. Acta Cytol 1994; 38:971-972.
- Stanley MW, Abele J, Kline T, Silverman JF, Skoog
L. What constitues adequate sampling of palpable breast lesions that appear
benign by clinical and mammographic criteria?. Diang Cytopathol 1995; 13:473-82.
- Theocharous C, Greenberg ML. Cytologic features
of ductal carcinoma in situ. Diagn Cytopathol 1966; 15:367-73.
- Torres FJ, Garrido A, Rodero MC, Galera H. Diagnóstico
citológico. En Matilla A, Galera H (ed.) Cáncer de mama. Patología básica,
diagnóstico y tratamiento. Universidad de Málaga, 1981, pp 85-102.
- Wang HH, Ducatman BS, Eick D. Comparative features
of ductal carcinoma in situ and infiltrating ductal carcinoma of the breast
on fine-needle aspiration biopsy. Am J Clin Pathol 1989; 92:736-740.
- Wang HH, Ducatman BS. Fine needle aspiration of
the breast. A probabilistic approach to diagnosis of carcinoma. Acta Cytol
1998; 42:285-289.
- Yoshida K, Inoue M, Furuta S, Sakai R, Imai R,
Hayakawa S, Fukatsu T, Nagasaka T, Nakashima N. Apocrine carcinoma vs. Apocrine
metaplasia with atypia of the breast: Use of aspiration biopsy cytology.
Acta Cytol 1996; 40:247-251.
- Yu GH, Sethi S, Cajulis RS, Gokaslan S, Frías-Hidvegi
D. Benign Pairs. A useful discriminating feature in fine needle aspirates
of the breast. Acta Cytol 1997; 41:721-726.
- Zardawi IM, Hearden , Meyer P, Trevan B. Ultrasound-guided
fine needle aspiration cytology of impalpable breast lesionsin a rural setting.
Comparison of cytology with imagin and final outcome. Acta Cytol 1999; 43:163-168.
IMÁGENES
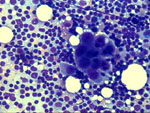 Figura 1. MGG, x20.
Punción axilar en la que se ve un grupo de células con núcleo denso
y nucléolo entre una población linfoide mixta. La punción de ganglios
linfáticos para decidir la existencia o no de metástasis es de reconocida
utilidad en la práctica diaria por su extraordinaria sensibilidad diagnóstica.
Figura 1. MGG, x20.
Punción axilar en la que se ve un grupo de células con núcleo denso
y nucléolo entre una población linfoide mixta. La punción de ganglios
linfáticos para decidir la existencia o no de metástasis es de reconocida
utilidad en la práctica diaria por su extraordinaria sensibilidad diagnóstica.
|
|
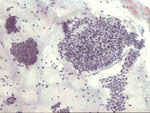 Figura 2.
Figura 2. |
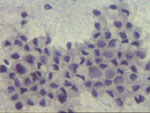 Figura 3.
Figura 3. |
Pap., x40 y x100. Cambios en un fibroadenoma durante
la lactancia. Comparar la placa de la izquierda, pequeña y de citoplasmas
cianófilos, con la de la derecha, que muestra citoplasmas amplios y
claros. En la imagen a mayor aumento destaca la anisonucleosis, con
frecuencia asociada a rasgos de actividad nuclear, que puede llevar
a un error diagnóstico.
|
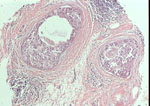 Figura 4.
Figura 4. |
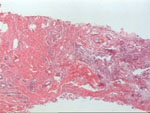 Figura 5.
Figura 5. |
H/E por 100. Cilindros tisulares obtenidos de mama donde
se muestra una lesión infiltrante de tipo lobulillar (4) y un carcinoma
"in situ" comedo (5). Los cilindros de nódulos grandes pueden realizarse
sin control radiológico pero los destinados a focos de microcalcificación
requieren precisos instrumentos que identifiquen la lesión y que introduzcan
el sistema de toma de muestra.
|
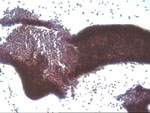 Figura 6. Pap, x200. Ducto
en forma de tubo con los núcleos en dos capas, que en el extremo izquierdo
se abre y se presenta en forma de placa con los núcleos en una sola
capa. Alrededor del tubo (parte derecha de la imagen) se observa un
fino reborde que corresponde al mioepitelio, que al romperse el ducto
se desparrama por el fondo de la muestra.
Figura 6. Pap, x200. Ducto
en forma de tubo con los núcleos en dos capas, que en el extremo izquierdo
se abre y se presenta en forma de placa con los núcleos en una sola
capa. Alrededor del tubo (parte derecha de la imagen) se observa un
fino reborde que corresponde al mioepitelio, que al romperse el ducto
se desparrama por el fondo de la muestra.
|
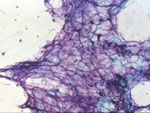 Figura 7. MGG, x40. Tejido
adiposo maduro. Es un material que se obtiene en punción frecuentemente,
especialmente en las lesiones benignas.
Figura 7. MGG, x40. Tejido
adiposo maduro. Es un material que se obtiene en punción frecuentemente,
especialmente en las lesiones benignas.
|
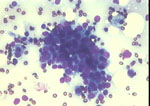
Figura 8.QDF, x200. Grupo tridimensional,
con amontonamiento de núcleos que presentan leves diferencias en el
tamaño, en un fondo benigno con células espumosas. El estudio histológico
mostró un cuadro mastopático con numerosos grupos de adenosis.
|
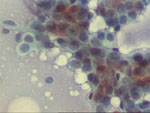
Figura 9.Pap, x400. Grupo irregular con anisonucleosis,
amontonamiento nuclear y nucléolos, aunque también conserva mioepitelio.
La pieza quirúrgica presentó una fibroadenoma intracanalicular con un
componente epitelial proliferado.
|
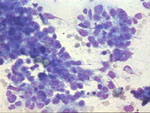 Figura 10. Pap, x200. Grupos
laxos con elementos de talla variable, amontonados, de nucléolo prominente,
en un fondo sucio. La pieza histológica mostró un carcinoma ductal infiltrante.
Figura 10. Pap, x200. Grupos
laxos con elementos de talla variable, amontonados, de nucléolo prominente,
en un fondo sucio. La pieza histológica mostró un carcinoma ductal infiltrante.
|
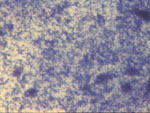 Figura 11.QDF, x400. Fondo
granular con elementos espumosos en degeneración. Todo el frotis presenta
un aspecto uniforme, y procede de una lesión quística que al aspirar
proporciona un líquido denso y blanquecino-grisáceo.
Figura 11.QDF, x400. Fondo
granular con elementos espumosos en degeneración. Todo el frotis presenta
un aspecto uniforme, y procede de una lesión quística que al aspirar
proporciona un líquido denso y blanquecino-grisáceo.
|
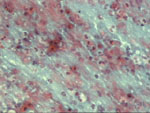 Figura 12. Pap, x200. Fondo
necrótico entre el que destacan polimorfonucleares neutrófilos, escasos
linfocitos y elementos de citoplasma eosinófilo denso con núcleos pequeños
y oscuros que pueden sugerir malignidad.
Figura 12. Pap, x200. Fondo
necrótico entre el que destacan polimorfonucleares neutrófilos, escasos
linfocitos y elementos de citoplasma eosinófilo denso con núcleos pequeños
y oscuros que pueden sugerir malignidad.
|
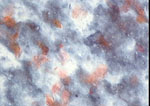 Figura 13. Pap, x400. En
las lesiones retroareolares destacan las escamas anucleadas entre un
fondo necrótico.
Figura 13. Pap, x400. En
las lesiones retroareolares destacan las escamas anucleadas entre un
fondo necrótico.
|
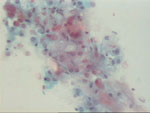 Figura 14. Pap., x200. Grupo
de histiocitos y células epitelioides, polimorfonucleares neutrófilos
y linfocitos entre espacios ópticamente vacíos correspondientes a grasa.
La punción se realizó sobre un área dolorosa que apareció tras un traumatismo.
Figura 14. Pap., x200. Grupo
de histiocitos y células epitelioides, polimorfonucleares neutrófilos
y linfocitos entre espacios ópticamente vacíos correspondientes a grasa.
La punción se realizó sobre un área dolorosa que apareció tras un traumatismo.
|
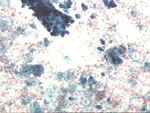 Figura 15. Pap, x100. Quiste
de mama. Fondo granular azurófilo en el que destacan células espumosas
con material fagocitado que les dan una coloración oscura.
Figura 15. Pap, x100. Quiste
de mama. Fondo granular azurófilo en el que destacan células espumosas
con material fagocitado que les dan una coloración oscura.
|
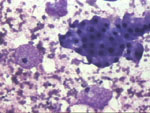 Figura 16.QDF, x200. Fondo
seroso sucio con histiocitos espumosos y una placa de epitelio apocrino.
Figura 16.QDF, x200. Fondo
seroso sucio con histiocitos espumosos y una placa de epitelio apocrino.
|
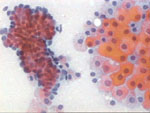 Figura 17. Pap., x200. Dos
grupos, de epitelio apocrino el de la derecha y de epitelio ductal el
de la izquierda, procedentes de una mastopatía fibroquística con focos
de fibroadenomatosis y con quistes que presentan metaplasia apocrina.
Figura 17. Pap., x200. Dos
grupos, de epitelio apocrino el de la derecha y de epitelio ductal el
de la izquierda, procedentes de una mastopatía fibroquística con focos
de fibroadenomatosis y con quistes que presentan metaplasia apocrina.
|
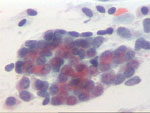 Figura 18
Figura 18. |
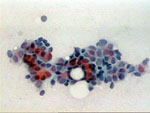 Figura 19
Figura 19. |
Pap., x200. Grupos celulares con los elementos
dispuestos en coronas acinares mal definidas. Ambos grupos proceden de
un área mastopática, en diferentes pacientes, que en su mayor parte estaba
constituido por focos de adenosis.
|
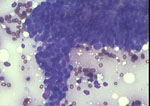 Figura 20.QDF, x200. Placa
ductal con una proyección papilar que muestra un leve amontonamiento
de núcleos con talla y morfología regular. Con frecuencia los ductos
dilatados de una mastopatía tienen proyecciones digitiformes que requieren
una cuidadosa observación pero que no suelen suponer un gran problema
diagnóstico.
Figura 20.QDF, x200. Placa
ductal con una proyección papilar que muestra un leve amontonamiento
de núcleos con talla y morfología regular. Con frecuencia los ductos
dilatados de una mastopatía tienen proyecciones digitiformes que requieren
una cuidadosa observación pero que no suelen suponer un gran problema
diagnóstico.
|
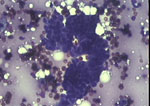 Figura 21.QDF, x200. Grupo
tridimensional de morfología papilar, levemente irregular, con espacios
en su espesor, que mantiene la cohesión de los grupos benignos pero
que carece de la limpieza de estos. La pieza quirúrgica presentó una
mastopatía fibroquística con diversas hiperplasias epiteliales entre
las que se encontraba la papilomatosis.
Figura 21.QDF, x200. Grupo
tridimensional de morfología papilar, levemente irregular, con espacios
en su espesor, que mantiene la cohesión de los grupos benignos pero
que carece de la limpieza de estos. La pieza quirúrgica presentó una
mastopatía fibroquística con diversas hiperplasias epiteliales entre
las que se encontraba la papilomatosis.
|
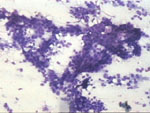 Figura 22. QDF, x200. Grupo
ductal de disposición laxa y con espacios claros en su espesor que presentan
células con cierta irregularidad del tamaño nuclear y diferencias en
el cromatismo nuclear. La pieza quirúrgica presentó una mastopatía fibroquística
con diversas hiperplasias epiteliales entre las que se encontraba la
epiteliosis, sin llegar al carcinoma "in situ".
Figura 22. QDF, x200. Grupo
ductal de disposición laxa y con espacios claros en su espesor que presentan
células con cierta irregularidad del tamaño nuclear y diferencias en
el cromatismo nuclear. La pieza quirúrgica presentó una mastopatía fibroquística
con diversas hiperplasias epiteliales entre las que se encontraba la
epiteliosis, sin llegar al carcinoma "in situ".
|
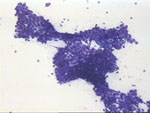 Figura 23. QDF, x100. Característico
grupo ductal procedente de un fibroadenoma de mama. La morfología del
grupo se complementa con elementos de talla y morfología regulares en
un fondo con mioepitelio y fragmentos de estroma.
Figura 23. QDF, x100. Característico
grupo ductal procedente de un fibroadenoma de mama. La morfología del
grupo se complementa con elementos de talla y morfología regulares en
un fondo con mioepitelio y fragmentos de estroma.
|
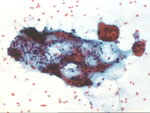 Figura 24. Pap, x100. En
el fibroadenoma, al igual que en otros cuadros benignos, es frecuente
la obtención de estroma fibroadiposo. Es este caso se acompaña de células
gigantes, un dato inhabitual, pero en absoluto raro, acompañando cualquier
patología de la mama.
Figura 24. Pap, x100. En
el fibroadenoma, al igual que en otros cuadros benignos, es frecuente
la obtención de estroma fibroadiposo. Es este caso se acompaña de células
gigantes, un dato inhabitual, pero en absoluto raro, acompañando cualquier
patología de la mama.
|
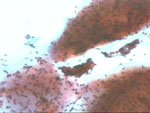 Figura 25. Pap, x200. Dos
grupos de estroma, densos pero con moderada celularidad oscurecen la
observación de dos pequeños grupos epiteliales que presentan un leve
amontonamiento nuclear de elementos regulares en talla y morfología.
La pieza histológica mostró un fibroadenoma con estroma mixoide.
Figura 25. Pap, x200. Dos
grupos de estroma, densos pero con moderada celularidad oscurecen la
observación de dos pequeños grupos epiteliales que presentan un leve
amontonamiento nuclear de elementos regulares en talla y morfología.
La pieza histológica mostró un fibroadenoma con estroma mixoide.
|
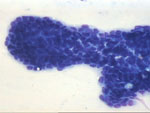
Figura 26. QDF, x200. Adenoma
tubular. Grupo redondeado de células ductales con leve amontonamiento
nuclear en el que la celularidad carece de irregularidad.
|
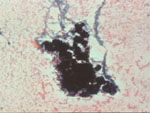
Figura 27. Pap, x100.
Grupo papilar entre un fondo hemático, procedente de un papiloma intraductal.
El grupo presenta proyecciones papilares fácilmente visibles cuya
celularidad, que no se puede ver en detalle en la imagen, muestra
regularidad y ausencia de atipia.
|
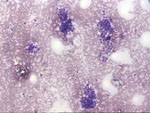
Figura 28. QDF, x40. Varios
grupos celulares de morfología irregular con elementos de talla y
morfología variable, que dejan escapar elementos aislados.
|
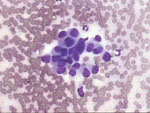 Figura 29. QDF, x200. Grupo
epitelial procedente de la punción de un carcinoma ductal infiltrante.
Unos de los rasgos más determinantes de malignidad es la falta de cohesión
celular, desprendiéndose de los grupos células con el citoplasma íntegro,
que aparecen igualmente dispersas por el fondo de las tomas.
Figura 29. QDF, x200. Grupo
epitelial procedente de la punción de un carcinoma ductal infiltrante.
Unos de los rasgos más determinantes de malignidad es la falta de cohesión
celular, desprendiéndose de los grupos células con el citoplasma íntegro,
que aparecen igualmente dispersas por el fondo de las tomas.
|
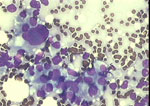 Figura 30. QDF, x400. Carcinoma
ductal infiltrante. De nuevo, la falta de cohesión celular, que junto
a la anisonucleosis y los nucléolos prominentes obligan a considerar
el grupo como maligno.
Figura 30. QDF, x400. Carcinoma
ductal infiltrante. De nuevo, la falta de cohesión celular, que junto
a la anisonucleosis y los nucléolos prominentes obligan a considerar
el grupo como maligno.
|
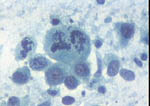 Figura 31. Pap, x400. Con
técnica de Papanicolaou es posible ver mejor el detalle nuclear, la
cromatina y los nucléolos resultan más llamativos, y las mitosis son
fácilmente observables. En la imagen se reconoce una mitosis atípica
que permite un diagnóstico fácil. No obstante, los carcinomas de mama
no se caracterizan por una elevada tasa mitótica.
Figura 31. Pap, x400. Con
técnica de Papanicolaou es posible ver mejor el detalle nuclear, la
cromatina y los nucléolos resultan más llamativos, y las mitosis son
fácilmente observables. En la imagen se reconoce una mitosis atípica
que permite un diagnóstico fácil. No obstante, los carcinomas de mama
no se caracterizan por una elevada tasa mitótica.
|
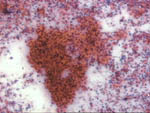 Figura 32. Pap, x40. Las
lesiones tipo comedo proporcionan con frecuencia grupos irregularmente
redondeados con elementos desprendidos en sus bordes y centros con material
necrótico en un fondo igualmente necrótico. La existencia de estos grupos,
sin otros grupos más pequeños de claro aspecto maligno pueden inducirnos
a pensar en un carcinoma "in situ".
Figura 32. Pap, x40. Las
lesiones tipo comedo proporcionan con frecuencia grupos irregularmente
redondeados con elementos desprendidos en sus bordes y centros con material
necrótico en un fondo igualmente necrótico. La existencia de estos grupos,
sin otros grupos más pequeños de claro aspecto maligno pueden inducirnos
a pensar en un carcinoma "in situ".
|
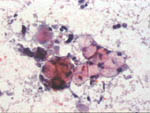 Figura 33. Pap, x200. Carcinoma
rico en lípìdos. Los citoplasmas tan vacuolados con rechazo del núcleo
permiten sospechar lesiones como el carcinoma rico en lípidos o en glucógeno.
Figura 33. Pap, x200. Carcinoma
rico en lípìdos. Los citoplasmas tan vacuolados con rechazo del núcleo
permiten sospechar lesiones como el carcinoma rico en lípidos o en glucógeno.
|
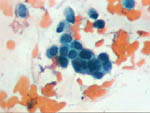 Figura 34. Pap, x40. Carcinoma
lobulillar infiltrante. Grupo relativamente compacto de células con
talla pequeña (compárese con los hematíes de alrededor) que presentan
moldeamientos entre sí.
Figura 34. Pap, x40. Carcinoma
lobulillar infiltrante. Grupo relativamente compacto de células con
talla pequeña (compárese con los hematíes de alrededor) que presentan
moldeamientos entre sí.
|
|
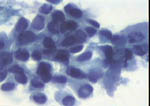 Figura 35
Figura 35. |
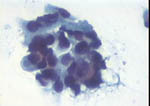 Figura 36
Figura 36. |
QDF, x200. Carcinoma lobulillar infiltrante. Ambas imágenes
presentan un grupo celular en el que los elementos presentan moldeamientos,
tienden a la disposición lineal y presentan vacuolas citoplasmáticas,
muy características, pero no exclusivas, de las lesiones lobulillares.
|
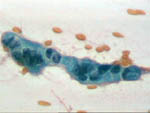 Figura 37
Figura 37. |
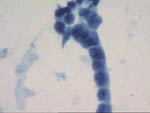 Figura 38
Figura 38.
|
Pap, x200. Carcinoma lobulillar infiltrante. La celularidad,
de tamaño algo mayor que los hematíes, tiende a formar hileras con sus
elementos moldeándose entre sí, remedando la forma de infiltración que
presentan en el estroma mamario.
|
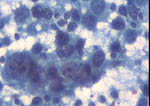 Figura 39
Figura 39. |
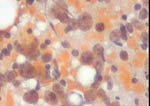 Figura 40
Figura 40. |
QDF y Pap, respectivamente, ambas x200. El carcinoma
medular presenta grupos y abundantes células sueltas con notable atipia,
entre un fondo en el que destacan los linfocitos.
|
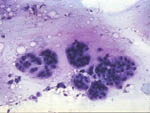 Figura 41.QDF, x100. En
el carcinoma coloide destaca de forma especial el fondo mucoide metacromático
en el que la celularidad neoplásica queda en grupos redondeados.
Figura 41.QDF, x100. En
el carcinoma coloide destaca de forma especial el fondo mucoide metacromático
en el que la celularidad neoplásica queda en grupos redondeados.
|
|
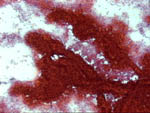 Figura 42
Figura 42. |
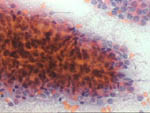 Figura 43
Figura 43. |
Pap, x40 y x200. El carcinoma papilar presenta grupos
claramente papilares en los que a pequeño aumento es posible adivinar
el eje fibrovascular a cuyo alrededor se dispone la celularidad maligna
en una irregular empalizada más fácilmente discernible a mayor aumento.
|
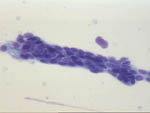
Figura 44. QDF, x20. Conducto
pequeño desflecado en sus extremos procedente de un nódulo que histológicamente
presentó una carcinoma ductal con amplias áreas de crecimiento tubular.
|
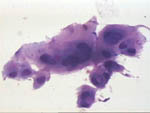
Figura 45. QDF, x400.
El epitelio apocrino es frecuente que tenga atipia nuclear sin que
ello conlleve malignidad. En estos casos, como en todos, es útil un
estudio completo del frotis que permita enfocar el caso hacia una
mastopatía o hacia un tumor apocrino.
|
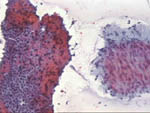 Figura 46
Figura 46. |
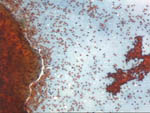 Figura 47
Figura 47. |
 Figura 48
Figura 48. |
|
Pap, x200, x100, x200. Las tres imágenes
corresponden a tres diferentes lesiones de tipo fillodes. La primera,
procedente de una paciente de 16 años, presentó un cuadro histológico
con difícil diferenciación de un fibroadenoma juvenil. La segunda, de
estroma denso pero sin gran atipia corresponde a un tumor fillodes del
que no hay recidiva 4 años después del estudio histológico. La tercera
imagen pertenece a un tumor fillodes claramente maligno, con importante
atipia celular y alta tasa mitótica.
|
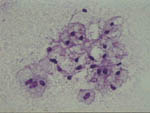
Figura 49. QDF, x200 -
Grupo celular laxo, de citoplasmas claros y núcleos pequeños, redondeados
y sin atipia, procedentes de una lesión que histológicamente mostró
luces ductales con capa mioepitelial prominente.
|
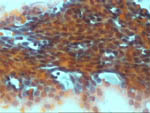
Figura 50. Pap, x100 - Placa
ductal con cierta tridimensionalidad que encierra espacios ópticamente
vacíos y un borde con arcos de cuyos pies se desprenden elementos con
citoplasma conservado. Este grupo, procedente de un fibroadenoma, presenta
características que le incluyen entre los frotis dudosos, y su observación
obliga a estudiar todo el frotis detenidamente para descartar proliferaciones
malignas bien diferenciadas.
|

















































