
ISBN: 978-84-692-76778
 COMUNICACIONES
COMUNICACIONES
Nº 2054. Otras disciplinas
|
Natalia Angel Villegas[1], Julio E Arce Miranda[1], Roque Romero Díaz[2], Mario Zernotti[2], Magdalena Roques Revol[2], Sebastián Picciafuoco[2], Marina Botiglieri[3], Marisa E. Paredes[4], M. Gabriela Paraje[1] |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
xareltoxarelto read hereventolin overdoseventolin over the counter usa xblogs.kompas-xnet.siINTRODUCCIÓN: OBJETIVO: MATERIALES Y MÉTODOS: RESULTADOS: DISCUSIÓN Y CONCLUSIONES:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
INTRODUCCIÓN El biofilms representa una comunidad de microorganismos derivados de células sésiles que crecen unidas irreversiblemente a una superficie sólida, viva o inerte, embebidas en una matriz extracelular producida por ellas mismas, exhibiendo un fenotipo alterado con respecto al índice de crecimiento y transcripción de genes. Aunque la composición del biofilms es variable, en general, el componente mayoritario es el agua, pudiendo representar el 97% del contenido total. La masa de éstas estructuras está formada aproximadamente por un 15% de células y el resto formada principalmente por exopolisacáridos secretados por las propias células que forman parte del mismo, pudiendo contener también, en menor cantidad, proteínas, DNA y productos diversos procedentes de lisis bacteriana. La matriz no es sólida y presenta canales que permiten el flujo de agua, nutrientes y oxígeno incluso hasta en las zonas más profundas, sin embargo, en su interior pueden existir diferentes concentraciones de los mismos, aumentando la heterogeneidad sobre el estado fisiológico en el que se encuentra la bacteria dentro del biofilms. En esa comunidad heterogénea, dinámica y de estructura compleja los microorganismos conviven y poseen un sistema de señales, que dirigen el fenotipo y regulan la expresión de genes que no siempre se expresan en las formas planctónicas o de vida libre. La capacidad de formación de biofilms no parece estar restringida a un grupo específico de microorganismos y se considera que bajo condiciones ambientales adecuadas todos son capaces de formar biofilms, pudiendo estar constituidos por una o más especies bacterianas (Costerton y col, 2003, Flemming, 2007). Actualmente se considera al biofilms como un factor de virulencia, puesto que constituye un modo de crecimiento protegido que permite la supervivencia en un medio hostil, facilitando la unión de las bacterias a distintas superficies, ayudando al mantenimiento de las colonias y protegiéndolas de distintos factores, como los cambios en las condiciones ambientales, la posibilidad de ser fagocitadas por células del huésped, depredadas por otros protozoos o por el efecto de los agentes antimicrobianos. Los biofilms están implicados en infecciones crónicas, lentas, resistentes a los tratamientos, asociadas a la adhesión a tejidos naturales, como en las infecciones otorrinolaringológicas, donde Pseudomonas aeruginosa, Haemophylus influenzae, Streptococcus pneumoniae y Staphylococcus aureus son los microorganismos más frecuentemente asociados. La formación de biofilms bacterianos provoca en el huésped la aparición de una respuesta inmune. Células como leucocitos polimorfonucleares, monocitos y macrófagos inducen una respuesta celular, con alteraciones morfológicas, liberación de especies reactivas del oxígeno y del nitrógeno, de enzimas lisosomales, etc. Esto frecuentemente contribuye a la cronicidad de la infección por el daño causado en el tejido circundante favoreciendo el crecimiento del biofilms. Cuatro criterios se han propuesto para calificar a un biofilms como agente etiológico: I) la bacteria patógena se encuentra asociada a una superficie o adherida a un sustrato; II) el examen directo muestra las bacterias en cúmulos, incrustadas en una matriz propia o formada por componentes del huésped; III) la infección es localizada, y IV) la infección puede ser resistente a los antibióticos (ATB) pese a la sensibilidad de las formas planctónicas. (Palmer, 2005; Post y col 2004; Sanclement y col 2002; Vuong y col, 2004). Otra característica que distingue las infecciones crónicas relacionadas con biofilms de las infecciones agudas, es su respuesta a tratamientos ATB. Varias razones han sido investigadas, aunque el mecanismo preciso de cómo se altera esta sensibilidad no está esclarecido. Aunque no sería el principal mecanismo de resistencia asociada a biofilms, se postula que los ATB podrían penetrar la estructura, pero no alcanzarían una concentración efectiva en algunos sitios del mismo por las características físicas y/o químicas de la matriz. La depleción de nutrientes y oxígeno dentro del biofilms podría ser la causa de que las bacterias se encuentren en un estado de latencia presentando resistencia a ATB comparado con las células planctónicas. También se ha descripto la existencia de microambientes que antagonizan la acción del ATB y mecanismos de degradación activa en algunas partes del biofilms. Debido a la naturaleza heterogénea del biofilms, es probable que existan múltiples mecanismos de resistencia microbiana comparado con las células planctónicas (Stoodley and Costerton, 2002). Una causa de resistencia a los ATB y a las defensas del huésped podría ser la presencia de biofilms en las criptas amigdalinas de pacientes con amigdalitis crónicas. Chole y col. (2002; 2003) han demostrado la presencia de biofilms en piezas quirúrgicas de amígdalas de niños, en quienes la cirugía fue indicada tanto por infecciones recurrentes como por patología obstructiva (hipertrofia), y afirman que las bacterias se encuentran protegidas de las defensas del huésped gracias al biofilms, continuando con su metabolismo y la producción de exotoxinas locales, lo que favorecería la cronicidad de la respuesta inflamatoria. A pesar del grado de conocimiento alcanzado en los últimos años, algunos aspectos importantes sobre biofilms continúan sin ser esclarecidos. En el laboratorio de Higiene y Microbiología de la FCQ-UNC estamos estudiando los mecanismos utilizados por algunos microorganismos para formar y mantener estas comunidades multicelulares, así como la influencia que tienen los biofilms en el proceso infeccioso. OBJETIVO Los objetivos de este trabajo fueron utilizar MCEL para el estudio de biofilms microbianos en tejidos de la vía aérea superior, determinando la calidad y cantidad de biofilms presentes. También, aislar los distintos géneros bacterianos formadores de los mismos y estudiar la capacidad de formar biofilms in vitro.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Muestra
poblacional En el presente trabajo se incluyeron dos tipos de pacientes. Un
grupo de 12 pacientes (entre 36 meses y 6 años de edad) que presentaron
antecedentes de cuadros infecciosos recurrentes u obstrucción de la vía aérea
superior a los cuales se les practicó cirugía de amígdalas o adenoides y otro
grupo de ocho pacientes adultos, de ambos sexos, sometidos a cirugía por
presencia de pólipos nasales. Los
protocolos se encuentran aprobados por los comités de ética de la Facultad de
Ciencias Químicas de la Universidad Nacional de Córdoba y de las dos
Instituciones Hospitalarias participantes, con el correspondiente
consentimiento firmado de los responsables de donar el material para este
estudio. Procesamiento
de la muestra Los
tejidos obtenidos de las cirugías, se extirparon
según técnicas convencionales, sin comprometer su integridad anatómica y luego
se cortaron en rodajas perpendiculares a su diámetro longitudinal las cuales
fueron colocadas, con su debida identificación, en formol 10%. Para el
montaje de las mismas se realizó un lavado con agua corriente para retirar el
exceso de formol y se efectuaron deshidrataciones en alcohol 96º y alcohol 100º
en estufa a 60ºC durante una hora, respectivamente, colocando otra hora,
las muestras en xilol. Se pusieron en un molde de parafina, donde se
dejaron solidificar y luego se realizaron cortes de 2 a 4 micrómetros de
espesor con micrótomo. Posteriormente, se distribuyeron en portaobjetos,
dejando en estufa a 60ºC para su fijación. Antes de
realizar las coloraciones para la observación microscópica, se procedió a
desparafinar el material por inmersiones en xilol, dos veces durante 15 min;
cinco inmersiones en alcohol 100º y 96º respectivamente, lavado con agua destilada
y secado a temperatura ambiente. Estudio
de la presencia de biofilms microbianos mediante Microscopia Confocal de
Exploración Láser Las
muestras fueron enjuagadas durante 10 minutos con Buffer Fosfato Salino (PBS)
estéril 50mM y posteriormente los biofilms fueron observados mediante MCEL
utilizando como colorantes una solución de yoduro de propidio (15μM) durante 5
minutos a temperatura ambiente para detectar las células bacterianas en rojo. A
continuación, se realizó un lavado con PBS y luego las muestras fueron
expuestas a una solución de 50 microgramos/ml de concanavalina A (Con A)
isotiocianato de fluoresceína (FITC), al mismo tiempo y temperatura que el
colorante anterior, para detectar la matriz de glucocáliz en color verde. El
yoduro de propidio fue exitado a 520 nm y las emisiones fueron monitoreadas a
620 nm mientras que el FICT fue exitado a 495 nm y monitoreado a 525 nm. (Psaltis
y col, 2007). Los
biofilms fueron examinados de manera no destructiva utilizando un MCEL (Olympus Fluoview Espectral FV1000) equipado
con una lente de inmersión 100X/1.40 (Olympus UPlanSApo UIS2). Se recogieron
secciones ópticas de 0,87 micras del espesor total del biofilms y
posteriormente las imágenes de tres posiciones elegidas al azar fueron
obtenidas y analizadas. Para el análisis de la imagen, tres investigadores
(JAM, NAV y MGP) evaluaron de forma independiente a simple ciego las imágenes
de una manera retrospectiva. Cuantificación in vitro de la
formación de biofilms La capacidad de formar biofilms in vitro se midió mediante la adhesión a placas de 96 pocillos utilizando el método de O`Toole y Kolter (1998) basado en la capacidad de las bacterias de formar biofilms sobre superficies sólidas y su posterior tinción con Cristal Violeta y elusión con alcohol/acetona (70:30), determinando la densidad óptica a 595nm. (Deighton y col,2001) Para llevar a cabo el estudio se
realizó un cultivo
over-night de cada especie bacteriana correspondiente a una DO595 nm
= 0,8 medida en espectrofotómetro (UV-1601 PC visible
Shimadzu). Luego se realizó
una dilución 1/100 del cultivo over-night en caldo tripetína-soya, la cual fue
sembrada por triplicado en una placa de polipropileno de 96 pocillos y se
incubó en estufa a 37 ºC sin agitación durante 24 hs. Transcurrido el período
de incubación, se retiró el sobrenadante y se enjuagó la placa tres veces con
PBS pH 7,2. Posteriormente se dejó secar la placa a temperatura ambiente
durante 24 hs y se realizó la coloración utilizando 200µl de cristal violeta 1%
durante 3 min. Se lavó la placa hasta retirar la totalidad del colorante que
quedo sin adherirse al biofilms y se colocó una solución de alcohol/acetona
para determinar la absorbancia del colorante a 595 nm con un elisómetro
(BioRad) (Bendouah y col, 206).
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Se estudió
la presencia de biofilms en 20 pacientes por MCEL. La demostración específica de la formación de
biofilms fue por MCEL basada en la reconstrucción
tridimensional del mismo y el empleo de dos marcadores fluorescentes. En los
pacientes con pólipos nasales se observaron las bacterias unidas
irreversiblemente en la superficie del tejido de la vía aérea superior, en
forma de racimos como microcolonias y/o macrocolonias con matriz extracelular a
su alrededor. Algunas estructuras bacterianas estuvieron presentes en las
invaginaciones del tejido pero la mayoría estuvo adherida a la superficie
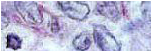
(Figura 1). En la
Figura 2 se observa un biofilm de tejido adenoideo, donde, de color rojo, por
tinción con yoduro de propidio, se ven las células bacterianas principalmente
en la base del biofilm y en verde la matriz extracelular (glucocálix) por
coloración con FITC. Los microorganismos formadores de biofilms que
pudieron ser aislados fueron: Staphylococcus aureus en cuatro pacientes;
Streptococcus viridians, en tres; Staphylococcus coagulasa
negativa y Haemophylus influenzae, en dos pacientes; Pseudomonas aeruginosa y Enterococcus
faecalis, en un paciente. También se encontraron biofilms mixtos, formados por
los complejos: Streptococcus viridians-Corinebacterium,
Streptococcus
viridiansHaemophylus influenzae, Haemophylus
influenzaeS.pneumoniae, Haemophylus influenzaeS. pyogenes, Haemophylus
influenzaeS. coagulasa negativa, Haemophylus influenzae Staphylococcus aureus, este último en dos pacientes.
Con las cepas aisladas se cuantificó la capacidad de formar biofilms in vitro por microtécnica en placas de polipropileno, coloración con cristal violeta y lectura de la DO595nm. La interpretación de resultados se realizó según la Tabla 1. El 83% de las cepas
fueron formadoras de biofilms (Positivo), con valores de DO595nm desde 0,173 hasta 4,764. Dos cepas se clasificaron como Positivas/Intermedias por estar
cercanas al punto de corte utilizado. Los pacientes 1 a 8 corresponden a
pacientes con pólipos nasales y de 9 a 20
a pacientes pediátricos, Tabla 2. En la figura 3 se muestra una comparación de distintas microscopías (ópticas, de fluorescencia y
MCEL) utilizadas para el estudio de biofilms bacterianos presentes en tejidos de la vía aérea superior. La microscopía óptica es
una técnica simple, accesible y económica en cuanto a reactivos y microscopio,
los cuales están presentes en todos los laboratorios de microbiología, pero
presenta dificultad para observar sobre todo las microcolonias del biofilms. Le
sigue la microscopía de fluorescencia, donde es más fácil la localización de
los biofilms, pero se elevan los costos para su estudio. La MCEL es la técnica
estándar de oro para el estudio de biofilms, la combinación de colorantes
fluorescentes permite el estudio diferencial de las células sésiles y de la
matriz exopolisacárida que conforman el biofilm y permite estudiar diferentes
cortes posibilitando la reconstrucción tridimensional del mismo. Sin embargo,
el elevado costo, la hace, muchas veces inaccesible para la clínica.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
En la última década, se ha
estudiado que el 99 % de las bacterias existen en la naturaleza agrupadas como
biofilms. Investigaciones recientes describen que al menos
65 % de todas las infecciones humanas de amígdalas son causadas por
biofilms bacterianos (Potera, 1999). Además, existe un porcentaje cada vez mayor de pacientes con
cuadros clínicos recurrentes de vía aérea superior con episodios de rinitis,
otitis y otras manifestaciones clínicas como hipertrofia del tejido linfoide.
Estos cuadros clínicos pueden tener relación directa con la presencia de
bacterias en forma de biofilms.
Demostrar la presencia de los
mismos en tejido de la vía aérea superior en piezas quirúrgicas de pacientes en
quienes la cirugía fue indicada tanto por infecciones recurrentes como por
patología obstructiva (hipertrofia), ayudaría a confirmar la hipótesis de que
las bacterias, protegidas de las defensas del huésped, en forma de biofilms,
continúan con su metabolismo y la producción de exotoxinas locales, lo que
favorecería la cronicidad de la respuesta inflamatoria evidenciable por los
cambios en la mucosa respiratoria. (Mladina y col 2008; Vlastarakos y col 2007). MCEL ha demostrado ser una
herramienta de gran utilidad al momento de analizar la estructura tanto de la
matriz exopolisacárida extracelular, como de las células que conforman los
biofilms inmersos en tejidos de la vía aérea superior. Con las cepas aisladas
se pudo corroborar la capacidad de las mismas de formar biofilm in vitro.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
El estudio de la presencia, la capacidad de
formar biofilms in vitro y los distintos géneros bacterianos que los forman,
aportan evidencias claves para entender la infección y colonización microbiana
en la vía aérea superior y la resistencia que muchas veces presentan a ATB de
uso clínico.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Natalia Angel Villegas es becaria doctoral de
CONICET y Julio Arce Miranda es becario doctoral de FONCyT. María Gabriela
Paraje es miembro de la carrera de Investigador de CONICET. Los autores agradecen a los Dres. Carlos Mas, María Cecilia Sampedro y
a la Bioq. Paula Icely por su excelente asistencia. Este trabajo fue subsidiado
por la Secretaría de Ciencia y Tecnología (Secyt 2008-2009).
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Bendouah Z, Barbeau J, Hamad WA, Desrosiers M. Use of an in vitro assay for determination of biofilmforming capacity of bacteria in chronic rhinosinusitis. Am J Rhinol. 2006; 20: 434438. Chole RA, Faddis BT. Anatomical evidence of microbial biofilms in tonsillar tissue. Arch Otolaryngol Head Neck Surg. 2003;124: 634-636. Chole RA, Faddis BT. Evidence for microbial biofilms in cholesteatomas. Arch Otolaryngol Head Neck Surg. 2002;128: 1129-1133. Costerton W, Veeh R, Shirtliff M, Passmore M, Post C, Ehrlich G. The applicacion of biofilm science to the study and control of chronic bacterial infections. J Clin Invest. 2003;112: 1466-77. Deighton MA, Capstick J, Domalewski E, Van Nguyen Trung. Methods for Studying Biofilms Produced by Staphylococcus epidermidis. In: Doyle RJ, editor. Methods in enzymology. Vol 336. San Diego (California): Academic Press. 2001; p177-95. Flemming HC, New TR, Wozmak DJ. The EPS matrix: the house of Biofilm cells. J Bacteriol 189: 7945- 7947; 2007. Mladina R, Poje G, Vuković K, Ristić M, Musić S. Biofilm in nasal polyps. Rhinology. 2008 Dec;46(4):302-7. O`Toole G, Kolter R. Flagellar and twitching motility are necessary for P.aeruginosa biofilm development. Mol Microbiol. 30(2):295-304, 1998. Palmer James N. Bacterial Biofilms: Do they play a role in chronic sinusitis?. Otolaryngology Clinics of North America. 2005;1193-1201. Post JC, Stoodley P, Hall-Stoodley L, Ehrlich GD. The role of biofilms in otolaryngologic infections. Curr Opin Otolaryngol Head Neck Surg. 2004;12 (3): 185-90. Potera C. Forging a link between biofilm and disease. Science 283: 1837-1839; 1999. Psaltis AJ, Ha KR, Beule AG, Tan LW, Wormald PJ. Confocal scanning laser microscopy evidence of biofilms in patients with chronic rhinosinusitis. Laryngoscope. 2007;117(7):1302-6. Sanclement JA, Webster P, Thomas J et al. Bacterial biofilms in surgical specimens of patients with chronic rhinosinusitis. Laryngoscope. 2005;115(4):578-82. Stoodley, P, Costerton, J. Biofilm as complex differentiated communities. Annu. Rev. Microbiol. 2002; 56: 187 209. Vlastarakos PV, Nikolopoulos TP, Maragoudakis P, Tzagaroulakis A, Ferekidis E. Biofilm in ear, nose and throat infections: how important are they? The Laryngoscope 117: 668-673; 2007. Vuong C, Kocianova S, Voyich JM, Yao Y, Fischer ER, Deleo FR et al. A crucial role for exopolysaccharide modification in bacterial biofilm formation, immune evasion, and virulence. J Biol Chem. 2004. 24;279(52):54881-6.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
- Rafael Martínez Girón - ESPAÑA (15/11/2009 15:30:55)
- MARIA GABRIELA PARAJE - ARGENTINA (16/11/2009 4:12:33)
- José Víctor Bolarín Lucas - ESPAÑA (18/11/2009 10:36:39)
- MARIA GABRIELA PARAJE - ARGENTINA (28/11/2009 4:46:01)
- José Luis Arce Diego - ESPAÑA (29/11/2009 19:52:14)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 11:37:37



