
ISBN: 978-84-692-76778
 PONENCIAS
PONENCIAS
Nº 1801. Citopatología
|
Punción Aspiración con AgujaFina (PAAF) en el diagnóstico de los tumores de los tejidos blandos Ricardo González Cámpora[1] |
|
citalopram alcohol nhscitalopram and alcohol overdoseResumen
Los tumores de los tejidos blandos constituyen un grupo heterogéneo de lesiones que presentan grandes dificultades diagnósticas, principalmente relacionadas con la baja incidencia de lesiones malignas y la existencia de cuadros morfológicos que no se ajuntan bien a los criterios clásicos de comportamiento biológico. Estas dificultades se suman a la responsabilidad que conlleva un diagnóstico que implica terapia radical o quimioterapia selectiva. En la actualidad, las biopsias a cielo abierto se vienen sustituyendo por procedimientos menos invasivos como la BAG y la PAAF. Al contrario de lo que sucede en otros órganos, como el tiroides o la piel, la PAAF en los tejidos blandos tiene escasa aceptación como método diagnóstico; sin embargo, los estudios de rentabilidad diagnóstica no señalan diferencias significativas en la indicación de benignidad vs. malignidad, cuando se compara con BAG y PAAF. En la actualidad existen criterios citológicos suficientes para emitir con garantía diagnósticos precisos en una gran variedad de lesiones primarias. El diagnóstico citológico, al igual que el histológico descansa en una estrecha correlación entre la morfología, la clínica y los estudios de imagen. Nosotros consideramos que teniendo en cuanta el gran número de lesiones primarias que existen en los tejidos blandos, el método de aproximación morfológica debe comenzar por un análisis de los patrones celulares, con el fin de ir delimitando las lesiones; en este sentido, nosotros clasificamos a las lesiones en una de los siguientes patrones: ricos en matriz mixoide, células redondas, células fusiformes, células poligonales, células pleomorfas y células bien diferenciadas. Posteriormente la búsqueda de hallazgos citológicos específicos, la correlación con la clínica y los estudios de imagen nos permitirán determinar, por un lado, la benignidad o el grado de malignidad y, en muchas ocasiones, también, el diagnóstico histogenético. En las lesiones ricas en células redondas, células fusiformes, células pleomorfas y células poligonales, los estudios de inmunohistoquímica, microscopía electrónica y de FISH pueden ser de gran ayuda. A lo largo de la exposición se señalarán los hallazgos citológicos de mayor interés diagnóstico con las posibles indicaciones de estudios especiales. Introducción
Los tumores de partes blandas constituyen un grupo muy heterogéneo de lesiones que se clasifican en base a criterios histogenéticos en 14 grandes categorías (figura 1). En cada una de ellas se incluyen lesiones benignas y malignas, aunque en algunos grupos también se incluyen lesiones de malignidad intermedia. En total, se consideran aproximadamente 51 lesiones benignas, 19 de malignidad intermedia y 32 sarcomas. Las lesiones benignas son muy frecuentes, mientras que los sarcomas son muy poco comunes. La proporción aproximada entre unos y otros es de 100/1. Para que nos hagamos una idea de la rareza de los sarcomas, la figura 2 muestra la frecuencia de los tipos principales de tumores malignos en función del órgano o tejido; por cada diagnóstico de sarcoma de partes blandas se realizan 20 de carcinomas de pulmón o 15 de colon-recto. En los protocolos diagnósticos de los tumores de tejidos blandos, en principio, se pueden utilizar cuatro procedimientos diferentes para la obtención del material (figura 3). La biopsia escisional se lleva a cabo en lesiones pequeñas, generalmente superficiales, y siempre con un pequeño margen de tejido sano. La biopsia incisional es una de las más usadas pero también de las más discutidas en vistas de una cirugía conservadora posterior, particularmente de miembros. Con estos dos procedimientos se obtiene suficiente material para realizar también estudios especiales. En la actualidad la biopsia incisional tiende a ser sustituida por la biopsia con aguja gruesa, puesto que con esta también se obtienen suficiente material. Sin embargo, esto nos parece una simplificación excesiva y con escaso fundamento, ya que las publicaciones sobre rentabilidad diagnóstica señalan que la PAAF es inferior a la BAG sólo en el tipaje histológico, no en la distinción entre lesiones benignas y malignas. Se han señalado como desventajas principales de la PAAF , en relación con la BAG, la escasez de material en los aspirados, que impide la realización de técnicas especiales, y la disociación celular, que no permite el reconocimiento de patrones arquitecturales. Pero estos inconvenientes tienen una importancia muy relativa, ya que mediante la PAAF con frecuencia se obtienen fragmentos tisulares que conservan la organización arquitectural, y los aspirados pueden concentrarse formando bloques celulares para realizar estudios inmunohistoquímicos; además, como el procedimiento es rápido y no causa molestias excesivas, se pueden realizar aspiraciones adicionales para estudios moleculares, citogenéticos o de citometría. A pesar de las reticencias señaladas al uso de la PAAF en el diagnóstico de los tumores de los tejidos blandos, el número de publicaciones no para de ir en aumento desde los años 80 y, en la actualidad, se dispone de criterios citológicos bien definidos que permiten el diagnóstico correcto en un gran número de las lesiones benignas y malignas (figura 5). Por otro lado, hay que tener en cuenta que la mayoría de las lesiones de los tejidos blandos son tumores benignos o metástasis de carcinomas y melanomas y que, salvo casos muy concretos (tumores infantiles y algunos pocos tumores del adulto), el tratamiento quirúrgico está en función, más que del tipo histológico de la lesión, de su localización anatómica y del grado de malignidad tumoral. Por tanto, la decisión terapéutica final no descansa exclusivamente en el diagnóstico histológico sino en una correlación estrecha de datos clínicos, radiológicos y morfológicos. Nosotros consideramos que la PAAF es un método extremadamente útil en el diagnóstico de los tumores de los tejidos blandos que debe ser utilizada en el estudio inicial de todas las lesiones superficiales (benignas y malignas), ya que por su eficacia y rapidez permite obtener en muy poco tiempo una idea bastante fidedigna de la naturaleza de la lesión y, por tanto, planificar racionalmente la siguiente actuación. En las lesiones profundas y en los tumores infantiles, es aconsejable el uso de la BAG, conjuntamente con el de la PAAF, - o, en su defecto, con un extendido citológico procedente del cilindro - ya que ambos métodos proporcionan información complementaria (los detalles nucleares se ven mejor en las extensiones, mientras que la organización arquitectural es más patente en los cortes tisulares). La BAG puede utilizarse también en aquellos casos en que los aspirados citológicos no han sido diagnósticos, por la dificultad en obtener células o porque el material aspirado no muestre signos concluyentes. En la figura 6 se recoge el procedimiento diagnóstico en función de la sospecha clínica y localización del tumor y como debe distribuirse el material para el estudio completo del tumor. Las figuras 7 y 8 recogen los aspectos más sobresalientes de la PAAF (detalles citoplásmicos y nucleares y matriz) y de la BAG (organización arquitectural y disponibilidad para técnicas especiales). Aunque hay un número considerable de publicaciones sobre criterios citológicos diagnósticos, son muy escasos los trabajos sobre la precisión diagnóstica del procedimiento. La serie más amplia es la recogida por Akerman y Willén en 1985, que incluye a un total de 517 tumores: 315 benignos y 202 sarcomas de extremidades y tronco. En ella se obtuvieron los siguientes parámetros: - Falso diagnósticos: 5% (falsos positivos 2,5% y falsos negativos 2,5%) - Material insuficiente: 6%. Más comunes en lesiones benignas que malignas. - Diagnóstico no conclusivo: 3% - Diagnóstico correcto (benigno vs. maligno) 94% Aproximación al diagnóstico citológico En principio, se siguen las mismas pautas que en el diagnóstico histológico, tratando de integrar los hallazgos clínicos con los morfológicos (figura 9). La primera actuación es encuadrar el extendido dentro de 5 patrones básicos que vienen definidos por la morfología celular o las características del estroma; de este modo dirigimos nuestra atención a una serie más concreta de lesiones. Posteriormente, buscamos hallazgos citológicos o arquitecturales que nos permitan orientar un poco más la lesión, tales como tipos específicos de células, estructuras organoides, detalles citológicos o nucleares o bien identificación de un segundo tipo celular, mediante este ejercicio vamos reduciendo de modo considerable las posibilidades diagnósticas. Por último, nos fijamos en los datos clínicos y radiológicos. Hay que tener en consideración que si bien existen normas generales que orientan hacia la benignidad o malignidad de una proceso existen numerosas excepciones a las reglas. Por ejemplo, los tumores profundos suelen ser malignos pero hay algunos como el lipoma, el mixoma intramuscular o el schwannoma que son benignos y, viceversa, hay lesiones malignas o de malignidad intermedia que son superficiales, tales como el mixofibrosarcoma y el dermatofibrosarcoma protuberans. Por otro lado, también hay excepciones a la forma de crecimiento tumoral; en general se considera que los tumores malignos crecen rápidamente y que los benignos lo hacen lentamente pero la fascitis nodular crece rápidamente y puede ser dolorosa y el sarcoma epiteliode o alveolar lo hace lentamente y durante años. Las técnicas especiales no siempre son necesarias; tienen muy poca utilidad en el diagnóstico de los tumores ricos en matriz mixoide pero mucha en los tumores de células redondas, fusiformes y poligonales (figura 10).
|
||
|
|
Tumores ricos en matriz mixoide En figura 11 se recogen las características de la matriz mixoide con la técnica del PAP y del Giemsa. Con el PAP suele tener una coloración verdosa muy tenue mientras que con el Giemsa toma una coloración violeta-azul, la intensidad del violeta varía en función del contenido de radicales sulfatos y es muy intensa en las lesiones con matriz condroide o cordoide. En la figura 12 se relacionan las lesiones benignas y malignas mejor caracterizadas mediante la PAAF y en la figura 13 los hallazgos citológicos más relevantes. En la evaluación de estas lesiones tres aspectos son especialmente relevantes; características de la matriz mixoide, tipo de celularidad y vascularización. La mayoría de las lesiones están compuestas por células fusiformes pero en algunas nos podemos encontrar otra celularidad que nos ayuda mucho a orientar el diagnóstico; por ejemplo, la presencia lipoblastos es característica del liposarcoma mixoide o del lipoblastoma (figura 14), las células ganglionares nos sugiere un proceso reactivo miofibroblástico, como puede ser la fascitis nodular o la miosistis proliferativa (figura 15). La existencia de células estrelladas o triangulares sin atipia en un extendido hipocelular es muy sugestiva de mixoma intramuscular (figura 16) y la presencia de células fusiformes con o sin células poligonales sin atipia es propia del condrosarcoma mixoide (figura 17). En cambio, la existencia de estas células pero con atipia nos sugiere un mixofibrosarcoma (figura 18). Las características de la matriz son hallazgos complementarios importantes, por ejemplo la existencia de metacromasia intensa nos sugiere un condrosarcoma mixoide (figura 17) mientras que la de una matriz pálida y granular un mixoma (figura 16) o un mixofibrosarcoma (figura 18). La trama vascular es otro hallazgo importante en el diagnóstico de los tumores mixoides. En el liposarcoma mixoide la vascularización es de tipo plexiforme (figura 19), en el mixofibrosarcoma los vasos aparecen engrosados y curvilíneos (figura 20) y en el mixoma intramuscular (figura 16), condrosarcoma mixoide extraesquelético (figura 17) prácticamente están ausentes o son muy poco relevantes. El diagnóstico diferencial de los tumores mixoides incluye carcinomas y melanomas metastásicos y, sobretodo, afectación de partes blandas por condrosarcomas y cordomas.
|
|
|
|
Los tumores de células redondas constituyen unos de los grupos más problemáticos porque son lesiones malignas, de gran agresividad, que se presentan preferentemente en la infancia y en la adolescencia y en la mayoría de las ocasiones necesitan quimioterapia adyuvante, por lo que el diagnóstico debe ser bastante preciso. Los aspirados suelen ser bastante celulares, como el que aparece en la figura 21. En la figura 22 se relacionan las entidades más características y en la 23 los hallazgos citológicos que permiten orientar el diagnóstico. La población celular puede ser monomorfa, polimorfa o puede contener otras estirpes celulares. En el primero de los casos, tres lesiones hay que tener en consideración: el tumor desmoplásico de células redondas, el tumor de Ewing/neuroepitelioma periférico y el sarcoma sinovial poco diferenciado. En el tumor desmoplásico de células redondas las células carecen de ningún distintivo morfológico y solo las características clínicas (localización y edad del paciente) y la presencia de colágeno podrían orientarnos el diagnóstico. En el tumor de Ewing/neuroepitelioma periférico las células con frecuencia presentan vacuolas citoplásmicas de glucógeno PAS+ (figura 24); aunque no son diagnósticas ( también se encuentran en rabdomioblastos y neuroblastos) su presencia en un extendido monomorfo de células redondas, conjuntamente con las características clínicas (edad y localización) nos pueden orientar mucho el diagnóstico citológico; por último, en el sarcoma sinovial poco diferenciado el monomorfismo celular a veces se encuentra alterado por la presencia de células con citoplasma rabdoide. En la diferenciación de estos tres tipos de lesiones la inmunohistoquímica y la biología molecular son de extraordinaria utilidad (figura 25). En los tumores con celularidad polimorfa hay que buscar signos específicos de diferenciación, tales como rabdomioblastos o neuroblastos. La lesión muscular de células redondas más característica es el rabdomiosarcoma alveolar/sólido. En los extendidos de estas lesiones predominan las células redondas con escasos citoplasma, a veces vacuolado, pero también se observan rabdomioblastos y células multinucleadas (figura 26). Los rabdomioblastos presentan citoplasma denso polarizado y núcleos con cromatina grumosa; con frecuencia entre estas células se observan células multinucleadas grandes y con núcleos en disposición periférica (figura 27). Las técnicas de inmunohistoquímica y de biología molecular son muy útiles a la hora de clasificar correctamente a la lesión (figura 28). Los neuroblastos se observan en los neuroblastomas y ganglioneuroblastomas y son células que también muestran polarización citoplásmica pero los núcleos, a diferencia de los del rabdomioblasto, contienen cromatina fina y gruesa en forma de sal y pimienta (figura 29). Un hallazgo característico de estas células es la presencia de prolongaciones citoplásmicas fina que forman una trama fibrilar intersticial bastante llamativa (figura 29). Los neuroblastos con diferenciación máxima reciben el nombre de células ganglionares y tienen forma esférica, núcleo marginado y nucléolo prominente (figura 29). Estas células se observan en los neuroblastomas bien diferenciados, ganglioneuroblastomas y gsanglioneuromas. Las rosetas neuroblásticas son características de los neuroblastomas bien diferenciados y ganglioneuroblastomas (figura 30) pero también pueden observarse en el sarcoma de Ewing/neuroepielioma periférico (figura 31). Por último, los tumores con componentes heterólogos son excepcionales; y este puede ser en forma de nidos de cartílago, como sucede en el condrosarcoma mesenquimal o bien en forma de células poligonales con pigmento melánico, como se observa en el progonoma melanótico (figura 32).
En la figura 33 se señalan las entidades con las que hay que establecer el diagnóstico diferencial en función de la edad del paciente.
|
|
|
|
Los tumores de células fusiformes constituyen un grupo ciertamente conflictivo puesto que es el más numeroso y el que menos signos de diferenciación celular presenta. Además, en muchas ocasiones no es posible determinar el carácter benigno o maligno de la lesión. En la figura 34 se muestran un extendido característico de células fusiformes con tendencia a formar haces compactos en el seno de una fondo hemorrágico. Las lesiones de células fusiformes más comunes y mejor caracterizadas aparecen recogidas en la figura 35. En esta categoría lesional son muy importantes los detalles nucleares, las características citoplásmicas y los patrones arquitecturales (figura 36) La forma nuclear puede ser muy orientadora. Los núcleos elongados con extremos romos son muy característicos de las lesiones de músculo liso (figura 37); en cambio, los núcleos con un extremo afilado, ondulados, en anzuelo o doblados como en hebilla lo son de las lesiones neurales (figura 38). En estas, a veces, se encuentran empalizadas nucleares que alternan con matriz fibrilar que reciben el nombre de cuerpos de Verocay (figura 39). En los tumores del estroma gastroitestinal los núcleos pueden presentar una morfología mixta. El diagnóstico de estas lesiones descansa principalmente en la correlación clínicopatológica y en la demostración mediante técnicas de inmunohistoquímica de reacción positiva al CD117 (KIT) (figura 40). Los núcleos ovales o redondos en células elongadas son propios del sarcoma sinovial, pero este diagnóstico solo es posible realizarlo si se encuentra un componente bifásico acompañante (figura 41) o bien se demuestra con técnicas de IHQ la expresión de CK o de biología molecular con la traslocación t(X;18) (figura 42). Los detalles citoplásmicos suelen ser poco relevantes; en la mayoría de las ocasiones los citoplasmas son escasos o bien aparecen tumefactos; en estas últimas situaciones suele tratarse de lesiones miofibroblásticas (figura 15 y 43). La presencia de remolinos en lesiones superficiales es bastante sugerente de DFSP. Por último un citoplasma amplio en forma de cinta o renacuajo es muy característico del rabdomiosarcoma embrionario (figura 44).. El diagnóstico diferencial de estas lesiones hay que establecerlo principalmente con las metástasis del melanoma fusocelular puesto que con frecuenta se presentan de modo imprevisto, incluso varios años después de la extirpación de un primario. El diagnóstico descansa en la correlación anatomoclínica y ne la demostración de inmunoreactividad difusa a marcadores melanocíticos (S-100, HMB-45 y melan A).
|
|
|
|
Por lo general, los tumores de células pleomórficas son lesiones agresivas, propias de adultos mayores que muestran marcado pleomorfismo celular, frecuentes mitosis y un fondo necrótico (figura 45). Pero no debemos olvidar que ciertas lesiones benignas, tales como el lipoma pleomórfico y otras, pueden presentar también células gigantes bizarras. En la figura 46 se recogen las lesiones con células pleomorfos. De todas ellas, las más frecuente es el fibrohistiocitoma maligno pleomorfo. En estas lesiones a veces se pueden encontrar hallazgos citoplásmicos que nos permiten orientar el diagnóstico (figura 47). Así, la presencia de lipoblastos orienta hacia LPS, la de rabdomioblasto o leiomioblasto a RMS y LMS, y la de osteoide a OS. Cuando no encontramos signos citoplásmicos específicos denominamos la lesión FHM. La forma más común es la denominada pleomórfica-estoriforme que se caracteriza por la presencia de remolinos centrados por un vaso (figura 48). Además de esta forma también se pueden identificar la variante mixoide o mixofibrosarcoma y la de células gigantes (figura 49). El diagnóstico diferencial de este tipo de lesiones hay que establecerlo con metástasis de carcinomas pleomorfos, melanomas y linfomas, particularmente si asientan en el RP.
|
|
|
|
Tumores de células poligonales tipo epitelioide
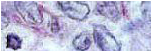
Esta categoría tumoral frecuentemente se confunde con metástasis de carcinomas o de melanomas. Suelen ser lesiones monomorfas, con tendencia a formar grupos celulares con poco cohesión (figura 50), que se presentan por lo general en personas jóvenes- edad media con crecimiento lento. En la figura 51 se recogen las lesiones más comunes de esta categoría y en la figura 52 los hallazgos citológicos más relevantes. Por ejemplo, los citoplasmas pueden ser granulares, densos o claros y vacuolados. Las vacuolas a su vez pueden ser groseras o finas. Las groseras se observan en los tumores de células granulares (figura 53). Estas células tienen marcada fragilidad de tal forma que el contenido aparece desparramado por el fondo del extendido. Las granulaciones finas, por el contrario son más propias del sarcoma alveolar; en esta lesión, la presencia de inclusiones cristalinas PAS positiva son de gran ayuda a la hora de emitir el diagnóstico definitivo (figura 54). Por otro lado, los citoplasmas claros o vacuolados son muy propios de los paragangliomas (figura 55) y de los sarcomas de células claras (figura 56). En ocasiones se pueden encontrar vacuolas citoplásmicas que nos pueden orientar el diagnóstico hacia un tumor adenomatoide (figura 57) o bien un hemangioendoteliolma epitelioide. Por último, los citoplasmas también pueden ser densos y sin ningún detalle adicional, esto es lo que se observa por ejemplo en el sarcoma epiteliode (figura 58) y, a veces en los paragangliomas y sarcomas de células claras. En lo referente al núcleo también hay algunos detalles importantes: Por ejemplo núcleos con nucleolos pequeños se observan en los tumores de células granulares (figura 53); en cambio, el nucléolo es bastante prominente en el sarcoma alveolar (figura 54), sarcoma de células claras (figura 56) y sarcoma epiteliode (figura 58). En los paragangliomas es muy característica la existencia de anisocariosis marcada (figura 55) y en estos y en los sarcomas de células claras (figura 56) se pueden sorprender inclusiones citoplásmicas nucleares.
|
|
|
|
Tumores de células bien diferenciadas
En esta categoría incluimos a lesiones bien diferenciadas compuestas por células maduras, tales como lipocitos, rabdomiocitos, leioliocitos, células meníngeas, o células cartilaginosas (figura 59). El grupo más importante por su frecuencia es el de los tumores lipomatosos. Resulta imposible diferenciar el aspirado de un lipoma del de la hipodermis, por lo que el dato de masa es importante para el diagnóstico (figura 60). Las lesiones adiposas de mayor interés actual por su frecuencia son los LPS bien diferenciados que pueden asentar tanto en EE como tronco y RP. En citología es posible realizar una aproximación en un número importante de casos, incluidas las formas desdiferenciadas (figura 61). 
Figura 59
|
|
|
|
Referencias seleccionadas:
Åkerman M, Willen H: Critical review on the role of fine needle aspiration in soft tissue tumors. Pathol Case Rev 1998;3:111117 Akhtar M, Iqbal MA, Mourad W, Ali MA: Fine-needle aspiration biopsy diagnosis of small round cell tumors of childhood: A comprehensive approach. Diagn Cytopathol 1999;21:8191 Bennert KW, Abdul-Karim FW: Fine needle aspiration cytology vs. needle core biopsy of soft tissue tumors. A comparison. Acta Cytol. 1994; 38:381384. Costa MJ, Campman SC, Davis RL, Howell LP: Fine-needle aspiration cytology of sarcoma: retrospective review of diagnostic utility and specificity. Diagn Cytopathol. 1996;15:2332. Domansky HA: Fine needle aspiration cytology of soft tissue lesions: diagnostic chalanges. Diagn Cytoplathol 2007;35:768-773. Domansky HA, Akerman M, Carlén B, Engellau J, Gustafson P, Jonsson K, Mertens F, Rydholm A: Core-needle biopsy performed by the cytopathologist. Cancer Cytopathol 2005;105:229-239. Domanski HA, Akerman M, Engellau J, Gustafson P, Mertens F, Rydholm A: Fine-needle aspiration of neurilemoma (schwannoma). A clinicocytopathologic study of 116 patients. Diagn Cytopathol. 2006;34:403-412. Domanski HA, Carlen B, Jonsson K, Mertens F, Akerman M: Distinct cytologic features of spindle cell lipoma. A cytologic-histologic study with clinical, radiologic, electron microscopic, and cytogenetic correlations. Cancer 2001;93:381-389. Geisinger KR, Abdul-Karim FW: Fine needle aspiration biopsies of soft tissue tumors. In: Weiss SW, Goldblum JR, eds. Enzinger and Weisss Soft Tissue Tumors. 5ª ed. Saint Louis: Mosby; 2008:103-118. González-Cámpora R: Fine needle aspiration cytology of soft tissue tumors. Acta Cytologica 200;44:337-344 González-Cámpora R: Cytoarchitectural findings in the diagnosis of primary soft tissue tumors. Acta Cytol. 2001;45:115-146 González-Cámpora R, Muñoz-Arias G, Otal-Salaverri C, Jorda-Heras M, García-Alvarez E, Gomez-Pascual A, Garrido-Cintado A, Hevia-Vázquez A, Sánchez-Gallego F, Galera-Davidson H: Fine needle aspiration cytology of primary soft tissue tumors. Morphologic analysis of the most frequent types. Acta Cytol. 1992;36:905-917 González-Cámpora R, Otal-Salaverri C, Hevia-Vázquez A, Muñoz-Muñoz G, Garrido-Cintado A, Galera-Davidson H: Fine needle aspiration in myxoid tumors of the soft tissues. Acta Cytol. 1990;34:179-191. González-Cámpora R, Otal-Salaverri C, Panea-Flores P, Lerma-Puertas E, Galera-Davidson H: Fine needle aspiration cytology of paraganglionic tumors. Acta Cytol. 1988;32:386-390 Gonzalez-Cámpora R, Ríos-Martín JJ, Solórzano-Amoretti A, Vargas de los Monteros MT, Trigo-Sánchez I, Otal-Salaverri C, Galera-Davidson H: Fine needle aspiration cytology of an acral myxoinflammatory fibroblastic sarcoma: case report with cytological and cytogenetic findings.Cytopathology. 2008 ;19:118-123. González-Cámpora R, Salas Herrero E, Otal-Salaverri C Villar-Rodriguez JL, San Martín Díez V, Hevia Vazquez A, Galera Davidson H: Diffuse tenosynovial giant cell tumor of soft tissues. Report of a case with cytologic and cytogenetic findings. Acta Cytol. 1995;39:770-776 Kilpatrick SE: Histologic prognostication in soft tissue sarcomas: grading versus subtyping or both? A comprehensive review of the literature with proposed practical guidelines. Ann Diagn Pathol. 1999;3:4861. Kilpatrick SE, Bergman S, Pettenati MJ, Gulley ML: The usefulness of cytogenetic analysis in fine needle aspirates for the histologic subtyping of sarcomas. Mod Pathol. 2006;19:815-819. Kilpatrick SE, Cappellari JO, Bos GD, Gold SH, Ward WG: Is fine needle aspiration biopsy a practical alternative to open biopsy for the primary diagnosis of sarcoma? Experience with 140 patients. Am J Clin Pathol 2001;115:59-68 Kilpatrick SE, Doyon J, Choong PFM, Chong PF, Sim FH, Nascimento AG: The clinicopathologic spectrum of myxoid and round cell liposarcoma: A study of 95 cases. Cancer 1996;77:14501458 Kilpatrick SE, Geisinger KR: Soft tissue sarcomas: the usefulness and limitations of fine-needle aspiration biopsy. Am J Clin Pathol. 1998;110:5068. Kilpatrick SE, Renner JB, Creager A: Diagnostic musculoskeletal surgical pathology. Clinicopathologic and cytologic correlations. Saunders. 2004. Kilpatrick SE, Teot LA, Stanley MW, Ward WG, Savage PD, Geisinger KR: Fine needle aspiration biopsy of synovial sarcoma: A cytomorphologic analysis of primary, recurrent, and metastatic tumors. Am J Clin Pathol 1996;106:769775 Kilpatrick SE, Ward WG: Myxofibrosarcoma of soft tissues: cytomorphologic analysis of a series. Diagn Cytopathol. 1999;20:69. Kilpatrick SE, Ward WG, Bos GD: The value of fine-needle aspiration biopsy in the differential diagnosis of adult myxoid sarcoma. Cancer.2000;90:167177. Kilpatrick SE, Ward WG, Cappellari JO, Bos GD: Fine-needle aspiration biopsy of soft tissue sarcomas. A cytomorphologic analysis with emphasis on histologic subtyping, grading, and therapeutic significance. Am J Clin Pathol. 1999;112:179188. Kilpatrick SE, Ward WG, Chauvenet AR, Pettenati MJ: The role of fine-needle aspiration biopsy in the initial diagnosis of pediatric bone and soft tissue tumors: an institutional experience. Mod Pathol. 1998;11:923928. Layfield LJ, Liu K, Dodge RK: Logistic regression analysis of myxoid sarcomas: A cytologic study. Diagn Cytopathol 1998;19:355360 Layfield LJ, Liu K, Dodge RK: Logistic regression analysis of small round cell neoplasms: A cytologic study. Diagn Cytopathol 1999;20:271277 Layfield LJ, Moffatt EJ, Dodd LG, Scully SP, Harrelson JM: Cytologic findings in tenosynovial giant cell tumors investigated by fine-needle aspiration cytology. Diagn Cytopathol 1997;16:317325 Layfield LJ, Mooney EE, Dodd LG: Not by blood alone: Diagnosis of hemangiomas by fine-needle aspiration. Diagn Cytopathol 1998;19:250254 Layfield LJ, Anders KH, Glasgow BJ, Mirra JM: Fine-needle aspiration of primary soft-tissue lesions. Arch Pathol Lab Med 1986;110:420-424. Liu K, Dodge RK, Dodd LG, Layfield L: Logistic regression analysis of high grade spindle cell lesions. Acta Cytol 1999;43:143152 Liu K, Layfield LJ, Coogan AC, Ball MS, Bentz JS, Dodge RK: Diagnostic accuracy in fine-needle aspiration of soft tissue and bone lesions. Influence of clinical history and experience. Am J Clin Pathol. 1999;111:632640. Miralles T, Gosalbez F, Menendez P, Astudillo A, Torre C, Buesa J: Fine needle aspiration cytology of soft-tissue lesions. Acta Cytol 1986; 30:671-677. Nordgren H, Akerman M: Electron microscopy of fine needle aspiration biopsy from soft tissue tumors. Acta Cytol 1982;26:179-188. Seidal T, Walaas L, Kindblom L-G, Angervall L: Cytology of embryonal rhabdomyosarcoma: A cytologic, light microscopic, electron microscopic, and immunocytochemical study of seven cases. Diagn Cytopathol 1988;4:292299 Wakely PE Jr: Myxomatous soft tissue tumors: correlation of cytopathology and histopathology. Ann Diagn Pathol. 1999;3:227242. Wakely PE Jr: Epitheliod /granular soft tisuue lesions: correlation of cytopathology and histopathology. Annal Diagn Pathol 2000; 4: 316-328. Wakely PE, Frable WJ: Fine-needle aspiration biopsy cytology of giant-cell tumor of tendon sheath. Am J Clin Pathol 1994;102:8790 Wakely PE, Geisinger KR, Cappellari JO, Silverman JF, Frable WJ: Fine needle aspiration cytopathology of soft tissue: Chondromyxoid and myxoid lesions. Diagn Cytopathol 1995;12:101105 Wakely PE Jr, Kneisl JS: Soft tissue aspiration cytopathology. Cancer. 2000;90: 292298. Walaas L, Angervall L, Hagmar RB, Save-Soderbergh J: A correlative cytologic and histologic study of malignant fibrous histiocytoma: An analysis of 40 cases examined by fine needle aspiration cytology. Diagn Cytopathol 1986;2:4654 Walaas L, Kindblom L-G: Lipomatous tumors: A correlative cytologic and histologic study of 27 tumors examined by fine needle aspiration cytology. Hum Pathol 1985;16:618 Walaas L, Kindblom L-G: Fine needle aspiration biopsy in the preoperative diagnosis of chordoma. Hum Pathol 1991;22:2228 Walaas L, Kindblom L-G, Gunterberg B, Bergh P: Light and electron microscopic examination of fine-needle aspirates in the preoperative diagnosis of cartilaginous tumors.Diagn Cytopathol 1990;6:396408 Weiss SW, Goldblum JR: Enzinger & Weiss´s sSoft Tissue Tumors, 5ª ed. St Louis, Mosby, 2008
|
|
|
|
- JOSE MELLADO SORIA - ESPAÑA (02/11/2009 0:07:48)
- Rafael Escalona Veloz - CUBA (03/11/2009 1:19:08)
- TERESA PEREDA SALGUERO - ESPAÑA (03/11/2009 18:43:52)
- SONIA PERALES - ESPAÑA (03/11/2009 23:18:07)
- Juan Jaime Borlando Rojas - CHILE (04/11/2009 3:02:51)
- CARMEN LÓPEZ PEÑA - ESPAÑA (04/11/2009 10:03:46)
- BEATRIZ EIZAGUIRRE - ESPAÑA (04/11/2009 12:37:59)
- EDUARDO ORTIZ RUIZ - ESPAÑA (04/11/2009 14:39:29)
- María de los Angeles Martín Suárez - CUBA (05/11/2009 16:21:39)
- JOSE LUIS CARRASCO - ESPAÑA (06/11/2009 9:30:33)
- Francisco Javier Velasco Albendea - ESPAÑA (07/11/2009 12:52:49)
- Francisco Javier Velasco Albendea - ESPAÑA (07/11/2009 12:59:10)
- maria carmen martin corriente - ESPAÑA (08/11/2009 13:08:57)
- Elena Santos Fuertes - ESPAÑA (10/11/2009 21:53:51)
- Ana Cecilia Matilde Casas Del Ben - PERU (11/11/2009 1:07:09)
- IGNACIO J. CLAROS GONZÁLEZ - ESPAÑA (11/11/2009 13:47:39)
- Ricardo González Cámpora - ESPAÑA (Autor) (12/11/2009 12:13:01)
- CONCEPCION LARA BOHORQUEZ - ESPAÑA (12/11/2009 18:38:48)
- YOLANDA LAPLAZA JIMENEZ - ESPAÑA (12/11/2009 22:01:38)
- MARIO CASTILLO GUTIÈRREZ - MEJICO (13/11/2009 4:31:57)
- YARITZA CASTELLANO - VENEZUELA (14/11/2009 15:12:22)
- IGNACIO J. CLAROS GONZÁLEZ - ESPAÑA (14/11/2009 16:20:24)
- BEGOÑA SANROMAN BUDIÑO - ESPAÑA (14/11/2009 16:34:05)
- MARIA SOLEDAD LOPEZ GOMEZ - ESPAÑA (14/11/2009 19:00:08)
- Ana Maria Toledo Araujo - ESPAÑA (14/11/2009 19:40:18)
- Josefa Dolores Miranda Tarragó - CUBA (15/11/2009 5:16:36)
- Alejandro Antúnez Infante - ESPAÑA (15/11/2009 21:47:03)
- FRANCISCO JAVIER FLORES - MEJICO (17/11/2009 2:56:11)
- Laura Lopez Marin - CUBA (17/11/2009 20:45:05)
- Isidro Machado - ESPAÑA (18/11/2009 14:12:09)
- Emilio Mayayo Artal - ESPAÑA (19/11/2009 14:05:56)
- Alfredo Basilio Quiñones Ceballos - CUBA (20/11/2009 21:11:58)
- Felipe Gustavo Junchaya Aparcana - PERU (20/11/2009 22:03:25)
- Mª Flora Tarrero Carrera - ESPAÑA (21/11/2009 8:46:09)
- SONIA MOLINA RIAÑO - ESPAÑA (21/11/2009 10:41:29)
- ANA ISABEL JIMENEZ SANCHEZ - ESPAÑA (21/11/2009 17:57:57)
- Ernesto Garcia-Ureta - ESPAÑA (22/11/2009 20:19:46)
- Edith Monielyck Mendonça Batista - BRASIL (24/11/2009 22:02:02)
- Rafael Esteban Carvia Ponsaillé - ESPAÑA (25/11/2009 19:26:24)
- ELENA ALMUDÉVAR BERCERO - ESPAÑA (25/11/2009 19:42:22)
- OLGA GARCIA-VIDAL - ESPAÑA (25/11/2009 20:00:30)
- Lissette Sixto Cordero - CUBA (25/11/2009 22:11:57)
- Luisa Mª Díaz Ruiz - ESPAÑA (26/11/2009 0:16:55)
- Mª Teresa Mosquera Martínez - ESPAÑA (26/11/2009 11:56:26)
- JUANA ISABEL CID MAÑAS - ESPAÑA (26/11/2009 18:38:26)
- SORKUNDE BERGARA ELORZA - ESPAÑA (27/11/2009 8:01:01)
- Carlos Vidal Puga - ESPAÑA (27/11/2009 21:14:55)
- MARIA DEL CARMEN GOMEZ MATEO - ESPAÑA (27/11/2009 22:48:30)
- Raimy Márquez Pedraza - CUBA (29/11/2009 1:46:33)
- RAFAEL ALEJANDRO PÉREZ ÉCIJA - ESPAÑA (29/11/2009 13:12:18)
- Susana Hernandez Delgado - CUBA (29/11/2009 19:01:46)
- Josefina Fernandez Palenzuela - ESPAÑA (29/11/2009 20:55:46)
- Patricia Liana Giacciani - ARGENTINA (30/11/2009 1:52:27)
|
|
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 11:37:37

.jpg)
.jpg)
.jpg)
.jpg)

.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)

.jpg)















.jpg)















.jpg)


.jpg)













