
ISBN: 978-84-692-76778
 COMUNICACIONES
COMUNICACIONES
Nº 1663. Patología Autópsica
|
Tromboembolismo pulmonar en fallecidos debido a hechos violentos Daisy Ferrer Marrero[1], Isnerio Arzuaga Anderson[2], Guadalupe Alfonso Barrios[2] |
||||||||||||||||||||||||
risperdalrisperdalprednisolon og alkoholprednisolon bivirkninger halsbrand mipnet.dkObjetivo.- Caracterizar elementos del tromboembolismo pulmonar en fallecidos víctimas de violencia, atendiendo a su diagnóstico morfológico y consecuencias.
Material y Método.- Estudio descriptivo y retrospectivo en una población de 1247 fallecidos debido a hechos violentos a los que se realizó estudio histopatológico en el período seleccionado. Se identifican, como muestra, 228 casos con lesiones tromboembólicas pulmonares. Como variables: su presentación anatomopatológica; la edad; el sexo; la estadia hospitalaria; la causa básica de muerte y su relación con la causa directa de muerte de los estudiados.
Resultados.- El 38.59% se encuentra en los grupos de edades por encima de los 60 años, con predominio del sexo masculino; de las caídas como causa básica de muerte, con estadia hospitalaria prolongada. La forma de presentación de la complicación es fundamentalmente microscópica predominantemente en ramas medianas y finas. En 69 de los casos estudiados se sugirió reparo de la causa directa de muerte.
Conclusiones.- Entre otras, su relación con sexo y causa básica de muerte se corresponden con las estadísticas de mortalidad por muerte violenta del IML y, como complicación, aparece en cualquier momento; incrementándose en frecuencia, variedad y gravedad, con el envejecimiento y con la estadia hospitalaria.
|
||||||||||||||||||||||||
|
|
El Tromboembolismo Pulmonar (TEP) se define como la oclusión total o parcial de la circulación pulmonar por un coágulo sanguíneo proveniente de la circulación venosa sistémica, incluidas las cavidades cardiacas derechas. Es una enfermedad potencialmente mortal y representa la tercera causa de morbilidad cardiovascular después de la cardiopatía isquémica y la enfermedad cerebrovascular.
También es importante tener en cuenta, que el TEP no solo se manifiesta en personas fumadoras, de edad avanzada o con trastornos circulatorios graves, hay que tenerlo en cuenta en la actualidad como una de las grandes y frecuentes complicaciones que pueden sufrir las víctimas de hechos violentos, en el campo de la Patología Forense.
Como es cierto que las complicaciones en Patología Forense no difieren de aquéllas observadas en otros pacientes que presentan similares condiciones a los que resultan nuestro objeto de estudio, sus características en cuanto a definición, etiopatogenia y morfología son similares; razón por la que, siendo los trastornos circulatorios parte de los contenidos de la asignatura Anatomía Patológica durante el cuarto semestre de la carrera de Medicina se aplican éstos durante la preparación y realización de este trabajo que hoy se presenta.
OBJETIVOS:
v Caracterizar elementos vinculados al tromboembolismo pulmonar en fallecidos víctimas de violencia, a partir de su diagnóstico morfológico.
MARCO TEORICO:
& Aspectos Generales.-
El TEP supone entre el 5-6% de las muertes hospitalarias y, la mayoría de los que fallecen por esta causa, lo hacen en pocas horas (el 85% muere en 6 horas). La mortalidad, en general, se considera que es del 6 al 10%, pero puede alcanzar el 25-30% en los casos graves no tratados; no obstante, la información disponible es muy variable.
En un registro general internacional reciente, la mortalidad a los 3 meses es del 17,5%. Llama la atención que, cuando se hace una comparación anatomoclínica, sólo se realiza el diagnóstico en el 30% de los casos (12-40%), lo que significa una omisión diagnóstica, a pesar de que entre un 8-52% de las autopsias muestra evidencia de TEP reciente ó antiguo; su incidencia no parece ir disminuyendo, debido a la existencia de una población en riesgo en continuo aumento.
El término tromboembolismo pulmonar agudo (TEPA) incluye dos procesos patológicos: trombosis venosa profunda (TVP) y embolismo pulmonar; por lo que el abordaje del tema debe ser a partir de considerar el embolismo pulmonar como una complicación de la TVP.
Existen diversas clasificaciones en función de criterios clínicos, angiográficos y hemodinámicos, la más utilizada es la que distingue entre TEPA masivo ó submasivo, según que el grado de obstrucción del árbol vascular pulmonar sea mayor o menor del 50% (criterios arteriográficos) ó que la presentación incluya ó no parada cardiaca, síncope o shock (criterios clínicos). Forma parte de una de las variedades de embolismo estudiadas en Anatomía Patológica, donde se define el grosor de los vasos ocluidos, su evolución y consecuencias.
Los factores de riesgo conocidos están en relación con la clásica triada que Virchow describió el siglo pasado (estasis venoso, hipercoagulabilidad sanguínea y lesiones en las paredes vasculares); entre ellos destacan la edad avanzada, antecedentes de TEP, embarazo con pico de riesgo durante el parto, cirugía ortopédica, neurológica y abdominal, politraumatismos e inmovilizaciones prolongadas debido a diversas condiciones tales como obesidad, estancias en UCI, ortopedia ó ictus, neoplasias, estados de hipercoagulabilidad (déficit de proteina C y S, antitrombina III y plasminógeno, aumento del inhibidor del activador del plasminógeno PAI-, policitemia, síndromes antifosfolípidos y homocistinuria), administración de estrógenos y anticonceptivos en general y condiciones cardiovasculares como el IAM y fallo cardiaco, entre ótras.
El impacto real de cada factor de riesgo es variable, en grandes series el 40% de los TEP son de causa primaria, sin factor de riesgo conocido, la cirugía está presente en el 36%, la insuficiencia cardíaca en el 14%, los traumatismos en 6%, las neoplasias en 4% y los trastornos sistémicos en el 1%; en el 10% se pueden detectar alteraciones de la coagulación.
La obstrucción del flujo sanguíneo en la arteria pulmonar tiene un componente anatómico fijo y otro funcional determinada por la liberación de sustancias vasoactivas. Cuando es de entidad suficiente se producen importantes consecuencias a nivel cardíaco y respiratorio, si el evento tromboembólico no merma la vida del paciente; en último extremo, la gravedad además de depender directamente del tamaño de la embolia, también está determinada por la situación cardiopulmonar previa.
& Repercusión en el corazón.-
El TEPA provoca una reducción del área transversal del lecho arterial pulmonar; a partir de un determinado grado (se requiere perder casi el 50% de esta área para que se eleve significativamente la presión de la arteria pulmonar), se producirá hipertensión pulmonar y un aumento de la postcarga del ventrículo derecho (VD) que al no poder vaciarse adecuadamente, y tolerar mal los incrementos de presión, provocará un rápido aumento de los volúmenes telesístólico y telediastólico. Una vez sobrepasada su capacidad de adaptación, que por sus características intrínsecas es pobre, se dilata de forma progresiva. La dilatación aguda puede tener varias consecuencias:
1. Aumento de presión de forma retrógrada con disminución del retorno venoso (precarga).
2. Aumento de la tensión parietal del VD (Ley de Laplace), esta tensión intramiocárdica es causante de un aumento del consumo de oxígeno.
3. Disminución del gradiente de presión arteriovenoso coronario y por lo tanto del flujo sanguíneo, motivado por el aumento de las presiones en el corazón derecho y seno coronario.
4. Interferencia mecánica con la función del ventrículo izquierdo. Se llega a producir un aplanamiento y posterior desplazamiento del septo interventricular hacia la izquierda con repercusión negativa en la distensibilidad y llenado de dicho ventrículo, lo que lleva a un fallo diatólico.
Todos estos hechos llevan, básicamente, a una disminución del gasto cardiaco y de la presión de perfusión coronaria, y por ende a isquemia, que puede ser severa con necrosis, primero del VD con graves alteraciones de la motilidad parietal (hipoquinesia ó aquinesia). En casos de TEP masivo nos encontraremos un VD dilatado, hipoquinético, con el septo aplanadao ó desplazado a la izquierda y con frecuencia con una aurícula derecha también dilatada con regurgitación tricuspídea. Esta situación hemodinámica tan especial nos obliga a evitar mayores sobrecargas, en este caso intempestivas, de líquidos y a ser muy cuidadosos con los modos de ventilación mecánica, si fuera precisa, porque todo aumento de presión positiva en la via aérea implica una disminución del retorno venoso derecho y un aumento de la postcarga.
Debido a la complejidad de este proceso es conveniente tener monitorizada la presión de la arteria pulmonar, la fracción de eyección del VD y la saturación venosa mixta en situaciones de fallo hemodinámico ó ventilación mecánica. Sin entrar en detalles más profundos, conviene indicar que las medidas de las presiones en arteria pulmonar, sólo pueden tener correlación con el grado del TEPA en el supuesto de ausencia de enfermedad cardiopulmonar previa, así unas presiones medias superiores a 40 mmHg indican TEP masivo con muy probable repercusión en el índice cardiaco, debido a la imposibilidad que presenta el VD para generar presiones mayores; en casos de enfermedad previa no existen tales correlaciones. & Repercusión en los pulmones.-
Las consecuencias fisiológicas inmediatas después de un TEPA son un aumento del espacio muerto alveolar y broncoconstricción, posteriormente pueden aparecer atelectasias por constricción del espacio aéreo pulmonar afectado por el embolismo, posiblemente relacionada con la hipocapnia local severa, las alteraciones del surfactante pulmonar y el infarto pulmonar que puede acompañarle.
La hipoxemia es el signo más frecuente encontrado en el TEPA y es debida a alteraciones en la relación ventilación-perfusión (V/Q). Aunque es posible encontrar casos de TEPA, inclusos grandes, sin hipoxemia por compensación, lo habitual es que exista una relación entre la gravedad del cuadro y el grado de hipoxemia. Por lo tanto, la corrección de la hipoxemia deberá basarse en el conocimiento de su causa, así el aumento de la FiO2 será suficiente en algún caso, pero en otros será preciso resolver shunt intrapulmonares ó aumentar el gasto cardiaco.
La hiperventilación, es el otro gran hallazgo clínico que puede encontrarse en casos masivos; es posible que tenga una relación más directa con la magnitud del émbolo que las alteraciones de la V/Q, y se debe a la estimulación de los receptores J pulmonares. Aunque es un mecanismo compensador de la hipoxemia, la hiperventilación suele ser desproporcionada para la magnitud de las anomalías del intercambio gaseoso y puede llegar a ser globalmente perjudicial en aquellos casos con gasto cardiaco deprimido ó con un aumento de las resistencias en la vía aérea por el consumo energético aumentado que comporta.
& Criterios Diagnósticos.-
Resulta uno de los capítulos más analizados y estudiados del diagnóstico en Medicina. Clásicamente se han seguido los siguientes pasos: 1) sospecha clínica fundada, 2) gammagrafía pulmonar de ventilación perfusión (V/Q) y 3) arteriografía pulmonar si persistían dudas. Nuevos métodos diagnósticos nos han hecho cambiar tal secuencia y se tiende ahora a la realización de técnicas no invasivas.
Son varios los sígnos clínicos a tener en cuenta para evaluar la posible evolución de un paciente hacia un TEPA.
Es clave que el clínico sospeche ó se plantee la posibilidad de que exista un TEPA. Su gravedad está en relación con su presentación clínica; en casos de TEP masivo, destaca la presencia de shock, cianosis, así como signos sugestivos de fallo del VD (ruidos de galope, soplo de regurgitación tricuspídea, etc.); si la afectación es menor, los enfermos suelen presentarse con disnea, taquipnea y taquicardia de instauración súbita; otros hallazgos como dolor pleurítico y hemoptisis son menos frecuentes e indican obstrucciones distales cercanas a la pleura. Se afirma que la semiología puede tener un valor pronóstico positivo del 0,60 y negativo del 0,84. Las pruebas diagnósticas clásicas que rutinariamente acompañan a la primera valoración son:
Radiografía de tórax: Fundamental para descartar otros procesos y para la valoración racional de la gammagrafía pulmonar; aunque se señala que puede aparecer normal en el 15% de los casos. Dentro de los hallazgos radiológicos más frecuentes en pacientes con sospecha clínica según tengan ó no confirmación diagnóstica posterior se encuentran la atelectasia, el derrame pleural y la elevación del hemidiafragma, entre ótros.
Electrocardiograma: Gran prueba de rutina ante todo paciente con molestias torácicas; ya que hasta un 63% de los pacientes con TEP probado tienen alguna alteración en el ECG; siendo los hallazgos más frecuentes la taquicardia sinusal, la inversión de la onda T, el bloqueo de rama derecha (completo ó incompleto), las alteraciones segmento ST, las arritmias supraventriculares, los trastornos de la conducción, las ondas p pulmonale, el bajo voltaje general y el clásico patrón S1Q3T3; aunque pueden aparecer en el 41% de los enfermos sin confirmación posterior.
A estos datos conviene añadir la valoración de las precordiales derechas (V4R-V6R) donde pueden aparecer ascensos del ST e incluso ondas q transitorias.
Pruebas de Laboratorio: La más utilizada es la determinación de gases en sangre, hallazgos de PaO2 menor de 80 mmHg con disminución de la PaCO2 apoyan el diagnóstico pero no es un dato absoluto.
Se han publicado otras pruebas, pero sin la suficiente validez diagnóstica. Ultimamente, se discute el valor del D-Dimero (producto de la degradación de la fibrina) como marcador de trombosis aguda y de TEPA; algunos señalan que valores por debajo de 500 microgramos/litro, prácticamente excluyen su presencia a la vez que plantean que puede elevarse en múltiples patologías como IAM, neumonía, fallo cardíaco, cáncer o cirugía.
& Diagnóstico de la trombosis venosa profunda (foco embolígeno).-
Siempre que la gammagrafía no sea diagnóstica o se quiera evaluar el riesgo de recurrencia hay que investigar la presencia de TVP. Las técnicas diagnósticas más utilizadas son la flebografía de contraste, como fuente de referencia, a pesar de ser invasiva y no estardisponible en muchos centros; la flebografía isotópica; la pletismografía de impedancia; la ecografía del sistema venoso, técnica que ha demostrado ser un poderoso recurso diagnóstico no invasivo, siendo especialmente útil para la valoración del eje femoral y de la vena poplítea; la venografía isotópica con anticuerpos monoclonales antifibrina, que se plantea que puede alcanzar una seguridad diagnóstica cercana al 90% siendo de especial interés porque puede distinguir entre procesos agudos ó crónicos.
& Tratamiento.-
La forma de presentación es fundamental a la hora de adoptar una actitud terapéutica correcta. En todos los supuestos, siempre hay que prevenir la recurrencia del tromboembolismo, pero si se trata de un TEPA masivo el objetivo fundamental es la estabilización de la función cardiorespiratoria, recuperación de la hipoxemia y reversión de la situación de cor pulmonale agudo; por lo que el tratamiento debe ser integrado y escalonado, en función de las circunstancias clínicas del paciente. Las medidas de soporte (aporte de volumen, drogas vasoactivas, ventilación mecánica), anticoagulantes, fármacos trombolíticos, interrupción de la vena cava y la embolectomía quirúrgica, forman parte del tratamiento, y cada uno de ellos cubre una parte de estos objetivos prioritarios. El empleo de anticoagulantes ha sido el tratamiento de elección al mejorar significativamente la supervivencia de estos enfermos, pero su acción es más preventiva de nuevas recidivas que resolutiva sobre la lisis del trombo pulmonar responsable del cuadro. Si el paciente logra sobrevivir a este proceso inicial, el sistema fibrinolítico natural se pone en marcha hacia el 2º-3º día, alcanzando su máxima efectividad a la semana. En el caso del TEPA masivo, es prioritaria la desobstrucción, lo más rápidamente posible, de la circulación pulmonar, bien por métodos mecánicos (embolectomía) o farmacológicos (trombolíticos).
Dentro del arsenal terapéutico., considerado en forma general, deben indicarse: Medidas Generales, tales como reposo y oxigenoterapia; el empleo, con precaución de fármacos vasoactivos (Isoproterenol, Noradrenalina, Adrenalina, Dopamina y Dobutamina).
Existe actualmente una gran controversia sobre el uso de ionotrópicos para incrementar el gasto cardiaco hasta valores suprafisiológicos en un intento de mejorar el transporte de oxígeno en el paciente crítico. En este sentido es importante tener en cuenta que en el TEPA, un incremento del gasto cardiaco, podría empeorar la relación ventilación-perfusión por redistribución del flujo sanguíneo desde vasos obstruidos vasos no obstruidos.
Deben adoptarse Medidas Específicas, en este caso, proceder a la anticoagulación; aunque está demostrado que su realización con heparina mejora significativamente la supervivencia de los pacientes con TEPA (la mortalidad disminuyó del 25 % al 7%), no actúa sobre la lisis directa del trombo pulmonar responsable del cuadro y en casos de embolismos masivos son precisos enfoques distintos, toda vez que el sistema fibrinolítico natural tarda días en comenzar su actuación y la mortalidad incide en las primeras horas de evolución. Existe una relación de fármacos anticoagulantes, que se añade a la heparina, tales como heparinas de bajo peso molecular (HBPM) y los anticoagulantes orales.
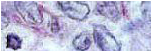
& Anatomía Patológica del Tromboembolismo Pulmonar.-
El empleo de los signos diagnósticos es, sin dudas, el primer escalón diagnóstico, aunque con una sensibilidad aislada muy baja; ya que la concordancia diagnóstica antemortem y, aún, en la autopsia oscila entre el 16-38%; lo que reitera la importancia del diagnóstico anatomopatológico.
Como ya se ha afirmado, la oclusión de las arterias pulmonares por coágulos sanguíneos, casi siempre es de origen embólico; siendo su mayor origen la presencia de trombos en las venas profundas de los miembros inferiores.
Las consecuencias morfológicas de la oclusión embólica de las arterias pulmonares dependen del calibre de la masa y del estado general de la circulación. Los émbolos voluminosos pueden quedar enclavados en el tronco de la arteria pulmonar o en sus ramas principales, sobre la bifurcación, en forma de émbolo en silla de montar.
Para poner de manifiesto los émbolos pulmonares de procederse a la apertura in situ de la arteria pulmonar, antes de separar el corazón, mediante la técnica descrita para ello; así como deben examinarse las venas profundas de las extremidades, mediante disección.
Es preciso además establecer la vitalidad del coágulo, mediante su caracterización, resultando ser cilindros de alrededor de 1 centímetro de diámetro y hasta 30 centímetros de longitud, que remedan una masa retorcida, como una serpiente, a nivel de la arteria pulmonar.
Si el estado circulatorio es suficiente, el riego de las arterias bronquiales puede mantener la vitalidad del parénquima, pudiendo apreciarse hemorragias, las que se caracterizan por la conservación del parénquima.
La presencia de émbolos de pequeño tamaño puede condicionar la existencia de un infarto pulmonar, cuando la circulación es insuficiente; sobre todo en cardiópatas o pacientes con cáncer avanzado, razón por la que son menos frecuentes en jóvenes.
El infarto no se produce por solo oclusión arterial; siendo importante la existencia de un aumento de la presión venosa, lo que se relaciona con una mayor frecuencia de presentación en los lóbulos inferiores donde la presión venosa es mayor y cuando hay otras patologías previas que, experimentalmente, favorecen el infarto.
El infarto pulmonar es hemorrágico, como zona elevada de color rojo azulado, con reacción fibrinosa en la pleura y friabilidad del parénquima a la presión. Su evolución traduce cambio de color por la producción de hemosiderina.
Su impacto en el tronco de la arteria pulmonar y sus ramas principales es frecuente causa de muerte súbita, debido, en gran parte, al obstáculo para el paso de la sangre a través de los pulmones.
Junto al diagnóstico morfológico del tromboembolismo pulmonar es importante establecer el diagnóstico de las posibles entidades favorecedoras de su aparición, tales como la localización y envergadura de los traumatismos y el encamamiento que de ellos derivan.
|
|||||||||||||||||||||||
|
|
Para dar salida al objetivo propuesto, se realiza un estudio descriptivo y retrospectivo en una población de 1247 fallecidos debido a hechos violentos a los que se realiza estudio histopatológico durante el quinquenio 2003- 2007 en el Instituto de Medicina Legal.
De la revisión de los informes histopatológicos del Departamento de Patología Forense de dicho centro, se identifican 228 casos en los que se diagnostican lesiones tromboembólicas, lo que constituye la muestra.
Como variables a estudiar se definen su presentación anatomopatológica, la edad y el sexo; la estadia hospitalaria; la causa básica de muerte y el significado, en relación con la causa directa de muerte, de los casos estudiados.
Los datos obtenidos se vuelcan en un modelo de recogida de información, confeccionado al efecto y se procesan calculando frecuencias absolutas y relativas, atendiendo a las propias variables y al objetivo propuesto.
Los resultados obtenidos se discuten, en relación con la bibliografía consultada sobre el tema y se ilustran convenientemente, con el empleo de imágenes, cuadros y figuras. Se presenta también la bibliografía, la que se acota en orden alfabético.
|
|||||||||||||||||||||||
|
|
De la población, constituida por 1247 fallecidos a los cuales se les realiza necropsia medicolegal con estudio histopatológico como investigación complementaria en el Instituto de Medicina Legal durante el quinquenio 2003-2007, 228 (18.28%) constituyen la muestra al tener, dentro de sus diagnósticos macro y microscópicos, alguna forma de presentación del tromboembolismo pulmonar, que es el objeto de estudio (Figura No. 1); no existiendo grandes discrepancias con las cifras que se presentan en la literatura, como en el caso de la Tesis para obtener el Grado de Master en Ciencias del Dr. Miguel López que reporta un 28.57%, sólo en una modalidad de hecho violento (la enfermedad por quemaduras). En tanto, Bounameaux H, reporta una frecuencia del 10% de TEP en necropsias, mientras que Michota F informa por estudio anatomopatológico una cifra muy superior, el 25 %.
El mayor porcentaje de fallecidos (38.59%) en los que se diagnostica alguna forma de tromboembolismo pulmonar se encuentra en los grupos de edades por encima de los 60 años (Cuadro No. 1 y Figura No. 2); pudiendo estar influido por tratarse de un intervalo de clase mayor.
A pesar de que la mortalidad por hechos violentos es relevante en edades tempranas de la vida, esta complicación aparece con frecuencia más tardíamente (por encima de los 40 años) como lo señalan Savel VS y Lazarenko VA y Mishustin VN, en sus respectivos trabajos; lo que puede explicarse por la existencia de factores etiopatogénicos propios de la edad y posiblemente, en relación con la causa básica que desencadena la muerte ya que, con mucha frecuencia se producen lesiones en miembros inferiores y /o encamamiento. En la literatura se señala que su aparición se incrementa con la edad hasta la séptima década; específicamente se acepta que el riesgo de muerte aumenta con la edad avanzada, tabaquismo, enfermedad cardiovascular, insuficiencia cardiaca congestiva, insuficiencia renal crónica y malignidad, que causan el 10% de las muertes en hospitales y que son factor contribuyente en 15% de todas ellas.
Gosta A reporta mayor incidencia de TEP a medida que aumenta la edad, siendo más frecuentes después de los 60 años; coincidiendo con Worralurt C y García Montero A quienes consideran que, a medida que aumenta la edad, es más frecuente la ocurrencia de TEP.
Existe un franco predominio del sexo masculino (Figura No. 3), en correspondenciacon las estadísticas de muerte violenta de la ciudad, del país y del mundo, donde se hace manifiesto este comportamiento. A pesar de este elemento vinculado con la característica medicolegal de la muestra, el comportamiento del sexo también coincide con la literatura donde se plantea que es ligeramente más frecuente en hombres que en mujeres, con mayor diferencia a partir del los 40 años, a pesar del uso de anticonceptivos en las mujeres, esto que por lo general se asocian a TVP.
Coincidiendo con el presente estudio, aunque con una muestra diferente, Tamayo Pérez observa que la relación masculina/ femenina en su trabajo es discretamente superior a 1 y; aunque con proporciones diferentes, se reporta predominio de ese sexo en el trabajo de López M y el de Worralurt C.
La consideración del diagnóstico de esta complicación circulatoria según causa básica de muerte certificada, revela que el mayor porcentaje (Figura No. 4) se encuentra en relación con muertes debido a caídas y precipitaciones, seguido de los accidentes de tránsito (35.08 y 28.07% respectivamente); en correspondencia con las estadísticas actuales de mortalidad por violencias en el Instituto de Medicina Legal. Esta asociación entre la aparición del fenómeno tromboembolico y estas violencias puede explicar su aparición; ya que, con mucha frecuencia, provocan lesiones de miembros inferiores y condicionan el encamamiento, factores ambos reconocidos como favorecedores para su aparición, incluso como causa directa de muerte; según se ha planteado en el marco teórico elaborado.
En relación con la estadia hospitalaria (Figura No. 5), se observa que el mayor porcentaje (71.05%) se encuentra en el ingreso hospitalario de más de 72 horas; comportamiento similar al observado para la mayoría de las complicaciones que se presentan en sujetos víctimas de violencia.
Llama la atención que sólo en el 14.47% de los casos en que se presenta el TEP (Figura No. 6), éste ha sido diagnosticado macroscópicamente; a pesar de afectar vasos gruesos y medianos en el 43.85% de los casos en que se diagnostica histológicamente; lo que no debe ocurrir regularmente durante la exploración de la necropsia. Ello conlleva a que la forma de presentación de la complicación en la muestra estudiada es fundamentalmente microscópica aunque a expensas de ramas medianas y finas (casos del total); pudiéndose considerar, en algunos casos, una complicación más que una causa directa de muerte.
Un elemento a considerar, como referente de calidad, y relacionado con los resultados plasmados en el epígrafe anterior (Figura No. 7), debe destacarse que, en 69 de los casos estudiados (30.26%), se recomienda reparo de la causa directa de la muerte, atendiendo al diagnóstico realizado; siendo la bronconeumonía la complicación que más se sobrediagnostica (43.47%) en relación con el tromboembolismo pulmonar.
|
|||||||||||||||||||||||
|
|
Las características de la muestra, en relación con sexo y causa básica de muerte, se corresponden con las estadísticas de mortalidad por muerte violenta en el IML.
Las alteraciones morfológicas del tromboembolismo pulmonar, como complicación, aparecen en cualquier momento y causa de muerte; incrementándose en frecuencia, variedad y gravedad, con el envejecimiento y con la estadia hospitalaria.
Existe un subregistro del diagnóstico macroscópico de tromboembolismo pulmonar, no debiendo ignorarse que estas patologías pueden resultar causas directa de muerte de los hechos violentos estudiados y que su omisión puede reflejar afectaciones de la calidad durante la confección del certificado médico de defunción a partir de la necropsia.
|
|||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||
|
|
- Amparo de la Candelaria Rivera Valdespino - CUBA (05/11/2009 18:55:54)
- Daisy Ferrer Marrero - CUBA (Autor) (06/11/2009 3:08:09)
- HERMINIA BRU GOMEZ - ESPAÑA (13/11/2009 17:41:19)
- Daisy Ferrer Marrero - CUBA (Autor) (15/11/2009 16:47:00)
- FELIX SANCHEZ UGENA - ESPAÑA (19/11/2009 12:15:17)
- Marta Grijalba Mazo - ESPAÑA (23/11/2009 17:36:14)
- Mirta García Jardón - REPUBLICA SUDAFRICANA (29/11/2009 16:43:14)
|
|||||||||||||||||||||||
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 11:37:37

.jpg)
.jpg)

.jpg)




