
ISBN: 978-84-692-76778
 COMUNICACIONES
COMUNICACIONES
Nº 1584. Patología Autópsica
|
Síndrome mielodisplástico y adenocarcinoma prostático. MCs Walter Marcial Martínez Rodríguez[1], Isidro Machado Puerto[2], María Nélida Valdés Santiesteban[1], Olga Forteza Trujillo[1], Solángel Rúa Martínez[3], Ana Gloria Pérez Reyes[1] |
|
symbicort generic alternativesymbicort inhaler coupon poisel.cz symbicort generic datefluoxetine and alcohol withdrawalfluoxetine alcohol memory loss
|
||
|
|
En pacientes con síndrome mielodisplástico pueden aparecer tumores malignos sólidos, antes, durante o después del síndrome. Según Sans-Sabrafen J. y cols. (1992) (1), el riesgo relativo de padecer de tumores malignos sólidos; en pacientes con este síndrome es significativamente más alto que en la población en general. Por la importancia que reviste se presenta el caso de un paciente con síndrome mielodisplástico y adenocarcinoma prostático.
|
|
|
|
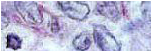
JRB, 59años, masculino, blanco, ingresó por decaimiento y fiebre de 38 grados, con antecedentes alcoholismo e hipertensión arterial (HTA). Exámenes al ingreso: creatinina 60 mmol/l; TGP 7 ud/l; TGO 7 ud/l; conteo de reticulocitos 6 x 10-3, hematocrito (HTO) 0,21; Hemoglobina (HB) 7,0 g/l; leucocitos 0,5 x 105 /l; eritrosedimentación 150 mm/h; lámina periférica: severa pancitopenia; Coagulograma: tiempo de protrombina: control 14 seg., paciente 50; coágulo retráctil; plaquetas: 5 x 104 /l; Ultrasonido de abdomen superior: ligera hepatomegalia, no esplenomegalia ni adenomegalias. Biopsia de médula ósea (BMO): Estado mielo displásico avanzado con marcada dismorfia megacariopoyética y granulopoyética con aumento del número de formas jóvenes y tempranas y fibrosis reticular grado II. Evoluciona tórpidamente, reingresa en varias ocasiones para ser transfundido y finalmente muere en un cuadro de choque séptico. Un Cuadro Clínico resumen aparece en Figura 1 Los resultados del examen macroscópico se presentan resumidos en la Figura 2.El resultado de la necropsia fue el siguiente: Causa directa muerte: Fallo múltiple de órganos; Causa intermedia I: Choque séptico; Causa intermedia II: Leucemia míelo monocítica aguda; Causa básica de muerte Síndrome mielodisplástico; Causa contribuyente de muerte: Adenocarcinoma de próstata grado 8 de Gleason (Figura 3). Otros Diagnósticos: Infiltración leucémica de pulmón (Figura 4), de hígado (Figura 5), bazo (Figura 6), infiltración del miocardio (Figura 7)
|
|
|
|
Sans-Sabrafen J. y cols. (1992) (1), estudiaron la asociación entre el Síndrome mielodisplásico (SMD) y el cáncer en una cohorte de 155 pacientes con SMD, 21 de ellos presentaron tumores sólidos. SMD estuvo presente después del diagnóstico de cáncer en 8 pacientes, con intervalo entre el diagnóstico de ambas entidades de 18 meses y supervivencia media de 49;5 meses; se presentaron simultáneamente en 11, con supervivencia media de 8 meses; y antes del cáncer en 2 pacientes; con intervalo de diagnóstico de ambas entidades, de 47 y 7 meses. Un paciente había recibido quimioterapia por tumor maligno de pulmón y tres radioterapia por adenocarcinoma de riñón y cáncer de próstata. En el momento del diagnóstico de SMD, 9 pacientes ya presentaban enfermedad metastásica. Catorce pacientes murieron, diez como resultado de complicaciones relacionadas con el tumor y 4 como resultado de la evolución del SDM hacia una leucemia aguda. El análisis de la incidencia de tumores sólidos en pacientes con SMD en el estudio de Sans-Sabrafen J. (1) fue estadísticamente significativo en el sexo masculino y, el riesgo relativo fue significativo en ambos sexos. Los resultados de este estudio muestran que los pacientes con SDM presentan una más alta incidencia de tumores malignos que la población general, que el SMD puede ser de real significación paraneoplásica, y que la ocurrencia de SDM en pacientes con tumores malignos este relacionada con la ocurrencia de tumores malignos múltiples más bien que fenómenos independientes.
Aunque el SMD fue inicialmente fue considerado por muchos como sinónimo de preleucemia. Ha cedido su lugar al concepto de que el SDM es un grupo heterogéneo de que enfermedades y que la mayoría de los pacientes sucumben a las complicaciones del fallo de la médula ósea más bien que a la leucemia aguda. La heterogeneidad tanto de la clínica como de los hallazgos morfológicos en el SMD refleja la diversidad y complejidad de los defectos genéticos subyacentes, de los cuales, la mayoría se ignora. Sin embargo, el común denominador de todos los casos de SMD es la inefectiva hematopoyesis, usualmente acompañada por displasia morfológica; a menudo, acompañada de un número incrementado de blastos en sangre periférica y/o médula ósea (MO). En 1982, la French-American-British (FAB, por su sigla en inglés) las guias para el diagnóstico y clasificación del SMD basada en los linajes mieloides morfológicamente afectados por la displasia y el porcentaje de blastos en sangre periférica y médula ósea. Numerosos estudios publicados documentan la utilidad clínica de la clasificación FAB y así validan la contribución de una clasificación basada en la morfología para predecir el pronóstico y evolución de la leucemia aguda (2). En el 2001, la clasificación FAB, fue revisada y actualizada por la Organización Mundial de la Salud (OMS) (3) (Tabla I). El concepto del sistema de la OMS es que la clasificación de las neoplasias hematopoyéticas debe utilizar no sólo hallazgos morfológicos sino también clínicos, genéticos, inmunofenotípicos, e información biológica; para definir las distintas entidades (4). Sin embargo por causa de que todavía no ha sido descubierto un marcador genético o biológico que de manera confiable identifique a todos los casos de SMD, la morfología sigue siendo la piedra angular del diagnóstico en el sistema de la OMS
|
|
|
|
El riesgo relativo de tumores malignos sólidos en pacientes con síndrome mielodisplástico es significativamente mayor. La aparición de síndrome mielodisplástico en pacientes con tumores malignos sólidos puede que no sea un fenómeno independiente
|
|
|
|
1-Sans-Sabrafen J, Buxo Costes J, Woessner S, Florensa L, Besses C, Malats N, Porta M. Myelodysplastic syndroms and malignant solid tumors análisis of 21 tumors. Am J Hematol, 1992 Se; 41(1): 1-4
2-Bennett JM, Catovsky D, Daniel MT, et al. Proposals for theclassification of the myelodysplastic syndromes. Br J Haematol. 1982;51:189-199.
3. Jaffe ES, Harris NL, Stein H, Vardiman JW (eds). World Health Organization Classification of Tumours. Pathology and Genetics of Tumours of Haematopoietic and Lymphoid Tissues. IARC Press: Lyon; 2001.
4. Vardiman JW, Harris NL, Brunning RD. The World Health (WHO) classification of the myeloid neoplasms. Blood. 2002;100:2292-302.
|
|
|
|
- Isidro Machado - ESPAÑA (13/11/2009 21:08:27)
- AMAIA Padilla - ESPAÑA (20/11/2009 13:00:51)
|
|
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 11:37:37

