
ISBN: 978-84-692-76778
 COMUNICACIONES
COMUNICACIONES
Nº 1578. Otras disciplinas
|
Lucía González Núñez[1], Enoy Leiva Pantoja[2], Sandra Rodríguez Salgueiro[2], José Luis Calunga[2], Tania Valdés Prieto[2], Yahima Harvey Pedroso[2], Mariuska Matos Terrero[2], Aimée Fernández[1] |
|
viagra and smoking weedviagra and weedviagra prodej prahaviagra prodej cena read hereLa isquemia-reperfusión renal es causa de insuficiencia renal aguda, la cual presenta un alto índice de mortalidad. En la actualidad los tratamientos empleados en la recuperación del riñón sometido a isquemia-reperfusión tienen un éxito limitado. Por tanto, se hace necesaria la búsqueda de estrategias terapéuticas efectivas que ayuden a prevenir el daño renal. La característica histopatológica más prominente de la isquemia-reperfusión renal es la lesión de los túbulos proximales corticales. El objetivo de este trabajo fue evaluar el efecto del precondicionamiento oxidativo con ozono sobre la morfología de los túbulos proximales de la corteza renal, en un modelo animal de isquemia-reperfusión. Se estudiaron fragmentos de corteza renal procedentes de 16 ratas, divididas en cuatro grupos: controles, dañadas por isquemia-reperfusión (60 min de isquemia seguidos por 180 min de reperfusión) y dos grupos de ratas precondicionadas con ozono (0,5 y 1,1 mg/kg de peso corporal respectivamente) y sometidas a isquemia-reperfusión. Las muestras se procesaron según la técnica convencional de inclusión en resina Spurr. Se realizaron cortes semifinos, que se analizaron cualitativa y cuantitativamente por Microscopia Óptica. Se identificaron los marcadores morfológicos del daño renal inducido por isquemia-reperfusión sobre los túbulos proximales renales: pérdida del ribete en cepillo, dilatación tubular, aumento de áreas y perímetros tubulares, necrosis celular y aumento de núcleos de células epiteliales en la luz tubular, relacionado con la formación de cilindros. El precondicionamiento oxidativo con ozono condujo a la recuperación de la morfología de los túbulos proximales. Al propiciar la protección de las células epiteliales de los túbulos proximales renales, la ozonoterapia podría considerarse una herramienta efectiva ante el daño por isquemia reperfusión renal.
|
||
|
|
La isquemia-reperfusión (I/R) renal es causa de insuficiencia renal aguda, que de no ser solucionada a tiempo, conlleva a la necrosis tubular aguda, la insuficiencia renal aguda y la disfunción endotelial causada por la restauración de los tejidos dañados.1-3 Los tejidos sometidos a I/R pueden recuperarse y tener una función normal, siempre que se logren interrumpir a tiempo las vías del daño celular involucradas en la I/R. La vasoconstricción renal y la disfunción tubular son los mecanismos más importantes que afectan el funcionamiento de la unidad funcional renal (nefrona) después de la I/R.4
La I/R renal deriva de muchas afecciones frecuentes como pueden ser: hemorragia aguda, shock, trasplante renal, quemaduras extensas, hipovolemia de cualquier tipo y es origen de complicaciones renales graves, que pueden comprometer la vida del paciente. 5
Las terapias para prevenir, tratar o disminuir el daño renal agudo por I/R tienen un alcance limitado en la recuperación del riñón sometido a I/R.6 Por tanto, se hace necesaria la búsqueda de estrategias terapéuticas efectivas que ayuden a prevenir el daño por I/R.
La característica histopatológica predominante en la I/R renal es la lesión de los túbulos proximales corticales, debida a muerte de células epiteliales tanto por necrosis como por apoptosis.7 Se plantea que la causa principal para el desarrollo y progresión del daño renal agudo por I/R es la pérdida del funcionamiento de las células epiteliales de los túbulos proximales renales.8 En la actualidad se estudian diferentes tratamientos para lograr la protección de esas células y así preservar al riñón contra la I/R, mediante modelos experimentales in vivo9-11 e in vitro.12-13
Durante la I/R, las células de los túbulos renales se hacen sensibles al ataque de las especies reactivas al oxígeno (ERO).14 La ozonoterapia es una práctica altamente beneficiosa y segura que se emplea en muchos países para el tratamiento de afecciones en las que están involucradas las ERO.15 El precondicionamiento oxidativo con ozono favorece el equilibrio antioxidante-pro-oxidante para la preservación del estado redox celular, aumentando los sistemas antioxidantes endógenos en varios modelos experimentales in vivo e in vitro.16
En diferentes modelos experimentales de I/R renal se ha validado el precondicionamiento oxidativo con ozono, obteniéndose la preservación del tejido renal en I/R de hasta 45 min.17-18 Sin embargo, en varias situaciones clínicas el tiempo de isquemia renal excede ese tiempo.
El objetivo de este trabajo fue evaluar el efecto del precondicionamiento oxidativo con ozono sobre la morfología de los túbulos proximales de la corteza renal, en un modelo de I/R en ratas (60 min de isquemia seguidos por 180 min de reperfusión).
|
|
|
|
Se emplearon 16 ratas machos Wistar clínicamente sanas procedentes del Centro Nacional para la Producción de Animales de Laboratorio (CENPALAB), con un peso promedio entre 220-250 g . Las ratas se alimentaron diariamente con 25 g de pienso normal (dieta estándar CENPALAB) y agua corriente. Los animales se dividieron aleatoriamente en 4 grupos de 3-5 ratas cada uno: un grupo control negativo (no tratados), un grupo control positivo (sometidos a I/R) y dos grupos de animales pretratados con Ozono 0,5 y 1,1 mg/kg y sometidos a I/R.
Administración del Ozono
El ozono se administró por vía rectal y se generó mediante un equipo OZOMED, fabricado en el Centro de Investigaciones del Ozono, de Ciudad de la Habana, Cuba. El ozono se obtuvo a partir de oxígeno medicinal y se utilizó inmediatamente después de ser generado. El ozono constituyó alrededor del 3 % de la mezcla gaseosa ozonooxígeno (O2 + O3). La concentración de ozono se determinó a través de un espectrofotómetro, a 254 nm (exactitud 0,002 a 1 DO, repetitividad 0,001 DO y calibrado con un estándar interno).
Las dosis de ozono se determinaron multiplicando la concentración de ozono expresada en mg/L por el volumen de la mezcla gaseosa O2 + O3. En este estudio, las dosis de ozono se corresponden con las empleadas en la práctica clínica y preclínica.17, 19, 20
Procedimiento quirúrgico para la I/R renal
Las ratas se anestesiaron con pentobarbital sódico a la dosis de 30 mg/kg de peso corporal, por vía intraperitoneal y se les administró 50 UI de heparina por la misma vía. Posteriormente se realizó la laparotomía por incisión longitudinal en la línea media de los animales. Se expusieron los paquetes vasculares renales, aislándose ambas arterias renales, en las cuales se colocaron las piezas de compresión y oclusión (clanes), provocando una isquemia durante 60 min. Luego se retiraron los clanes, permitiendo la reperfusión de los riñones durante 180 min. Se controló la temperatura corporal del animal mediante el uso de un termómetro clínico en la zona rectal.
Procesamiento histológico
Se procesaron cuatro fragmentos de corteza renal por animal. La fijación se realizó con glutaraldehído 3,2 % y tetróxido de osmio 2 %, en disolución estabilizadora fosfato de sodio 0,1 mol/L, pH 7,2-7,4; la deshidratación fue con acetona a concentraciones crecientes desde 10 % hasta 100 %. Los fragmentos de tejido se incluyeron en bloques de resina Spurr.21 De los bloques obtenidos se realizaron cortes semifinos de 2 µm, mediante un ultramicrótomo LKB Ultrotome III, que se tiñeron con azul de Stevenel.22
Estudio morfológico y morfométrico
Se estudiaron imágenes de túbulos proximales de la corteza renal cortados transversalmente; digitalizadas en al menos cinco campos seleccionados en un corte semifino por cada bloque de inclusión. En total se analizaron como mínimo 20 imágenes por animal.
Las imágenes se tomaron a 1000 X, mediante una cámara digital de alta resolución DS-5M-U1 acoplada a un microscopio Nikon 50i.
Se evaluó la presencia de cambios degenerativos en los túbulos proximales: presencia o no del ribete en cepillo de las células epiteliales, número de núcleos en la luz tubular (dos túbulos por campo) y se midió el área y el perímetro tubulares (un túbulo por campo) (Fig. 1).
Todas las mediciones se realizaron con ayuda del programa morfométrico Image J.23
Se comprobó la circularidad de los túbulos como indicador de que estaban cortados transversalmente, mediante la fórmula:24
4π área/(perímetro)2
Análisis estadístico
Para el procesamiento estadístico se empleó el programa Graph Pad Prism versión 5.0 para Windows. En todos los casos se determinaron los valores de media y desviación estándar mediante estadística descriptiva. Se realizaron comparaciones entre grupos en cuanto a: área tubular, perímetro tubular y número de núcleos en la luz tubular.
Para el análisis de las diferencias entre grupos en cuanto a áreas y perímetros tubulares, se realizó un análisis de varianza (ANOVA) de clasificación simple. Las medias de dichos tratamientos se compararon utilizando la prueba paramétrica Newman-Keuls. Para comparar el número de núcleos en la luz tubular se emplearon la prueba de comparaciones múltiples de Dunn y la prueba no paramétrica Kruskal-Wallis.
|
|
|
|
Resultados cualitativos
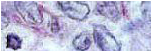
En los animales controles negativos se observó la estructura normal de los túbulos proximales de la corteza renal, los cuales presentaron un epitelio simple cúbico alto; formado por células que presentaron gran cantidad de microvellosidades en su borde apical, constituyendo el ribete en cepillo; núcleo voluminoso situado hacia la base y nucleolo prominente, el citoplasma se observó pálido, de aspecto homogéneo (Fig. 2A).
En el grupo control positivo se observó dilatación tubular, pérdida del ribete en cepillo de las células epiteliales, extrusión nuclear, taponamiento de la luz tubular y diversos grados de vacuolización citoplasmática (Fig. 2B).
En los grupos precondicionados con ozono y sometidos a I/R, se evidenció una mejor conservación de la morfología de los túbulos, en cuanto a conservación del ribete en cepillo de las células epiteliales y luz tubular evidente (Fig. 2C).
Resultados cuantitativos
Área tubular
Al comparar las áreas tubulares entre los diferentes grupos estudiados se observó un aumento significativo del área en los animales del grupo control positivo. En los grupos precondicionados con ozono hubo un aumento de área significativamente menor que en el grupo control positivo, sin observarse diferencias entre las dos dosis de ozono (Fig. 3).
El aumento de área indica dilatación tubular relacionada con la extrusión de núcleos celulares y la formación de cilindros que obstruyen la luz tubular.
Perímetro tubular
El perímetro tubular aumentó significativamente en el grupo control positivo con respecto al control negativo. En los grupos precondicionados con ozono, los valores de esta variable fueron similares a los del grupo control negativo y significativamente menores que los del control positivo, sin observarse diferencias entre las dos dosis de ozono (Fig. 4).
El aumento del perímetro tubular se corresponde directamente conel del áreacuando los contornos tubulares son regulares, por tanto el aumento del perímetro tubular se debe al aumento del área.
Número de núcleos en la luz tubular
El análisis estadístico evidenció un aumento significativo del número de núcleos en la luz tubular en el grupo control positivo con respecto al resto de los grupos. No se observaron diferencias entre los grupos precondicionados con las dos dosis de ozono y el grupo control negativo (Fig. 5).
El aumento de esta variable revela necrosis renal tubular, ya que los núcleos presentes en la luz del túbulo proximal son producto de la ruptura de las membranas citoplasmáticas de las células epiteliales y salida de su contenido.
|
|
|
|
Existen situaciones clínicas en la práctica médica diaria como: el trasplante renal, las nefrotomías renales para el tratamiento de la litiasis renal y la cirugía conservadora de los tumores renales entre otras, en las cuales es necesario realizar I/R temporal, donde se produce una lesión morfológica y funcional la cual depende del tiempo de isquemia. Hay otros casos en los que se produce I/R temporal, tales como la vasodilatación periférica en el curso de una bacteriemia, la hipovolemia en el curso de una hemorragia, la obstrucción vascular renal en el curso de un embolismo a nivel de la arteria renal, el taponamiento cardiaco, la cardiopatía congestiva y el infarto agudo del miocardio.5
Como consecuencia de la I/R se produce una lesión tubular. Cuando este evento es clínicamente severo se comporta como una necrosis tubular, que de no ser corregida lleva al paciente a la insuficiencia renal aguda.4
Está bien documentado que las ERO juegan un papel determinante en el deterioro funcional y estructural del riñón sometido a daño isquémico, sobre todo cuando este daño excede los 45 min de abolición de la perfusión renal.18 Actualmente se ha correlacionado un incremento de las ERO con un decremento de la función renal en modelos de I/R renal.17,18
El ozono tiene influencia directa sobre el metabolismo del oxígeno. Esto lo logra por el incremento de la presión parcial de oxígeno en sangre y tejidos; por su efecto de estimular el metabolismo de los eritrocitos y por evitar la disposición de los eritrocitos en pilas de monedas, mejorando de esta forma el flujo sanguíneo y por tanto, el transporte de oxígeno a los tejidos.25 La ozonoterapia induce la activación de enzimas que intervienen en la degradación de peróxidos y radicales libres.16
El precondicionamiento con ozono previene el daño por I/R en diferentes órganos.17,20,26 En estas condiciones el precondicionamiento oxidativo comparte características similares al precondicionamiento isquémico.27-28
Los resultados histológicos presentados en este trabajo concuerdan con lo obtenido por otros autores sobre el efecto de un precondicionamiento con ozono en órganos sometidos a I/R.17,18,26 En el presente trabajo los riñones se sometieron a un tiempo de isquemia mayor a lo reportado anteriormente.
Estos resultados se correlacionan con los obtenidos de la medición de marcadores de la función renal realizados en paralelo con el estudio morfológico. El precondicionamiento con las dos dosis de ozono permitió una mejor preparación del tejido renal para soportar el evento de I/R, al estimular la actividad de enzimas antioxidantes, preservar los niveles tisulares de productos avanzados de la glicosilación, ejercer efecto estabilizador de la fosfolipasa A2 y disminuir la expresión de IL-6 a nivel del riñón postisquémico.29
|
|
|
|
En este trabajo se demostró el efecto protector del precondicionamiento oxidativo con ozono sobre la morfología de los túbulos proximales de la corteza renal en riñones de ratas sometidos a 60 min de isquemia seguidos de 180 min de reperfusión.
Al propiciar la protección de las células epiteliales de los túbulos proximales renales, la ozonoterapia podría considerarse como una herramienta efectiva ante el daño por isquemia reperfusión renal.
|
|
|
|
1. Alfonso M. A, Simón C. R, Quintela A. M, Mercedes M. R. Modelo isquemia reperfusión en miembros inferiores de ratas. Rev Cubana Angiol y Cir Vasc. 2000;1(1): 38-41.
2. Kadkhodaee M, Hanson GR, Towner RA, Endre ZH. Detection of hydroxyl and carbon-centred radicals by EPR spectroscopy after ischaemia and reperfusion of the rat kidney. Free Radic Res. 1996;25: 31-42.
3. Kadkhodaee M, Hemmati M, Zahmatkesh M, Ghaznavi R, Mirershadi F, Mahdavi-Mazde, et al. Assessment of plasma antioxidant status in hemodialysis patients. Ther Apher Dial. 2008;12: 147-151.
4. Brenner BM. The Kidney. 6th ed. EU: Ed WE Saunders Company:T1: 2000: p. 1201- 1215.
5. Novic AC, Streem SB.Surgery of the kidney.In Walsh PC, Retik AB, Vaughan ED, Wein AJ. 7th ed.Ed. Campbell`s. Urology.Philadelphia: WB Saunders. 1997; p. 301-732
6. Safirstein R, Andrade L, Vieira JM. Acetylcysteine and nephrotoxic effects of radiographic contrast agents-a new use for an old drug. N Engl J Med. 2000;343 (3): 180-4.
7. Padanilam BJ. Cell death induced by acute renal injury: a perspective on the contributions of apoptosis and necrosis. Am J Physiol Renal Physiol. 2003;284: F608F627.
8. Gobé G, Willgoss D, Hogg N, Schoch E, Endre Z. Cell survival or death in renal tubular epithelium after ischemia-reperfusion injury. Kidney Int. 1999;56(4): 1299-304.
9. Torres A, Conde C, Martín M, González JA, Gutiérrez V, Carrera S, et al. Prevención del daño renal tras isquemia aguda mediante la administración de PGE1. Estudio morfométrico. Angiología.2001;53(6): 381-392.
10. Isaka Y, Suzuki C, Abe T, Okumi M, Ichimaru N, Imamura R, et al. BcI-2 protects tubular epitelial cells from ischemia/reperfision injury by dual mechanisms. Transplant Proc. 2009;41(1): 52-4
11. Onem Y, Ipcioglu OM, Haholu A, Sen H, Aydinoz S, Suleymanoglu S, et al. Posttreatment with aminoguanidine attenuates renal ischemia/reperfusion injury in rats. Ren Fail. 2009;31(1): 50-3.
12. Sue YM, Cheng CF, Chang CC, Chou Y, Chen CH, Juan SH. Antioxidation and anti-inflammation by haem oxygenase-1 contribute to protection by tetramethylpyrazine against gentamicin-induced apoptosis in murine renal tubular cells. Nephrol Dial Transplant. 2009;24(3): 769-77.
13. Bi B, Guo J, Marlier A, Lin SR, Cantley LG. Erythropoietin expands a stromal cell population that can mediate renoprotection. Am J Physiol Renal Physiol. 2008;295(4): F1017-22.
14. Barrouillet M, Moiret A, Cambar J. Protective effects of polyphenols against cadmium-induced glomerular mesangial cell myocontracture. Arch Toxicol.1999;73:485-488.
15. Kontorschikova CN. Biochemical safety control in ozonetherapy of the Int. Proceedings XII Ozone World Congress of the Internathional Ozone Association. Ozone in Medicine. Lille, France. 1995;p.231-234.
16. Borrego A, Zamora ZB, González R, Menéndez S, Hernández F, Montero T, et al. Protection by ozone preconditioning is mediated by the antioxidant system in cisplatin-induced nephrotoxicity in rats.Mediat Inflamm.2004;13(1): 13-19.
17. Barber E, Menéndez S, León OS, Barber MO, Merino N, Calunga JL, et al. Prevention of renal injury after induction of ozone tolerance in rats submitted to warm ischaemia. Mediat Inflamm. 1999;8: 37-41.
18. Chen H, Xing B, Liu X, Zhan B, Zhou J, Zhu H, et al. Ozone oxidative preconditioning inhibits inflammation and apoptosis in a rat model of renal ischemia/reperfusion injury. Eur J Pharmacol.2008;581: 306-314.
19. León OS, Menéndez S, Merino N, Castillo R, Sam S, Pérez L, et al. Ozone oxidative preconditioning: a protection against celluar damage by free radicals. Med Inflamm. 1998;7: 289-294.
20. Peralta C, León OS, Xaus C, Bartrons R Gelpi E, Roselló-Catafau J, et al.Effect ozone treatment on reactive oxygen species and adenosine production during hepatic ischemica-reperfusion. Free Rad Res.2000;33: 595-605.
21. Spurr A.R. A low-viscosity epoxy resin embedding medium for electron microscopy. J.Ultrastruct Res. 1969;26: 31.
22. Del Cerro M., Cogen J., Del Cerro C. Stevenel Blue, an excellent stain for optical microscopical study of plastic embedded tissue.Microsc Acta1980;83: 117.
23. Wayne Rasband. ImageJ: A public domain Java image processing program. National Institute of Mental Health, Bethesda, Maryland, USA. http://rsb.info.nih.gov/ij/. Consultado: 27 de mayo de 2008.
24. Agterberg MJ, Versnel H, de Groot JC, Smoorenburg GF, Albers FW, Klis SF. Morphological changes in spiral ganglion cells after intracochlear application of brain-derived neurotrophic factor in deafened guinea pigs. Hear Res. 2008;244(1-2): 25-34.
25. Hernández F. La ozonoterapia y la peroxidación de lípidos. Relaciones y efectos en la ateroesclerosis. Rev CENIC Ciencias Biol. 1993;24(3): 25.
26. Peralta C, León OS, Xaus C, Prats N, Jalil EC, Sala-Planell E, et al.Protective effect of ozone treatment on the injury associated with hepatic ischemia-reperfusion: Antioxidant- Proxidant balance. Free Rad Res.1999;31: 191-196.
27. Candelario-Jalil E, Mohammed-Al-Dalain S, Fernández OS, Menéndez S, Pérez-Davison G, Merino N, et al. Oxidative preconditioning affords protection against carbon tetrachloride-induced glycogen depletion and oxidative stress in rats. J Appl Toxicol. 2001;21: 297-301.
28. Ajamieh HH, Berlanga J, Merino N, Sánchez G, Carmona A, Menéndez-Cepero S, et al. Role of protein synthesis in the protection conferred by ozone-oxidative-preconditioning in hepatic ischaemia/reperfusion. Transpl Int.2005;18 (5): 604-612.
29. Calunga JL. Precondicionamiento oxidativo con ozono en el daño renal por isquemia-reperfusion. [Tesis presentada en opción del título de Doctor en Ciencias Médicas]. Ciudad de la Habana, Instituto de Ciencias Básicas y Preclínicas ¨Victoria de Girón¨; enero, 2009.
|
|
|
|
- Rosa María Coro-Antich - CUBA (30/10/2009 18:46:39)
- Mª Piedad Ramirez Fernandez - ESPAÑA (03/11/2009 9:27:48)
- IGNACIO J. CLAROS GONZÁLEZ - ESPAÑA (14/11/2009 12:15:14)
- ana maria calvo niebla - ESPAÑA (21/11/2009 10:52:15)
|
|
|
|
|
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 11:37:37







.jpg)